Clear Sky Science · he
DCTPP1 מארגן את הדינמיקה של מאגרי dCTP ויציבות mtDNA בתאים רדומים
שמירה על תחנות הכוח של התא בריאות
כל תא בגופנו מסתמך על "תחנות כוח" פנימיות זעירות הנקראות מיטוכונדריה כדי לייצר אנרגיה. מבנים אלה נושאים את הגנום הקטן שלהם, DNA מיטוכונדריאלי (mtDNA), שצריך להיות מועתק ומתוקן לאורך כל החיים, גם בתאים שהפסיקו להתחלק. מחקר זה חושף כיצד אנזים שרוב האנשים לא מכירים, DCTPP1, מסייע לבקרה על אבני הבניין הכימיות הדרושות ל-mtDNA ומראה שכיוון פעילות האנזים הזה עשוי לסייע בטיפול במחלות נדירות שבהן ה-DNA המיטוכונדריאלי מדולל בצורה מסוכנת.
אבני הבניין של החיים באיזון
DNA נבנה מארבע "לבני" כימיות הידועות כדאוקסינוקלאוטידים, ותאים חייבים לשמור על יחס נכון ביניהן. יותר מדי או מעט מדי מסוג אחד עלול לפגוע ב-DNA ולסכן את הישרדות התאים. בתאים שאינם מתחלקים, או בתאים ברדומה (quiescent), הגרעין ברובו "מבחינת העתקת DNA" במצב מנוחה, אך המיטוכונדריה עדיין זקוקה לאספקה רציפה של לבנים אלה כדי לתחזק את ה-DNA שלה. החוקרים התמקדותו ב-DCTPP1, אנזים שמפרק לבנה ספציפית, dCTP, ובחנו כיצד הוא פועל בפיברובלסטים של ריאות אנושיות ברדומה — מודל מקובל לחקר הומאוסטזיס מיטוכונדריאלי.
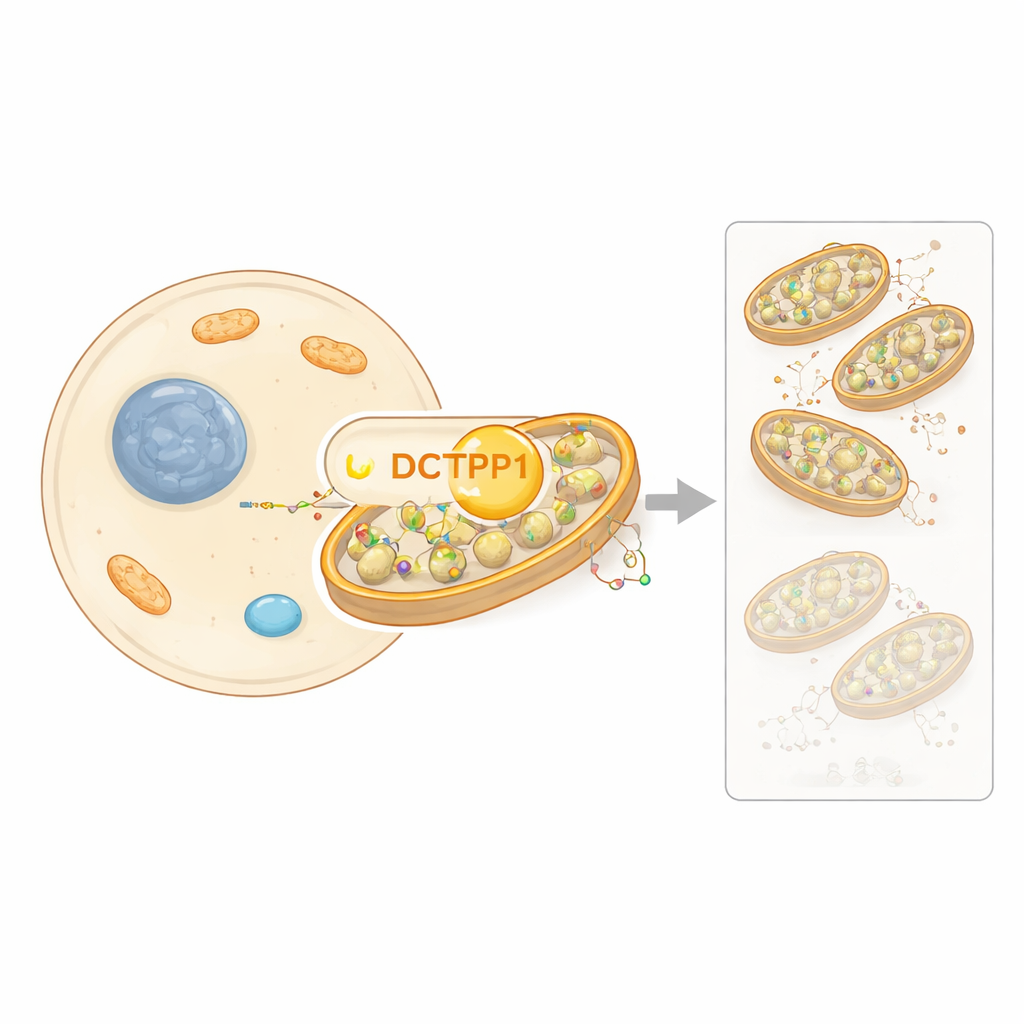
כשהתאים במנוחה, DCTPP1 עובר לתחנות הכוח
על ידי רעבון התאים מסרום הצמיחה, הצוות דחק אותם למצב מנוחה ממושך בלי להרוג אותם. לאחר מכן מדדו לוח של אנזימים שמייצרים, ממחזרים או הורסים אבני בניין של DNA. רבים מהאנזימים הקשורים לסינתזה המונית של DNA הופחתו, כפי שציפו. באופן בולט, הם גילו שה-DCTPP1 שעדיין הוצג בתא שינה את מיקומו: במקום להיות מפוזר בין הגרעין והציטוזול, רובו כעת ישב בתוך המיטוכונדריה. ממצא זה מרמז שבתאים ברדומה DCTPP1 עלול להתמחות בניהול מאגר dCTP מקומי ממש במקום שבו מתבצעת שכפול ה-mtDNA.
הסרת מעצור משנה את מאגרי הנגזרות הכימיות
כדי לבדוק את תפקידו של DCTPP1 השתמשו המדענים ב-RNA התערבותי קטן (siRNA) להוריד משמעותית את רמותיו גם בתאים מתחלקים וגם בתאים ברדומה. בתאים מתחלקים הדבר הוביל לצמיחה איטית יותר ולעלייה ב-dCTP וגם בלבנה אחרת, dTTP. בתאים ברדומה, איבוד DCTPP1 גרם לעיצוב מחודש של המאגר הכימי באופן אפילו דרמטי יותר: dCTP ו-dGTP הפכו לשופעים במיוחד, כאשר dGTP שלט בתערובת הכוללת. שינויים אלה אישרו ש-DCTPP1 פועל בדרך כלל כמעצור על סוגים מסוימים של נוקלאוטידים ורמזו שלהרפות מעצור זה עשויה להיות השפעה על יכולת המיטוכונדריה לתחזק את ה-DNA שלה.
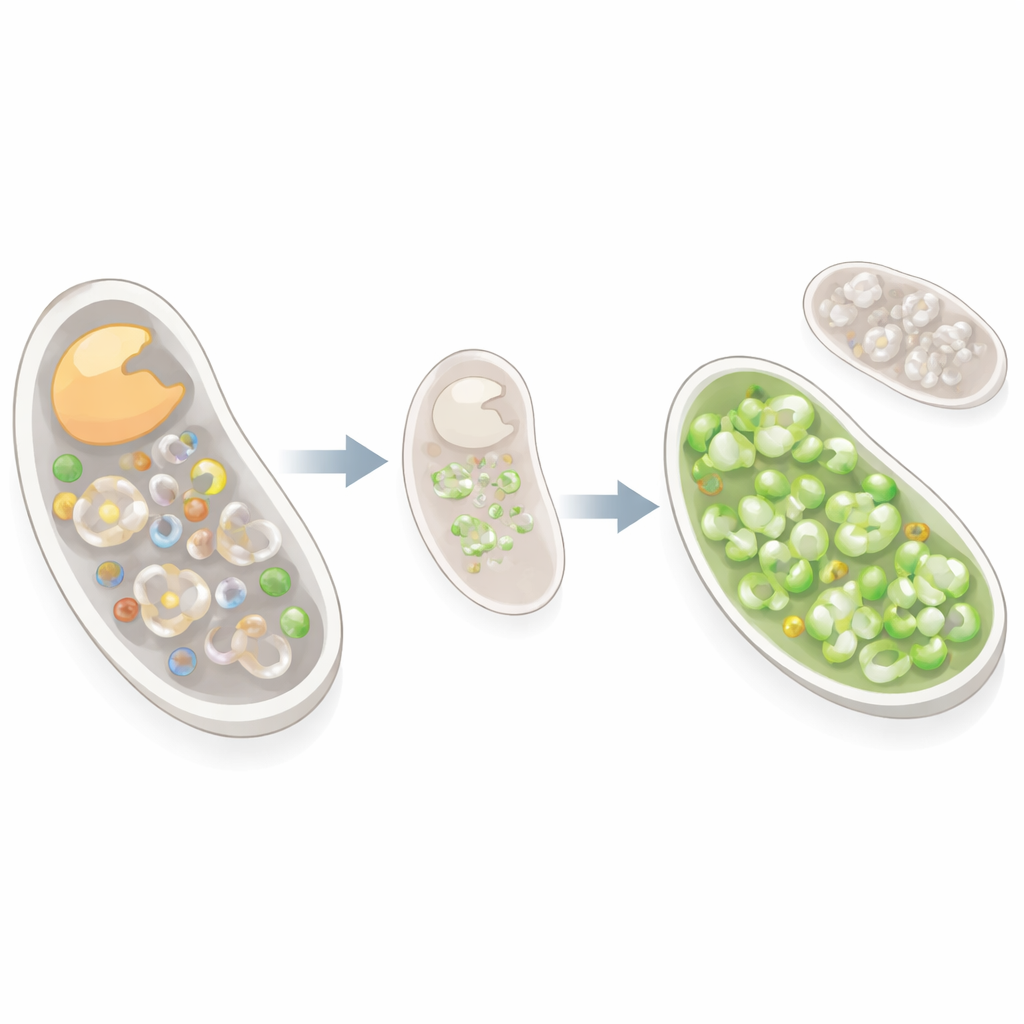
הגנה על ה-DNA המיטוכונדריאלי תחת לחץ
הצוות הביט לאחר מכן ישירות בתפקוד המיטוכונדרי וביציבות הגנום. בעזרת צבענים פלואורסצנטיים וטכניקות תיוג DNA הם הראו שבתאים ברדומה הורדת DCTPP1 למעשה שימרה את ביצועי המיטוכונדריה והגדילה את העתקי ה-mtDNA. לאחר מכן פנו לדגם מעבדה של מחלה אנושית חמורה, mitochondrial neurogastrointestinal encephalomyopathy (MNGIE), שבה ליקוי בפירוק תימידין מייצר הפרעה באיזון אבני הבניין של ה-DNA ומוביל לדילול mtDNA. על ידי העמסת תאים בתימידין, החוקרים שיחזרו את חוסר האיזון הזה: רמות ה-mtDNA ירדו, אך ניתן היה לשחזרן או על ידי הוספת דאוקסיציטידין או על ידי דיכוי DCTPP1, שהרחיב את מאגר ה-dCTP והציל את ה-mtDNA.
מטרה תרופתית עם הבטחה טיפולית
לבסוף, המדענים בחנו מעכב מולקולרי קטן של DCTPP1, TH1217, בתאים ברדומה. במינונים נמוכים, תרכובת זו הייתה רעילה במידה קטנה בלבד אך הגדילה את מספר העתקי ה-mtDNA, בעיקר תחת העמסת תימידין המדמה MNGIE. מדידות ביוכימיות הראו כי TH1217 הגביר את רמות ה-dCTP בהתאם להשפעתו המגוננת על ה-DNA המיטוכונדריאלי. יחד, ממצאים אלה מציעים כי השתקה מדודה של פעילות DCTPP1 יכולה לאזן מחדש את התערובת הנוקלאוטידית המיטוכונדריאלית ולעזור להגן על ה-mtDNA מפני דילול.
מה משמעות הדברים עבור מטופלים
במילים פשוטות, עבודה זו מזהה את DCTPP1 כאמצעי מולקולרי שתאים משתמשים בו כדי לכוונן בעדינות את אספקת אבני הבניין של ה-DNA בתוך המיטוכונדריה, במיוחד ברקמות ארוכות־חיים שאינן מתחלקות כמו מוח ושריר. כאשר dCTP בחסר, כפי שקורה בתסמונות דילול DNA מיטוכונדריאלי כמו MNGIE, הקטנת פעילות המנע עשויה לאפשר לתא לשקם את המלאי ולתחזק טוב יותר את ה-mtDNA. בעוד שדרושים מחקרים נוספים, כולל ניסויים בבעלי חיים ובדיקות בטיחות, מטרה של DCTPP1 יכולה להפוך לאסטרטגיה טיפולית חדשה לייצוב "תחנות הכוח" של התא במחלות המונעות על ידי אובדן mtDNA.
ציטוט: Fernández, B., Pérez-Moreno, G., Martínez-Arribas, B. et al. DCTPP1 orchestrates dCTP pool dynamics and mtDNA stability in quiescent cells. Cell Death Dis 17, 404 (2026). https://doi.org/10.1038/s41419-026-08632-1
מילות מפתח: DNA מיטוכונדריאלי, מטבוליזם נוקלאוטידים, DCTPP1, MNGIE, מחלה מיטוכונדריאלית