Clear Sky Science · ru
Пониженный RTN3 стабилизирует DHCR7, вызывая холестерин-зависимое прогрессирование опухоли и нечувствительность к ингибиторам MEK при раке щитовидной железы
Почему это важно для пациентов
Рак щитовидной железы обычно хорошо поддаётся лечению, но небольшая, но упрямая часть опухолей учится игнорировать современные таргетные препараты и продолжает расти. В этом исследовании показано, что малоизвестный внутриклеточный белок RTN3 помогает сдерживать рост опухоли и устойчивость к лекарствам, ограничивая производство холестерина. Полученные данные позволяют предположить, что недорогой класс сердечных препаратов — статины — может быть перепрофилирован для усиления действия ключевого противоракового препарата у пациентов с низким уровнем RTN3 в опухоли.
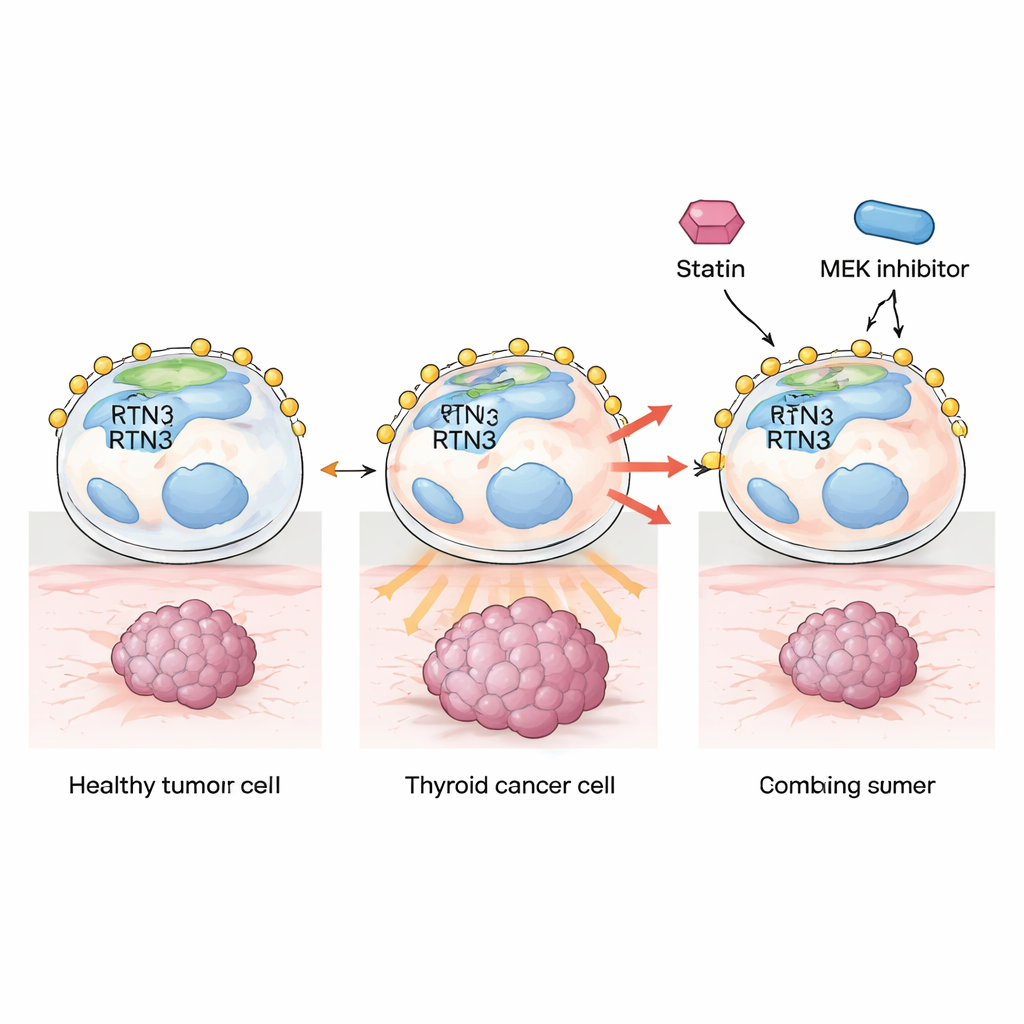
Скрытый тормоз внутри клеток щитовидной железы
Рак щитовидной железы — самый распространённый рак эндокринной системы, и большинство пациентов успешно лечатся операцией, радиоактивным йодом и таргетной терапией. Тем не менее у 5–15% развивается агрессивное заболевание, которое рецидивирует, даёт метастазы или теряет чувствительность к лечению. Авторы сосредоточились на белках эндоплазматического ретикулума — мембранной сети в клетке, где синтезируются многие строительные блоки, включая липиды и холестерин. Один из таких белков, RTN3, предполагали как фактор, влияющий на поведение опухолей, но он не изучался в контексте рака щитовидной железы. Анализ баз данных пациентов и образцов опухолей показал, что уровни RTN3 значительно ниже в раковых тканях щитовидной железы по сравнению с нормой, и особенно низки в более продвинутых опухолях. У пациентов с низким RTN3 регистрировалась худшая безрецидивная выживаемость, что указывает на RTN3 как на естественный «тормоз» прогрессирования болезни.
Когда тормоз даёт сбой, опухоли ускоряются
Чтобы выяснить роль RTN3, команда удаляла его в клеточных линиях рака щитовидной железы с помощью генетических инструментов и, наоборот, создавали клетки с избыточной экспрессией RTN3. Клетки без RTN3 образовывали больше колоний, делились быстрее и легче мигрировали в стандартных лабораторных тестах, тогда как клетки с дополнительным RTN3 вели себя противоположно и замедлялись. У мышей опухоли, сформированные из клеток, лишённых RTN3, росли быстрее и хуже контролировались лечением по сравнению с опухолями с нормальным RTN3. В совокупности эти эксперименты показывают, что RTN3 ведёт себя как супрессор опухоли: при его потере раковые клетки получают преимущество в росте и распространении.
Холестерин как «топливо» для сигнальных путей роста
Далее исследователи выясняли, как RTN3 реализует своё влияние. С помощью методов «ловли» белков они обнаружили, что RTN3 связывается с DHCR7 — ключевым ферментом на позднем этапе пути синтеза холестерина. RTN3 способствует пометке DHCR7 для разрушения, снижая его уровни. Когда RTN3 уменьшен, DHCR7 становится более стабильным, синтез холестерина растёт, и в мембранах клеток накапливается больше холестерина. Такая обогащённая мембранная среда усиливает сигнализацию по пути EGFR–ERK — важному маршруту, который побуждает раковые клетки к росту и делению. Команда показала, что снижение DHCR7 или блокирование синтеза холестерина статином симвастатином может обратить вспять повышенный рост и миграцию, наблюдаемые при отсутствии RTN3.
Почему некоторые опухоли не реагируют на ингибиторы MEK
Многие раки щитовидной железы лечат препаратами, блокирующими MEK — ключевое звено в том же ERK-пути роста. Авторы протестировали три таких препарата и обнаружили, что удаление RTN3 снижает чувствительность раковых клеток ко всем ним, при этом наибольший эффект наблюдался для ингибитора MEK мирдаметиниба. В клетках и в опухолях у мышей мирдаметиниб обычно снижал активность ERK и замедлял пролиферацию, но этот эффект значительно ослабевал при отсутствии RTN3. Важно, что подавление DHCR7 или добавление симвастатина восстанавливало значительную часть утраченной чувствительности к препарату как в культурах клеток, так и у мышей. Опухоли с низким RTN3, ранее резистентные к мирдаметинибу, уменьшались в размере при добавлении симвастатина и содержали меньше активно делящихся клеток.
Что это может значить для будущей помощи пациентам
Для непрофессионалов ключевая мысль такова: некоторые раки щитовидной железы становятся более агрессивными и устойчивыми к лекарствам за счёт наращивания холестерина внутри клеток, и это обусловлено потерей внутреннего защитного белка RTN3. Контролируя фермент синтеза холестерина DHCR7, RTN3 обычно помогает ослаблять сигналы роста. При дефиците RTN3 избыток холестерина усиливает эти сигналы и снижает эффективность MEK-блокаторов, таких как мирдаметиниб. Поскольку статины уже безопасно снижают холестерин у миллионов людей, сочетание статина (например, симвастатина) с ингибитором MEK может предложить практическую новую стратегию для пациентов с опухолями с низким RTN3, которые плохо поддаются лечению.
Цитирование: Ren, A., Feng, N., Yang, T. et al. Declined RTN3 stabilizes DHCR7 to induce cholesterol-dependent tumor progression and MEK inhibitors insensitivity in thyroid cancer. Cell Death Dis 17, 306 (2026). https://doi.org/10.1038/s41419-026-08538-y
Ключевые слова: рак щитовидной железы, обмен холестерина, устойчивость к лекарствам, статины, ингибиторы MEK