Clear Sky Science · nl
Verminderde RTN3 stabiliseert DHCR7 en veroorzaakt cholesterolf-afhankelijke tumorprogressie en ongevoeligheid voor MEK-remmers bij schildklierkanker
Waarom dit belangrijk is voor patiënten
Schildklierkanker is gewoonlijk goed behandelbaar, maar een hardnekkig deel van de tumoren leert moderne gerichte medicijnen te negeren en blijft doorgroeien. Deze studie onthult hoe een weinig bekend eiwit in cellen, RTN3, bijdraagt aan het remmen van tumorgroei en medicijnresistentie door de aanmaak van cholesterol te beperken. De bevindingen suggereren dat een goedkope klasse hartmedicijnen, statines, hergebruikt zou kunnen worden om de werking van een belangrijk kankermedicijn te versterken bij patiënten waarvan de tumoren lage RTN3-niveaus hebben.
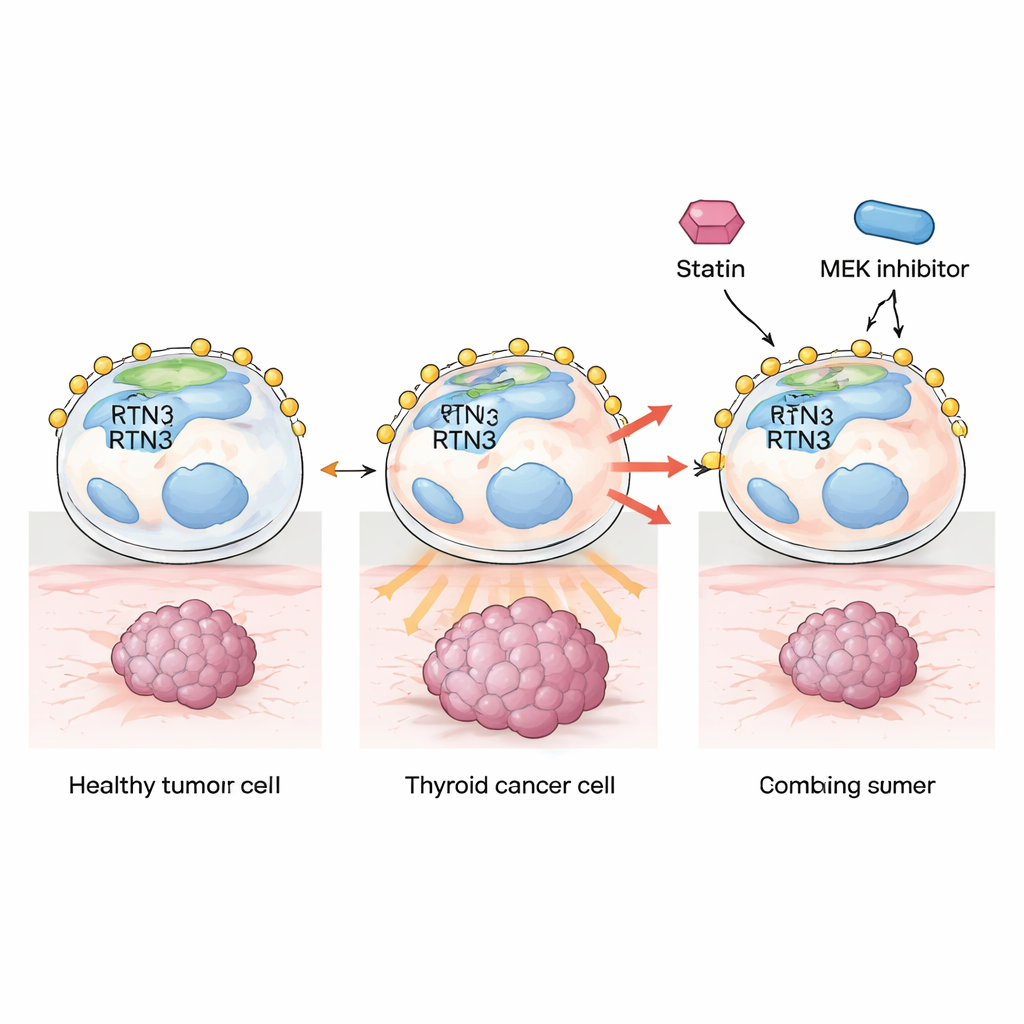
Een verborgen rem in schildkliercellen
Schildklierkanker is de meest voorkomende kanker van het hormoonsysteem en de meeste patiënten doen het goed met chirurgie, radioactief jodium en gerichte middelen. Toch ontwikkelt 5–15% een agressieve ziekte die terugkeert, uitzaait of niet meer op behandeling reageert. De auteurs concentreerden zich op eiwitten in het endoplasmatisch reticulum, een membraannetwork in cellen waar veel bouwstoffen, waaronder vetten en cholesterol, worden gemaakt. Eén van die eiwitten, RTN3, werd verdacht invloed te hebben op kankergedrag maar was niet bestudeerd in schildkliertumoren. Door patiëntendatabases en tumormonsters te analyseren, vonden de onderzoekers dat RTN3-niveaus duidelijk lager zijn in schildklierkankers dan in normaal schildklierweefsel, en vooral laag in meer gevorderde tumoren. Patiënten met lage RTN3 hadden een slechtere progressievrije overleving, wat wijst op RTN3 als een natuurlijke rem op ziekteverslechtering.
Als de rem faalt, versnellen tumoren
Om te onderzoeken wat RTN3 doet, verwijderde het team het uit schildklierkankercellijnen met genbewerkingstools en creëerde ook cellen die extra RTN3 produceren. Cellen zonder RTN3 vormden meer kolonies, deelden sneller en migreerden gemakkelijker in standaard laboratoriumtests, terwijl cellen met extra RTN3 het tegenovergestelde deden en vertraagden. In muizen groeiden tumoren die waren opgebouwd uit RTN3-deficiënte cellen groter en werden ze minder goed onder controle gehouden door behandeling dan tumoren met normaal RTN3. Samen tonen deze experimenten aan dat RTN3 zich gedraagt als een tumorsuppressor: wanneer het verloren gaat, krijgen kankercellen een groeien verspreidingsvoordeel.
Cholesterol als brandstof voor groeisignalen
De volgende vraag was hoe RTN3 deze controle uitoefent. Met eiwit‑vangtechnieken ontdekten de onderzoekers dat RTN3 bindt aan DHCR7, een sleuteleiwit dicht bij het eind van de cholesterolaanmaakroute. RTN3 bevordert het taggen van DHCR7 voor afbraak, waardoor de niveaus dalen. Wanneer RTN3 verminderd is, wordt DHCR7 stabieler, stijgt de cholesterolproductie en hoopt zich meer cholesterol op in celmembranen. Deze verrijkte membraanomgeving bevordert sterke signalering via de EGFR–ERK-route, een belangrijke weg die kankercellen aanzet tot groei en deling. Het team liet zien dat het verlagen van DHCR7, of het blokkeren van cholesterolproductie met de statine Simvastatine, de extra groei en migratie kon omkeren die werden waargenomen wanneer RTN3 ontbrak.
Waarom sommige tumoren MEK-remmers afslaan
Veel schildklierkankers worden behandeld met middelen die MEK blokkeren, een belangrijke schakel in dezelfde ERK-groeiroute. De auteurs testten drie van zulke middelen en vonden dat het verwijderen van RTN3 kankercellen minder gevoelig maakte voor alle drie, met het sterkste effect voor de MEK-remmer Mirdametinib. In cellen en in muistentumoren verlaagde Mirdametinib normaal gesproken ERK-activiteit en vertraagde het de proliferatie, maar dit voordeel was sterk verzwakt wanneer RTN3 ontbrak. Belangrijk is dat het terugschakelen van DHCR7 of het toevoegen van Simvastatine veel van de verloren gevoeligheid voor het medicijn herstelde, zowel in kweek als in muizen. Tumoren met weinig RTN3 die resistent waren tegen Mirdametinib krompen meer wanneer Simvastatine werd toegevoegd en toonden minder cellen die actief deelden.
Wat dit kan betekenen voor toekomstige zorg
Voor niet‑specialisten is de kernboodschap dat sommige schildklierkankers gevaarlijker en medicijnresistenter worden door het opvoeren van cholesterol in hun cellen, en dat dit wordt aangedreven door verlies van een interne beschermende eiwit, RTN3. Door het cholesterol‑producerende enzym DHCR7 in toom te houden, helpt RTN3 normaal gesproken groeisignalen te dempen. Wanneer RTN3 schaars is, versterken extra hoeveelheden cholesterol die signalen en verzwakken ze het effect van MEK-blokkers zoals Mirdametinib. Omdat statines al veilig het cholesterol verlagen bij miljoenen mensen, kan het combineren van een statine zoals Simvastatine met een MEK-remmer een praktische nieuwe strategie bieden voor patiënten wiens tumoren lage RTN3 hebben en moeilijk te behandelen zijn.
Bronvermelding: Ren, A., Feng, N., Yang, T. et al. Declined RTN3 stabilizes DHCR7 to induce cholesterol-dependent tumor progression and MEK inhibitors insensitivity in thyroid cancer. Cell Death Dis 17, 306 (2026). https://doi.org/10.1038/s41419-026-08538-y
Trefwoorden: schildklierkanker, cholesterolmetabolisme, medicatieresistentie, statines, MEK-remmers