Clear Sky Science · pt
Solvatocrômico, espectroscópico, cálculos DFT, estudos antimicrobianos e de docking de novas quelas de Fe(III), Co(II) e Ni(II) contendo 1,2,4-triazina
Novas Moléculas que Combatem Germes e Emitem Luz
Químicos criaram uma família de pequenas moléculas à base de metal que tanto podem brilhar sob certas condições quanto retardar o crescimento de microrganismos nocivos. Esses materiais de dupla função são interessantes porque sugerem futuros fármacos que poderiam ser rastreados no corpo por meio de sua luminescência, ou revestimentos inteligentes que detectam e eliminam bactérias e fungos em dispositivos médicos.
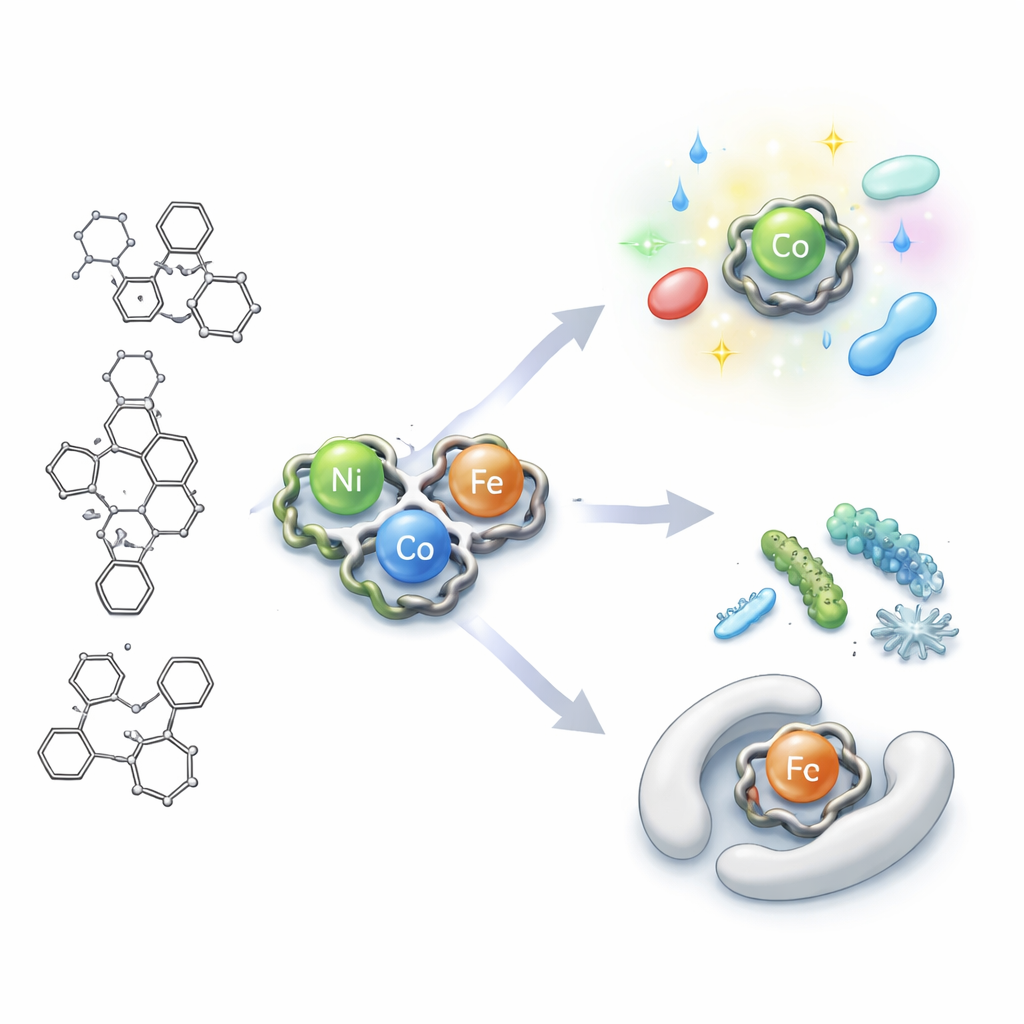
Construindo Pequenas Gaiolas Metálicas
A equipe partiu de uma estrutura de base carbônica conhecida por sua rica atividade biológica e pela capacidade de coordenar metais. Eles a modificaram para criar uma unidade semelhante a uma garra (um ligante hidrazona–triazina) que pode se ligar a íons metálicos em três pontos, usando dois átomos de nitrogênio e um de oxigênio. Quando esse ligante foi combinado com sais de níquel, cobalto ou ferro, as peças se juntaram formando três novas “quelas” metálicas: uma com níquel, outra com cobalto e outra com ferro. Uma bateria de testes — incluindo espectroscopia no infravermelho e na luz visível, medidas magnéticas e análise térmica — revelou como os átomos estão arranjados. A versão com níquel adota uma forma aproximadamente tetraédrica, enquanto as versões com cobalto e ferro preferem uma geometria octaédrica ao redor dos centros metálicos.
De Nanopartículas a Materiais Sensíveis à Luz
Usando difração de raios X e microscopia eletrônica de transmissão, os pesquisadores descobriram que os complexos formam partículas com apenas alguns bilionésimos de metro de diâmetro, com o composto de níquel aparecendo como pequenas esferas e cubos. Todos os três complexos emitem luz e alteram sua resposta de cor dependendo do líquido ao redor. Ao registrar como seus sinais de absorção e fluorescência mudam em solventes de polaridade distinta, os autores puderam estimar como a distribuição de carga interna varia entre os estados fundamental e excitado. Os dados mostram que, quando essas moléculas são excitadas, sua carga interna se desloca de forma significativa, tornando-as mais polares e mais facilmente influenciáveis pelo ambiente. Esse comportamento é valioso para sensores e dispositivos ópticos, pois significa que os complexos podem transformar mudanças sutis no ambiente em variações visíveis de cor ou intensidade.
Investigando o Comportamento com Modelos Computacionais
Para complementar os experimentos, a equipe recorreu a cálculos quântico-químicos. Utilizaram teoria do funcional da densidade para otimizar as conformações dos complexos e examinar os orbitais moleculares mais ocupados e menos ocupados, que determinam como os elétrons se movem durante reações e absorção de luz. O complexo de ferro mostrou a menor lacuna de energia entre esses orbitais, sugerindo que é o mais reativo quimicamente dos três. Os modelos também mapearam regiões de carga negativa e positiva ao longo de cada molécula, destacando os mesmos átomos de nitrogênio e oxigênio identificados experimentalmente como pontos de contato chave. Importante, os valores calculados de polarizabilidade e hiperpolarizabilidade indicam que esses complexos respondem fortemente a campos elétricos, muito mais do que um composto de referência padrão. Isso os torna promissores para aplicações ópticas não lineares, como chaves fotônicas avançadas e componentes de processamento de sinais.
Desafiando Bactérias e Fungos
Os pesquisadores então testaram quão bem os novos complexos poderiam retardar ou impedir o crescimento de microrganismos comuns causadores de doenças: as bactérias Staphylococcus aureus e Escherichia coli, e o fungo Candida albicans. O ligante livre isoladamente mostrou efeitos fracos, mas suas quelações metálicas foram muito mais potentes. O complexo de ferro, em particular, produziu grandes zonas de inibição onde os microrganismos não cresceram e agiu em concentrações relativamente baixas, com forte atividade contra bactérias e fungos. Para entender o motivo, a equipe utilizou simulações de docking molecular, posicionando virtualmente cada complexo no bolso ativo de uma enzima bacteriana crucial para a síntese de ácidos graxos. O complexo de ferro acomodou-se mais ajustadamente nesse bolso e formou as interações simuladas mais fortes, espelhando seu desempenho antimicrobiano superior observado em laboratório.
O Que Esses Achados Podem Significar
Em conjunto, o trabalho apresenta três novos complexos metálicos em escala nanométrica que combinam forte atividade antimicrobiana com respostas sensíveis baseadas em luz e elevada estabilidade térmica. Para um público não especialista, a mensagem principal é que pequenas mudanças em como as “garras” orgânicas prendem íons metálicos podem ajustar não apenas a forma como essas partículas brilham, mas também quão efetivamente interferem em processos vitais de bactérias e fungos. O complexo contendo ferro destaca-se como o melhor desempenho geral, apontando para materiais futuros que podem simultaneamente detectar o ambiente, desempenhar funções ópticas e atuar como agentes antimicrobianos direcionados na medicina ou em revestimentos inteligentes.
Citação: Abdelrhman, E.M., Samy, F., Adly, O.M. et al. Solvatochromic, spectroscopic, DFT calculations, antimicrobial and docking studies of new Fe(III), Co(II), and Ni(II) chelates containing 1,2,4-triazine. Sci Rep 16, 13406 (2026). https://doi.org/10.1038/s41598-026-48416-3
Palavras-chave: quelas metálicas, antimicrobianos luminiscentes, hidrazona de triazina, materiais ópticos não lineares, docking molecular