Clear Sky Science · de
Solvatochromische, spektroskopische, DFT-Berechnungen, antimikrobielle und Docking-Studien neuer Fe(III)-, Co(II)- und Ni(II)-Chelate mit 1,2,4-Triazin
Neue Moleküle, die Keime bekämpfen und leuchten
Chemiker haben eine Familie winziger metallbasierter Moleküle entwickelt, die unter bestimmten Bedingungen leuchten und gleichzeitig das Wachstum schädlicher Mikroben verlangsamen können. Diese zweckgebundenen Materialien sind interessant, weil sie auf künftige Medikamente hinweisen, die durch ihr Leuchten im Körper verfolgt werden können, oder auf intelligente Beschichtungen, die Bakterien und Pilze auf medizinischen Geräten sowohl erkennen als auch abtöten.
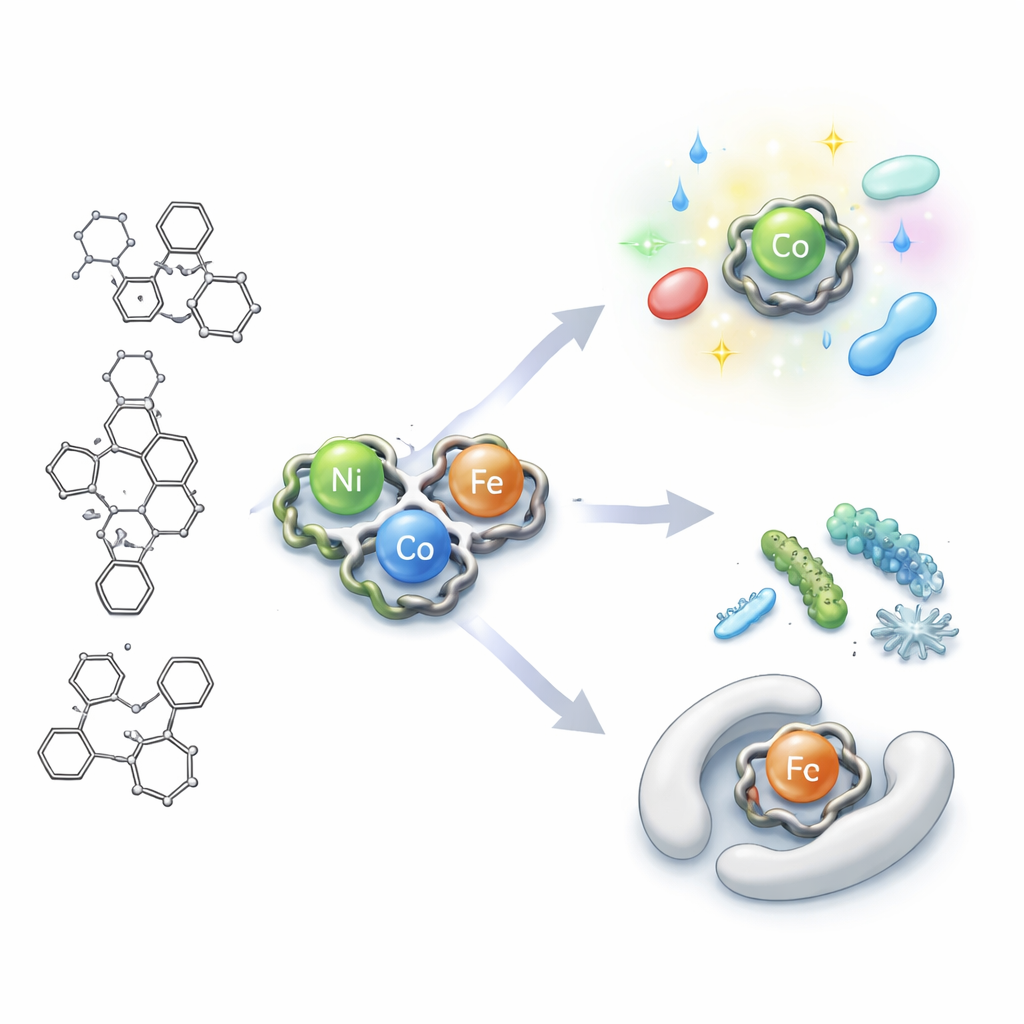
Winzige Metallkäfige bauen
Das Team begann mit einem kohlenstoffbasierten Gerüst, das für seine ausgeprägte biologische Aktivität und seine Fähigkeit, Metalle zu binden, bekannt ist. Sie modifizierten es, um eine klauenähnliche Einheit (ein Hydrazon–Triazin-Ligand) zu erzeugen, die an drei Stellen an Metallionen andocken kann und dabei zwei Stickstoff- und ein Sauerstoffatom nutzt. Beim Mischen dieser „Klaue“ mit Nickel-, Kobalt- oder Eisen-Salzen setzten sich die Bausteine zu drei neuen Metallchelaten zusammen: einem mit Nickel, einem mit Kobalt und einem mit Eisen. Eine Reihe von Tests — darunter Infrarot- und Sichtbarkeitspektroskopie, Magnetismus und Thermalanalysen — zeigte die Anordnung der Atome. Die Nickelversion nimmt annähernd eine vier-eckige (tetraedrische) Form an, während die Kobalt- und Eisenvarianten eine sechseckige (oktaedrische) Anordnung um die Metallzentren bevorzugen.
Von Nanopartikeln zu lichtempfindlichen Materialien
Mithilfe von Röntgenbeugung und Transmissions-Elektronenmikroskopie fanden die Forscher heraus, dass die Komplexe Partikel von nur wenigen Milliardstel Metern Durchmesser bilden, wobei die Nickelsubstanz als winzige Kugeln und Würfel erscheint. Alle drei Komplexe emittieren Licht und ändern ihre Farbreaktion abhängig von der umgebenden Flüssigkeit. Durch Aufzeichnen, wie sich ihre Absorptions- und Fluoreszenzsignale in Lösungsmitteln mit unterschiedlicher Polarität verschieben, konnten die Autoren abschätzen, wie sich die interne Ladungsverteilung zwischen Grund- und angeregtem Zustand verändert. Die Daten zeigen, dass bei Anregung eine erhebliche Ladungsverschiebung innerhalb der Moleküle stattfindet, wodurch sie polarer werden und stärker von ihrer Umgebung beeinflusst werden. Dieses Verhalten ist für Sensoren und optische Geräte wertvoll, weil es bedeutet, dass die Komplexe subtile Umweltveränderungen in sichtbare Farb- oder Helligkeitsänderungen übersetzen können.
Verhalten mit Computermodellen untersuchen
Zur Ergänzung der Experimente wandte sich das Team quantenchemischen Berechnungen zu. Sie nutzten die Dichtefunktionaltheorie, um die Geometrien der Komplexe zu optimieren und die höchstbesetzten sowie die niedrigstunbesetzten Molekülorbitale zu untersuchen, die steuern, wie Elektronen bei Reaktionen und Lichtabsorption bewegt werden. Der Eisenkomplex zeigte die kleinste Energielücke zwischen diesen Orbitalen, was darauf hindeutet, dass er von den dreien chemisch am reaktivsten ist. Die Modelle kartierten außerdem Regionen negativer und positiver Ladung über jedem Molekül und hoben dieselben Stickstoff- und Sauerstoffatome hervor, die experimentell als Schlüsselpunkten identifiziert wurden. Wichtigerweise deuten die berechneten Werte für Polarisierbarkeit und Hyperpolarisierbarkeit darauf hin, dass diese Komplexe stark auf elektrische Felder reagieren, deutlich mehr als eine Standard-Referenzverbindung. Das macht sie vielversprechend für nichtlineare optische Anwendungen wie fortgeschrittene photonische Schalter und Signalverarbeitungsbauteile.
Bakterien und Pilze herausfordern
Anschließend testeten die Forscher, wie gut die neuen Komplexe das Wachstum häufiger Krankheitserreger hemmen können: die Bakterien Staphylococcus aureus und Escherichia coli sowie den Pilz Candida albicans. Der freie Ligand allein zeigte nur schwache Effekte, seine Metallchelate waren jedoch deutlich wirksamer. Besonders der Eisenkomplex erzeugte große Hemmhöfe, in denen Mikroben nicht wachsen konnten, und wirkte bei vergleichsweise niedrigen Konzentrationen mit starker Aktivität gegen sowohl Bakterien als auch Pilze. Um zu verstehen, warum, nutzte das Team molekulare Docking-Simulationen und platzierte jeden Komplex virtuell in die aktive Tasche eines bakteriellen Enzyms, das für die Fettsäuresynthese entscheidend ist. Der Eisenkomplex saß am engsten in dieser Tasche und bildete die stärksten simulierten Wechselwirkungen, was seine überlegene antimikrobielle Leistung im Labor widerspiegelt.
Was diese Ergebnisse bedeuten könnten
Insgesamt führt die Arbeit drei neue nanometergroße Metallkomplexe ein, die starke antimikrobielle Aktivität mit sensiblen lichtbasierten Reaktionen und robuster thermischer Stabilität kombinieren. Für Nichtfachleute ist die Kernbotschaft, dass kleine Änderungen darin, wie organische „Krallen“ Metallionen halten, nicht nur das Leuchten dieser Partikel, sondern auch deren Wirksamkeit bei der Störung lebenswichtiger Prozesse in Bakterien und Pilzen feinabstimmen können. Der eisenhaltige Komplex sticht als bester Allrounder hervor und weist auf künftige Materialien hin, die gleichzeitig ihre Umgebung detektieren, optische Funktionen erfüllen und als gezielte antimikrobielle Wirkstoffe in der Medizin oder als intelligente Beschichtungen dienen können.
Zitation: Abdelrhman, E.M., Samy, F., Adly, O.M. et al. Solvatochromic, spectroscopic, DFT calculations, antimicrobial and docking studies of new Fe(III), Co(II), and Ni(II) chelates containing 1,2,4-triazine. Sci Rep 16, 13406 (2026). https://doi.org/10.1038/s41598-026-48416-3
Schlüsselwörter: Metallchelate, lumineszente antimikrobielle Mittel, Triazin-Hydrazon, nichtlineare optische Materialien, molekulares Docking