Clear Sky Science · pt
Um modelo de atenção convolucional classifica variantes no número de cópias a partir de sequenciamento do exoma inteiro
Encontrando pistas ocultas em nosso DNA
Médicos usam cada vez mais o sequenciamento de DNA para buscar alterações genéticas que possam explicar doenças, mas algumas das pistas mais importantes não são mutações pontuais — são trechos de DNA que estão ausentes ou duplicados. Essas alterações, chamadas variantes no número de cópias, podem ser difíceis de detectar nos dados que a maioria dos hospitais já gera. Este estudo apresenta um novo modelo computacional que lê padrões ruidosos de cobertura do DNA e identifica essas peças ausentes ou extras com mais precisão e consistência entre diferentes máquinas de sequenciamento, potencialmente aprimorando uma ferramenta já comum na genética médica.
Por que DNA extra ou ausente importa
Variantes no número de cópias são segmentos de DNA que ocorrem em menos ou mais cópias do que o habitual. Um segmento pode ser totalmente deletado ou copiado várias vezes. Essas mudanças podem moldar traços cotidianos, influenciar o risco de condições como câncer ou distúrbios do desenvolvimento neurológico e afetar a evolução de populações humanas ao longo do tempo. Clinicamente, encontrar essas variantes é crucial tanto no diagnóstico de doenças raras quanto no perfil tumoral. Muitos pacientes já passam por sequenciamento do exoma inteiro, que foca nas partes do genoma que codificam proteínas. Aproveitar esses exames de exoma existentes para também detectar variantes no número de cópias pode tornar as análises genéticas mais informativas sem exigir ensaios adicionais mais caros.
Por que as ferramentas atuais têm dificuldade
Detectar variantes no número de cópias a partir de dados de exoma é tecnicamente desafiador. O processo de captura do exoma amostra o genoma de forma desigual, levando a uma profundidade de leitura recortada e ruidosa — quantas leituras de sequenciamento cobrem cada região. Ferramentas tradicionais suavizam esse ruído usando truques estatísticos e regras manuais, depois aplicam limites para decidir se uma região é normal, deletada ou duplicada. Embora úteis, esses métodos costumam falhar quando a cobertura é baixa, quando o sequenciamento é feito em máquinas ou químicas diferentes, ou quando padrões sutis em regiões vizinhas e entre cromossomos são relevantes. Como resultado, a sensibilidade pode diminuir, especialmente para eventos menores ou mais ruidosos, e o desempenho pode não se transferir bem entre laboratórios ou plataformas.

Uma nova maneira de ler sinais ruidosos
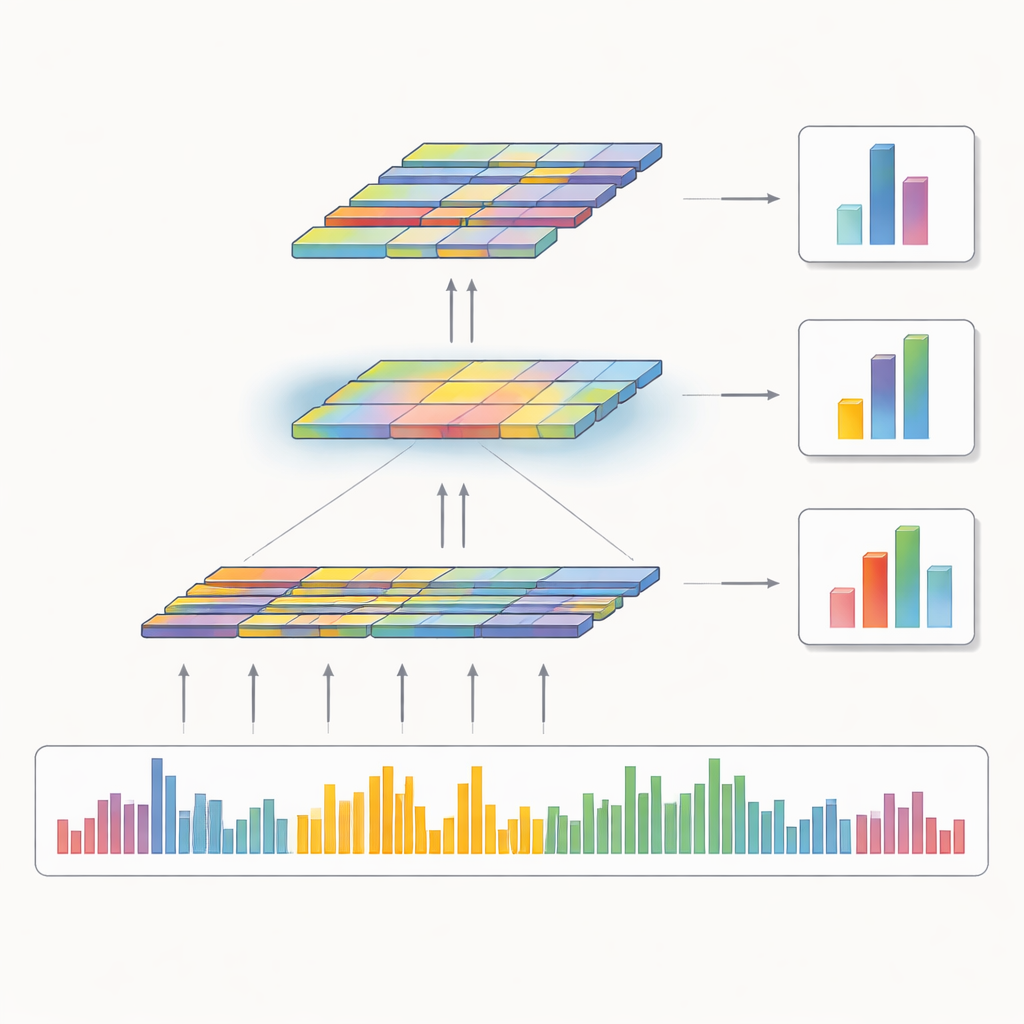
Os autores projetaram um modelo de aprendizado profundo, chamado CNN‑Att, que aprende diretamente a partir dos padrões brutos de cobertura em vez de se apoiar principalmente em regras fixas. Para cada segmento codificador de proteínas (um éxon), o modelo recebe um instantâneo padronizado da profundidade de leitura ao longo do éxon e de sua região circundante, junto com suas posições genômicas de início e fim. Também recebe uma etiqueta codificada indicando de qual cromossomo o éxon provém. Camadas convolucionais — popularizadas originalmente para análise de imagens — varrem esse sinal unidimensional para capturar formas locais no padrão de cobertura, como quedas que podem indicar deleções ou leves elevações sugerindo duplicações. Um mecanismo de atenção então destaca as características mais informativas, particularmente sinais fracos que podem corresponder a eventos pequenos ou ruidosos, antes que o modelo tome uma decisão em três vias: normal, deleção ou duplicação.
Quão bem o modelo performa
Para avaliar o CNN‑Att, os pesquisadores o treinaram em um grande conjunto de referência construído a partir do 1000 Genomes Project, onde dados de exoma estão emparelhados com rótulos inferidos a partir de um sequenciamento do genoma inteiro mais abrangente. Em um conjunto separado de 50 amostras de exoma reservadas para teste, o modelo classificou corretamente cerca de 83% das janelas de éxon no geral e mostrou forte capacidade de distinguir entre as três classes, com pontuações altas tanto nas curvas ROC (receiver‑operating) quanto nas de precisão‑recall. Deleções foram um pouco mais fáceis de detectar do que duplicações, refletindo o fato de que deleções normalmente deixam um sinal mais forte na cobertura. O modelo superou um baseline mais simples que conhecia apenas as coordenadas genômicas, indicando que estava realmente aprendendo a partir dos padrões de profundidade em vez de memorizar locais “quentes” onde variantes são comuns.
Confiável em diferentes sequenciadores
Como centros clínicos e de pesquisa usam uma variedade de máquinas de sequenciamento, uma ferramenta prática precisa se comportar bem entre plataformas. Os autores, portanto, testaram o CNN‑Att em dados de exoma da mesma amostra de DNA de referência sequenciada em quatro tecnologias principais: HiSeq 4000, NovaSeq 6000, MGISEQ 2000 e BGISEQ 500. Entre esses instrumentos diversos, a pontuação F1 geral do modelo — um equilíbrio entre precisão e sensibilidade — variou de 0,89 a 0,96, consistentemente mais alta que a de várias ferramentas tradicionais amplamente usadas. Em um experimento adicional, a equipe ajustou apenas as camadas finais de decisão do modelo usando um pequeno conjunto de sete amostras rotuladas cuidadosamente por especialistas. Mesmo com esses dados curados limitados, o ajuste fino aumentou notavelmente a sensibilidade para deleções e duplicações verdadeiras em amostras mantidas fora do treino, ao custo de alguns falsos positivos adicionais, uma troca frequentemente aceitável quando chamadas duvidosas podem ser verificadas com testes complementares.
O que isso significa para pacientes e pesquisa
Este trabalho mostra que uma abordagem de aprendizado profundo focada pode transformar a cobertura ruidosa e desigual do sequenciamento de exoma rotineiro em um detector mais confiável de segmentos de DNA ausentes e extras. O CNN‑Att alcança alta sensibilidade mantendo erros em níveis manejáveis e permanece robusto entre diferentes máquinas de sequenciamento, tornando‑o útil para estudos multi‑sítio e projetos populacionais em grande escala. Embora ainda precise de validação em coortes maiores anotadas por especialistas e atualmente dependa de um genoma de referência específico, o arcabouço aponta para exames de exoma que deixam passar menos variantes importantes. Na prática, isso pode significar que mais pacientes recebam respostas genéticas acionáveis, oportunas, a partir do sequenciamento que já estão realizando.
Citação: Ouhmouk, M., Abik, M. A convolutional attention model classifies copy number variants from whole exome sequencing. Sci Rep 16, 14310 (2026). https://doi.org/10.1038/s41598-026-44691-2
Palavras-chave: variantes no número de cópias, sequenciamento do exoma inteiro, aprendizado profundo em genômica, rede neural convolucional, genética clínica