Clear Sky Science · nl
Een convolutioneel aandachtmodel classificeert copy number-varianten uit whole exome-sequencing
Verborgen aanwijzingen in ons DNA ontdekken
Artsen gebruiken DNA-sequencing steeds vaker om genetische veranderingen te zoeken die ziekte kunnen verklaren, maar enkele van de belangrijkste aanwijzingen zijn geen losse “typo”-mutaties — het zijn stukken DNA die ontbreken of gekopieerd zijn. Deze veranderingen, copy number-varianten genoemd, zijn moeilijk te zien in de gegevens die de meeste ziekenhuizen al genereren. Deze studie introduceert een nieuw computermodel dat ruisige DNA-coveragepatronen leest en ontbrekende of extra stukken nauwkeuriger en consistenter detecteert over verschillende sequencingplatforms heen, wat mogelijk een veelgebruikt hulpmiddel in de medische genetica kan verscherpen.
Waarom extra of ontbrekend DNA ertoe doet
Copy number-varianten zijn DNA-fragmenten die in minder of meer exemplaren voorkomen dan gebruikelijk. Een segment kan volledig verwijderd zijn of meerdere keren gekopieerd worden. Zulke veranderingen kunnen alledaagse kenmerken beïnvloeden, het risico op aandoeningen zoals kanker of neuro‑ontwikkelingsstoornissen wijzigen en de evolutie van menselijke populaties beïnvloeden. Klinisch is het vinden van deze varianten cruciaal bij zowel zeldzame ziekte-diagnostiek als tumorprofilering. Veel patiënten ondergaan al whole-exome sequencing, gericht op de eiwitcoderende delen van het genoom. Het benutten van deze bestaande exoomtests om ook copy number-varianten te detecteren kan genetisch onderzoek informatiever maken zonder dat duurdere aanvullende assays nodig zijn.
Waarom huidige tools moeite hebben
Het detecteren van copy number-varianten uit exoomdata is technisch lastig. Het exoomcaptureren bemonstert het genoom ongelijkmatig, wat leidt tot rafelige, ruisige read depth — het aantal sequencingreads dat elk gebied dekt. Traditionele software gladstrijkt deze ruis met statistische trucs en handgemaakte regels en past vervolgens drempels toe om te beslissen of een regio normaal, verwijderd of gedupliceerd is. Hoewel nuttig, falen deze methoden vaak bij lage coverage, bij sequencing op verschillende machines of chemieën, of wanneer subtiele patronen over aangrenzende regio’s en chromosomen belangrijk zijn. Daardoor kan de sensitiviteit afnemen, vooral voor kleinere of luidruchtigere events, en presteert de methode mogelijk minder goed tussen laboratoria of platforms.

Een nieuwe manier om ruisige signalen te lezen
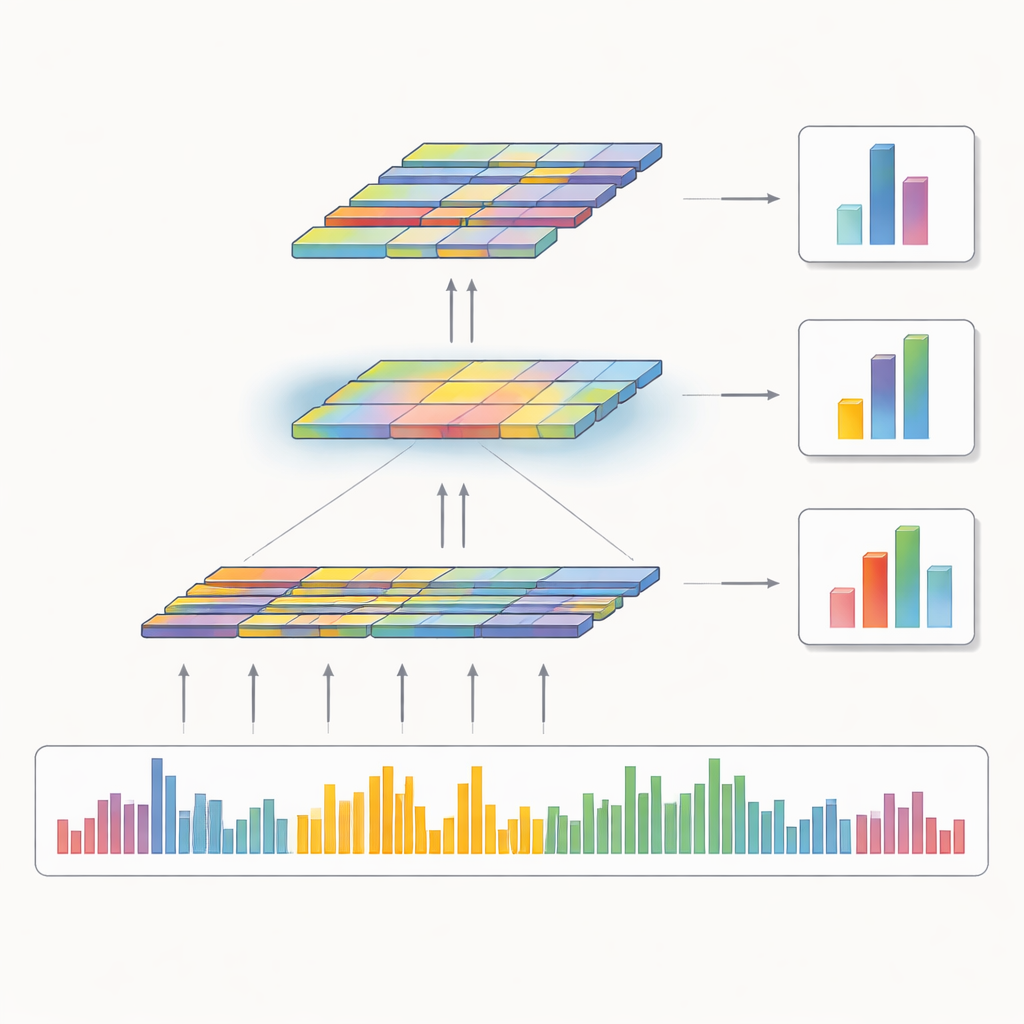
De auteurs ontwierpen een deep learning-model, CNN‑Att genoemd, dat direct leert van de ruwe coveragepatronen in plaats van voornamelijk op vaste regels te vertrouwen. Voor elk eiwitcoderend segment (een exon) neemt het model een gestandaardiseerde momentopname van de read depth over het exon en de omliggende regio op, samen met de genomische start- en eindposities. Het krijgt ook een gecodeerde aanduiding welke chromosoom het exon afkomstig is. Convolutionele lagen — oorspronkelijk populair voor beeldanalyse — scannen langs dit eendimensionale signaal om lokale vormen in het coveragepatroon vast te leggen, zoals dalen die deleties kunnen aangeven of subtiele bulten die op duplicaties wijzen. Een attention-mechanisme markeert vervolgens de meest informatieve kenmerken, met name vage signalen die bij kleine of ruisige events horen, voordat het model een driedelige beslissing neemt: normaal, deletie of duplicatie.
Hoe goed het model presteert
Om CNN‑Att te evalueren trainden de onderzoekers het op een grote benchmark opgebouwd uit het 1000 Genomes Project, waarbij exoomdata gekoppeld waren aan labels afgeleid uit uitgebreidere whole-genome sequencing. Op een aparte set van 50 exoommonsters die voor testen waren achtergehouden, classificeerde het model ongeveer 83 procent van de exonvensters correct en toonde het een sterke mogelijkheid om de drie klassen te onderscheiden, met hoge scores op zowel receiver-operating als precision–recall-curves. Deleties waren iets makkelijker te detecteren dan duplicaties, wat verklaard wordt doordat deleties meestal een sterker spoor in de coverage achterlaten. Het model presteerde beter dan een eenvoudiger baseline die alleen de genomische coördinaten kende, wat aangeeft dat het daadwerkelijk leert van de dieptepatronen in plaats van “hotspot”-locaties te memoriseren waar varianten veel voorkomen.
Betrouwbaar over verschillende sequencers heen
Aangezien klinische en onderzoekcentra verschillende sequencingmachines gebruiken, moet een praktisch hulpmiddel goed functioneren over platforms heen. De auteurs testten CNN‑Att daarom op exoomdata van hetzelfde referentie-DNA-monster dat werd gesekvenst op vier belangrijke technologieën: HiSeq 4000, NovaSeq 6000, MGISEQ 2000 en BGISEQ 500. Over deze uiteenlopende instrumenten varieerde de algemene F1-score — een balans tussen precisie en recall — van 0,89 tot 0,96, consistent hoger dan meerdere veelgebruikte traditionele tools. In een vervolgexperiment fine‑tunede het team alleen de uiteindelijke beslissingslagen van het model met een kleine set van zeven monsters die zorgvuldig door experts waren geannoteerd. Zelfs met deze beperkte, gekeurde data verhoogde fine‑tuning merkbaar de recall voor echte deleties en duplicaties op achtergehouden monsters, ten koste van meer false positives, een afweging die vaak acceptabel is wanneer twijfelachtige calls met vervolgtests gecontroleerd kunnen worden.
Wat dit betekent voor patiënten en onderzoek
Dit werk laat zien dat een gerichte deep learning-aanpak de ruisige, ongelijkmatige coverage van routinematige exoomsequencing kan omzetten in een betrouwbaardere detector van ontbrekende en extra DNA-segmenten. CNN‑Att behaalt hoge sensitiviteit terwijl fouten op beheersbare niveaus blijven en blijft robuust over verschillende sequencingmachines, wat het nuttig maakt voor multi‑site studies en grote populatieprojecten. Hoewel het nog validatie nodig heeft op grotere door experts geannoteerde cohorten en momenteel afhankelijk is van een specifiek referentiegenoom, wijst het raamwerk in de richting van exoomtests die minder belangrijke varianten missen. In de praktijk kan dat betekenen dat meer patiënten tijdig en praktisch bruikbare genetische antwoorden krijgen uit de sequencing die ze al ondergaan.
Bronvermelding: Ouhmouk, M., Abik, M. A convolutional attention model classifies copy number variants from whole exome sequencing. Sci Rep 16, 14310 (2026). https://doi.org/10.1038/s41598-026-44691-2
Trefwoorden: copy number-varianten, whole exome-sequencing, deep learning-genomics, convolutioneel neuraal netwerk, klinische genetica