Clear Sky Science · pt
Percepções experimentais e computacionais sobre microesferas de CMC modificadas com CuFeMoO₄ para remoção eficaz de azul de metileno de meios aquosos
Limpeza de Águas Fortemente Coloridas
Muitas indústrias geram águas residuais com cores intensas, e esses tons vivos de azul e vermelho podem causar danos a rios e à saúde humana. Este estudo explora um novo material de baixo custo que pode remover rapidamente um corante azul comum da água enquanto também ajuda a liberar hidrogênio limpo. Os pesquisadores combinam experimentos de laboratório com simulações computacionais para compreender exatamente como o material funciona, abrindo caminho para um tratamento industrial de águas residuais mais inteligente e ambientalmente correto.
Uma Nova Microesfera para Águas Contaminadas
O cerne do trabalho é um novo tipo de microesfera microscópica formada pela união de dois componentes: um óxido metálico misto contendo cobre, ferro e molibdênio (CuFeMoO₄) e um espessante de origem vegetal chamado carboximetilcelulose (CMC). Usando um sal simples como agente de reticulação, a equipe forma microesferas quase esféricas onde nanopartículas metálicas rígidas e em forma de haste ficam envolvidas por uma concha polimérica macia e biodegradável. Testes com várias técnicas de imagem e análise superficial mostram que essas esferas têm área superficial moderada, poros em escala nanométrica e uma estrutura interna relativamente uniforme, características que as ajudam a interagir de forma eficiente com poluentes na água. 
Como as Esferas Eliminam o Corante Azul
Para testar as esferas, os pesquisadores focaram no azul de metileno, um corante brilhante amplamente usado em têxteis, tintas, cosméticos e medicina. Em vez de simplesmente adsorver o corante à superfície, eles utilizaram um agente químico reativo, o borohidreto de sódio, que pode doar elétrons e átomos de hidrogênio. Por si só, esse agente pouco altera o corante, e as esferas isoladas também não removem a cor. Mas quando ambos estão presentes juntos com as novas microesferas, o tom azul desaparece quase completamente em cerca de 45 minutos. O corante é transformado quimicamente em uma forma incolor, em vez de apenas ser transferido da água para um sólido, o que torna a remoção mais permanente.
Ajustando as Condições para Melhor Desempenho
A equipe variou sistematicamente a dose de catalisador, a concentração do corante e do borohidreto, a acidez (pH), o teor de sal e a temperatura. Aumentar a quantidade de esferas acelerou a reação, pois mais superfícies ativas ficaram disponíveis. Tornar a solução de corante mais concentrada desacelerou o processo, já que a superfície limitada ficou mais ocupada e parcialmente bloqueada. Níveis maiores de borohidreto aumentaram a velocidade ao fornecer mais elétrons. A reação apresentou melhor desempenho em pH quase neutro, por volta de 6: em condições fortemente ácidas a superfície da esfera repeliu o corante carregado positivamente, enquanto em condições fortemente básicas repeliu o borohidreto, carregado negativamente. A adição de sal comum prejudicou o processo, porque os íons do sal competiam com o corante e o borohidreto pelos mesmos sítios na superfície da esfera. Temperaturas mais altas, de modo geral, aumentaram a velocidade, mas também mostraram que o processo requer certo aporte energético e não é espontâneo sob todas as condições.
Dentro do Caminho de Reação Invisível
Testes de laboratório com uma molécula captadora de radicais mostraram que a reação não depende de radicais agressivos de curta duração, mas sim de um fluxo mais ordenado de elétrons através da superfície da esfera. Os metais na microesfera atuam como pequenas estações de retransmissão: íons de cobre, ferro e molibdênio são reduzidos pelo borohidreto, depois transferem elétrons para o corante e, por fim, retornam ao estado original, prontos para repetir o ciclo. Para entender por que o corante reage dessa forma, os autores utilizaram cálculos modernos de química quântica. Essas simulações mapeiam como os elétrons estão distribuídos na molécula do corante e identificam sua parte mais vulnerável. Eles descobriram que o átomo de enxofre no centro do anel do corante, portando carga positiva, é o principal alvo do ataque eletrônico, em concordância com o caminho observado em que a forma colorida é reduzida para uma forma incolor. 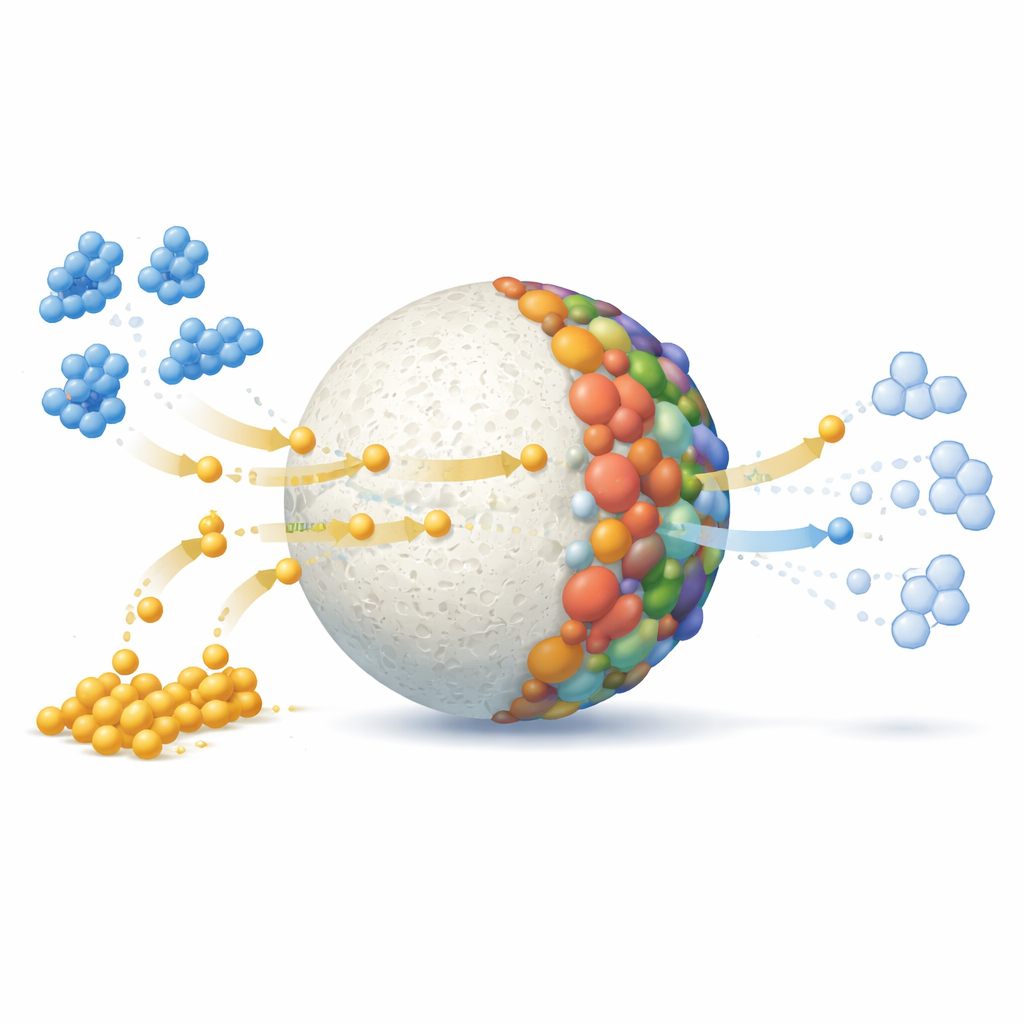
Resistência ao Reuso
Para qualquer planta de tratamento real, um catalisador só é útil se puder ser reutilizado muitas vezes. Os pesquisadores realizaram múltiplos ciclos de remoção do corante, filtrando, lavando e secando as esferas antes de cada nova utilização. As esferas mantiveram quase todo o seu desempenho durante cinco ciclos, caindo para cerca de metade da eficiência apenas no oitavo. Microscopia após o uso mostrou algum tornamento e aglomeração das nanopartículas internas, mas os elementos-chave e a estrutura geral permaneceram intactos, explicando a boa durabilidade. Quando compararam seu material com muitos outros catalisadores relatados para remoção de azul de metileno, as novas esferas se destacaram tanto pela alta eficiência quanto pela reação relativamente rápida.
O Que Isso Significa para Águas Mais Limpas
Em termos práticos, este trabalho demonstra que uma mistura simples e econômica de metais comuns e um polímero biodegradável pode remover de maneira muito eficaz e repetida um corante persistente da água quando combinada com um agente redutor suave. Experimentos e simulações se reforçam mutuamente, revelando como os elétrons se movem pelo sistema e qual parte do corante é atacada. Como as esferas são fáceis de recuperar e reutilizar, e seus componentes são abundantes e de baixo custo, elas oferecem uma rota promissora para o tratamento escalável de efluentes corados, ajudando indústrias a reduzir sua pegada ecológica sem depender de metais raros ou preciosos.
Citação: Salem, M.A., Awad, M.K., Sleet, R.K. et al. Experimental and computational insights into the CuFeMoO₄ modified CMC microbeads for effective removal of methylene blue from aqueous media. Sci Rep 16, 12040 (2026). https://doi.org/10.1038/s41598-026-43208-1
Palavras-chave: tratamento de águas residuais, azul de metileno, nanocatalisador, carboximetilcelulose, teoria do funcional da densidade