Clear Sky Science · pl
Eksperymentalne i obliczeniowe poznanie modyfikowanych mikrocząstek CMC z CuFeMoO₄ do skutecznego usuwania błękitu metylenowego z mediów wodnych
Usuwanie intensywnie zabarwionej wody
Wiele gałęzi przemysłu pozostawia za sobą jaskrawo zabarwione ścieki, a te żywe odcienie niebieskiego i czerwonego mogą szkodzić rzekom i zdrowiu ludzi. W badaniu tym analizuje się nowy, niedrogi materiał, który może szybko usuwać z wody powszechny niebieski barwnik, jednocześnie wspomagając uwalnianie czystego wodoru. Naukowcy łączą eksperymenty laboratoryjne z symulacjami komputerowymi, aby dokładnie zrozumieć mechanizm działania materiału, co otwiera drogę do bardziej inteligentnego i ekologicznego oczyszczania ścieków przemysłowych.
Nowa mikrokulka do oczyszczania wody
Rdzeniem pracy jest nowy rodzaj mikroskopijnych kuleczek powstałych w wyniku połączenia dwóch składników: tlenku metali mieszanego zawierającego miedź, żelazo i molibden (CuFeMoO₄) oraz pochodnej roślinnej o właściwościach zagęszczających, karboksymetylocelulozy (CMC). Przy użyciu prostej soli jako sieciującego czynnika zespół formuje prawie sferyczne mikrokulki, w których twarde, prętowe nanocząstki metalu są owinięte miękką, biodegradowalną powłoką polimerową. Badania z wykorzystaniem różnych technik obrazowania i analizy powierzchni wykazały, że kuleczki mają umiarkowaną powierzchnię właściwą, pory w skali nanometrycznej i dość jednolitą strukturę wewnętrzną — cechy sprzyjające efektywnej interakcji z zanieczyszczeniami w wodzie. 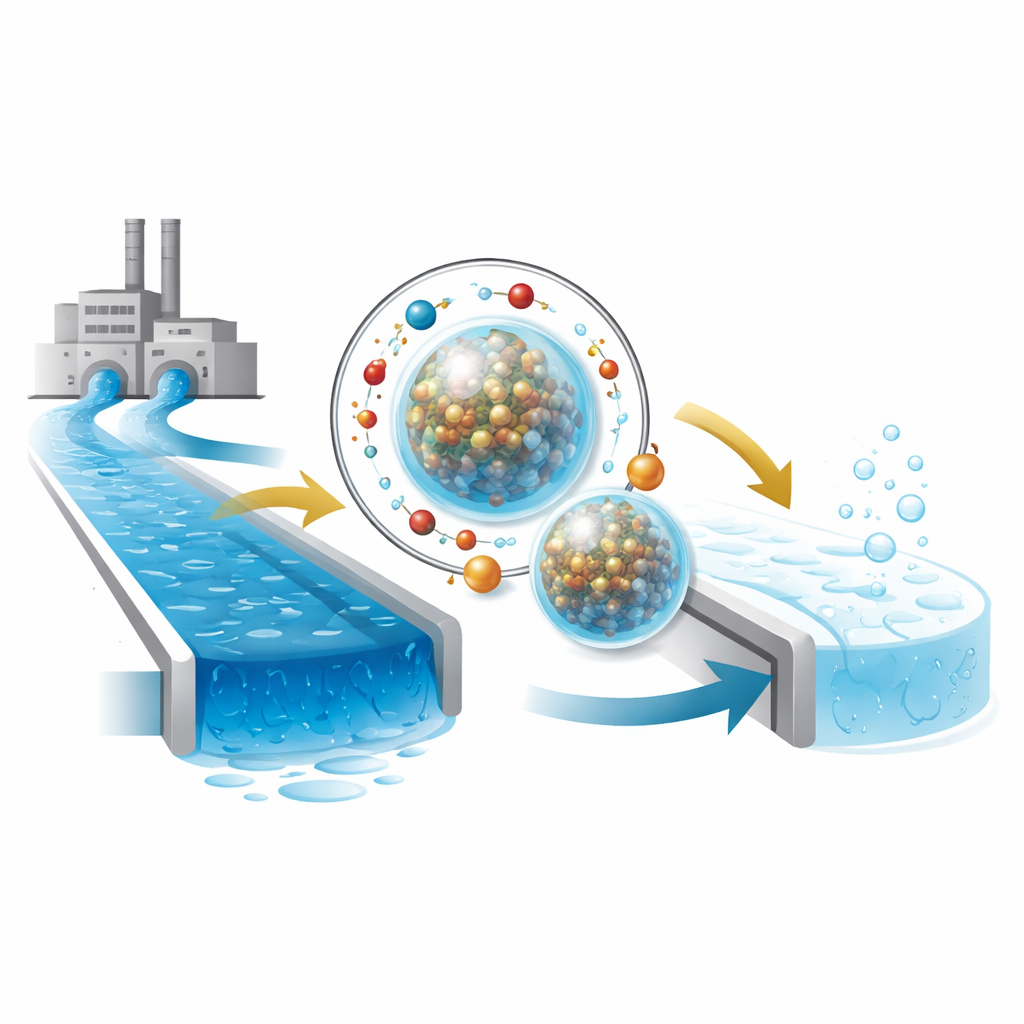
Jak kulki usuwają niebieski barwnik
Do testów badacze użyli błękitu metylenowego, intensywnego barwnika szeroko stosowanego w tekstyliach, atramentach, kosmetykach i medycynie. Zamiast polegać jedynie na adsorpcji barwnika na powierzchni, zastosowali chemicznego pomocnika — borowodorek sodu, który może dostarczać elektrony i atomy wodoru. Samodzielnie ten reduktor niemal nie wpływa na barwnik, a same kulki również nie usuwają koloru. Jednak gdy oba składniki są obecne razem z nowymi mikrokulkami, niebieski kolor niemal całkowicie zanika w ciągu około 45 minut. Barwnik ulega chemicznej przemianie do bezbarwnej formy, zamiast być tylko przeniesionym z wody na ciało stałe, co czyni oczyszczanie trwalszym.
Dostrajanie warunków dla najlepszej wydajności
Zespół systematycznie zmieniał dawkę katalizatora, stężenie barwnika i borowodorku, kwasowość (pH), zawartość soli i temperaturę. Zwiększenie ilości kulek przyspieszało reakcję, ponieważ dostępnych było więcej aktywnych powierzchni. Wyższe stężenie roztworu barwnika spowalniało proces, gdyż ograniczona powierzchnia stawała się zatłoczona i częściowo zatkana. Podwyższenie stężenia borowodorku zwiększało szybkość, dostarczając więcej elektronów. Reakcja działała najlepiej przy prawie neutralnym pH około 6: w silnie kwaśnym środowisku powierzchnia kulek odrzucała dodatnio naładowany barwnik, natomiast w silnie zasadowym odpychała ujemnie naładowany borowodorek. Dodatek zwykłej soli hamował proces, ponieważ jony soli konkurowały z barwnikiem i borowodorkiem o te same miejsca na powierzchni kulek. Wyższe temperatury generalnie zwiększały szybkość reakcji, ale także wykazały, że proces wymaga pewnego wkładu energetycznego i nie jest spontaniczny we wszystkich warunkach.
Wnętrze niewidocznej ścieżki reakcji
Testy laboratoryjne z użyciem cząsteczki wychwytującej rodniki pokazały, że reakcja nie opiera się na krótkotrwałych, agresywnych rodnikach, lecz na bardziej uporządkowanym przepływie elektronów po powierzchni kulek. Metale w kulce działają jak małe stacje przekaźnikowe: jony miedzi, żelaza i molibdenu są redukowane przez borowodorek, następnie przekazują elektrony do barwnika, a w końcu wracają do stanu wyjściowego, gotowe do powtórzenia cyklu. Aby zrozumieć, dlaczego barwnik reaguje w ten sposób, autorzy wykorzystali współczesne obliczenia chemii kwantowej. Symulacje mapują rozkład elektronów w cząsteczce barwnika i identyfikują jej najbardziej podatne miejsce. Stwierdzili, że atom siarki w centrum pierścienia barwnika, niosący dodatni ładunek, jest głównym celem ataku elektronowego, co odpowiada obserwowanej ścieżce, w której zabarwiona forma zostaje zredukowana do bezbarwnej. 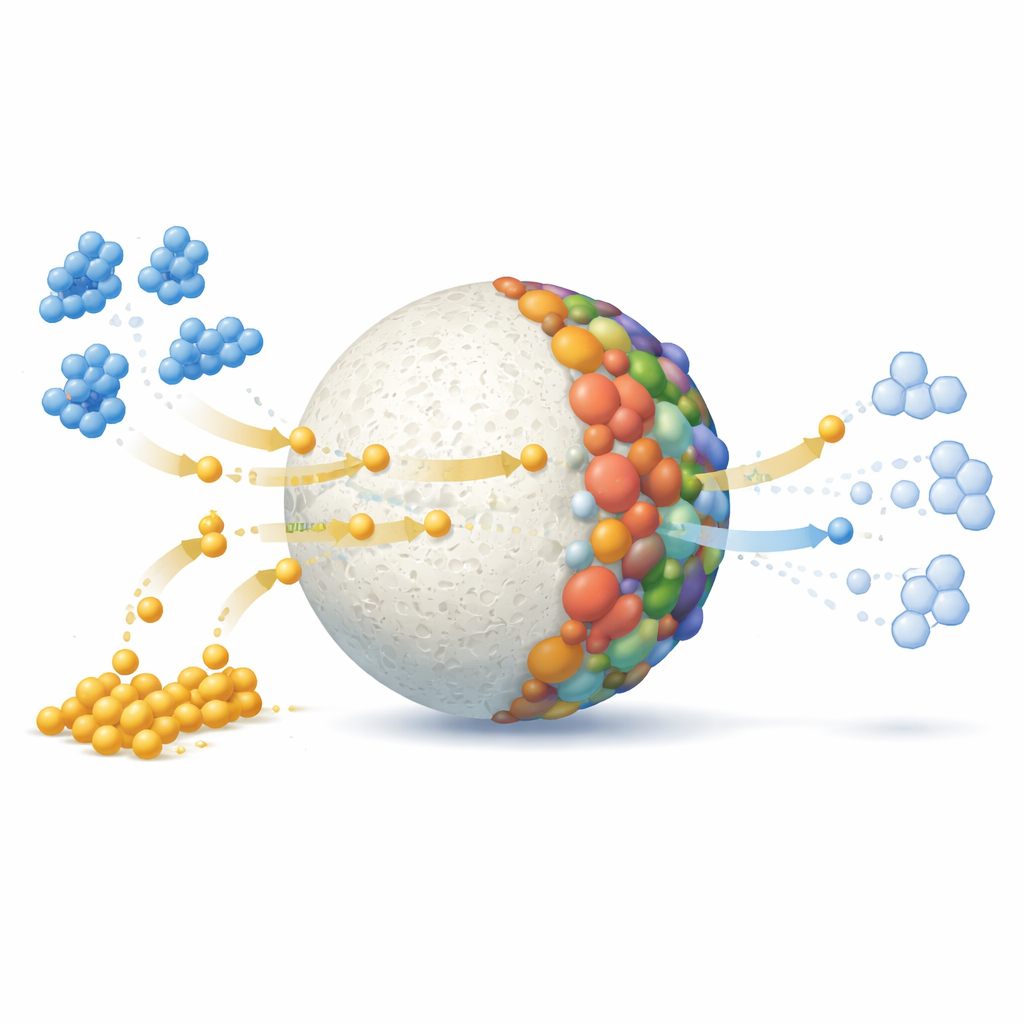
Trwałość przy ponownym użyciu
Dla zakładu oczyszczania praktyczne zastosowanie katalizatora zależy od jego możliwości wielokrotnego użycia. Badacze przeprowadzili kilka cykli usuwania barwnika, za każdym razem filtrując, myjąc i susząc kulki przed ponownym użyciem. Kulki zachowały niemal pełną skuteczność przez pięć cykli, spadając dopiero do około połowy wydajności po ósmym cyklu. Mikroskopia po użyciu wykazała pewne szorstkienie i zlepianie nanocząstek wewnątrz, lecz kluczowe pierwiastki i ogólna struktura pozostały nienaruszone, co tłumaczy dobrą trwałość. Porównanie z wieloma innymi opisanymi katalizatorami do usuwania błękitu metylenowego pokazało, że nowe kulki wyróżniają się zarówno bardzo wysoką efektywnością, jak i stosunkowo szybkim przebiegiem reakcji.
Znaczenie dla czystszej wody
Krótko mówiąc, praca ta pokazuje, że prosta, niedroga mieszanka powszechnych metali i biodegradowalnego polimeru może bardzo skutecznie i wielokrotnie usuwać oporny barwnik z wody, gdy zastosuje się łagodny czynnik redukujący. Eksperymenty i symulacje wzajemnie się uzupełniają, ujawniając, jak elektrony przemieszczają się przez system i która część barwnika jest atakowana. Ponieważ kulki są łatwe do odzyskania i ponownego użycia, a ich składniki są dostępne i tanie, oferują obiecującą drogę do skalowalnego oczyszczania ścieków barwionych, pomagając przemysłowi zmniejszyć ślad ekologiczny bez odwoływania się do rzadkich czy drogocennych metali.
Cytowanie: Salem, M.A., Awad, M.K., Sleet, R.K. et al. Experimental and computational insights into the CuFeMoO₄ modified CMC microbeads for effective removal of methylene blue from aqueous media. Sci Rep 16, 12040 (2026). https://doi.org/10.1038/s41598-026-43208-1
Słowa kluczowe: oczyszczanie ścieków, błękit metylenowy, nanokatalizator, karboksymetyloceluloza, teoria funkcjonału gęstości