Clear Sky Science · pt
Esferas magnéticas funcionalizadas com aptâmeros combinadas com reação em cadeia de hibridização para detecção de Bacillus cereus
Por que isso importa para o consumo diário
Intoxicações alimentares por arroz para viagem, leite ou refeições prontas costumam ser atribuídas a um micro-organismo resistente chamado Bacillus cereus. Testes laboratoriais tradicionais para detectar esse germe podem levar dias, tempo excessivo para cozinhas movimentadas, empresas de alimentos ou inspetores de segurança. Este estudo apresenta um método laboratorial rápido e altamente sensível que, no futuro, pode ajudar a tornar alimentos como leite e arroz mais seguros, detectando níveis muito baixos de B. cereus sem equipamentos caros ou procedimentos genéticos complexos.
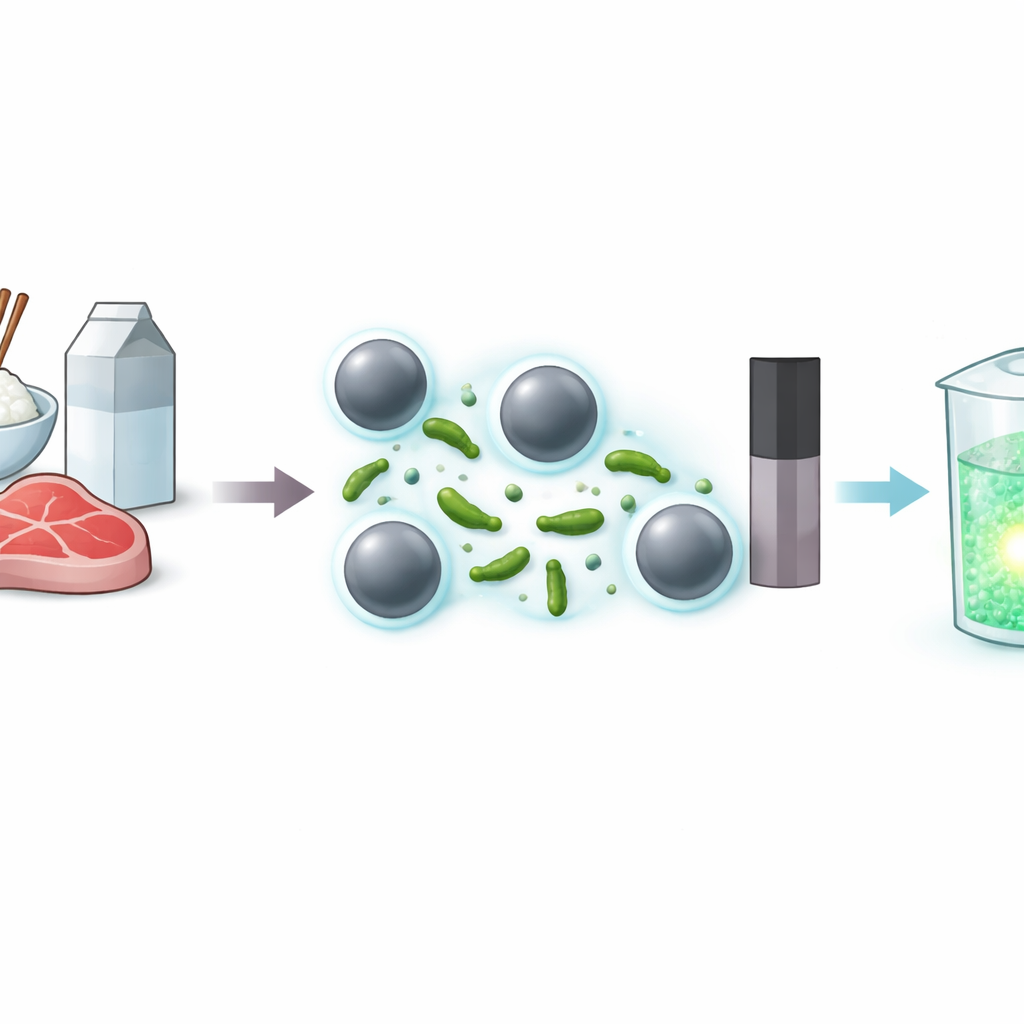
A ameaça oculta em alimentos comuns
Bacillus cereus está presente em alimentos cotidianos como arroz, leite e carne. Ele sobrevive a condições adversas, forma esporos resistentes e produz toxinas que provocam vômito e diarreia. A detecção padrão baseia-se no cultivo das bactérias em placas, que é precisa mas lenta e trabalhosa, tornando-se impraticável para verificações rápidas no local. Testes moleculares como PCR são mais rápidos, mas exigem extração cuidadosa de DNA, instrumentos especializados e controle rigoroso de contaminação. Outros testes baseados em anticorpos podem ser mais ágeis, porém frequentemente carecem da sensibilidade necessária ou continuam custosos demais para triagens rotineiras.
Usando “travas” inteligentes e minúscimos ímãs
Os autores aproveitam uma classe mais nova de “travas” biológicas chamadas aptâmeros — curtas fitas de DNA que se dobram em estruturas capazes de reconhecer um alvo específico, neste caso células de B. cereus. Esses aptâmeros são ligados a esferas magnéticas, criando partículas que podem capturar seletivamente as bactérias em uma amostra complexa. Quando uma mistura contendo B. cereus é adicionada, as bactérias se ligam às esferas revestidas com aptâmeros. Após um ímã puxar as esferas (e qualquer bactéria capturada) para a lateral, o restante da amostra pode ser descartado, enriquecendo efetivamente o alvo e removendo grande parte do material interferente presente em alimentos reais.
Transformando bactérias capturadas em um sinal luminoso
A sacada é como a presença das bactérias é convertida em um forte brilho fluorescente. Uma curta fita de DNA marcada com um corante fluorescente é desenhada para competir com B. cereus pelo mesmo aptâmero na esfera magnética. Se não houver bactérias, essa fita fluorescente se liga majoritariamente às esferas e é removida com elas, deixando pouco sinal. Se bactérias estiverem presentes, elas vencem a competição e a fita é liberada na solução. Essa fita liberada então aciona uma reação em cadeia de hibridização, na qual duas peças de DNA em forma de alfinete abrem-se repetidamente e se ligam formando longas cadeias duplas que carregam muitas moléculas de corante. Isso funciona como um amplificador embutido, transformando um evento molecular minúsculo em um sinal brilhante e mensurável.
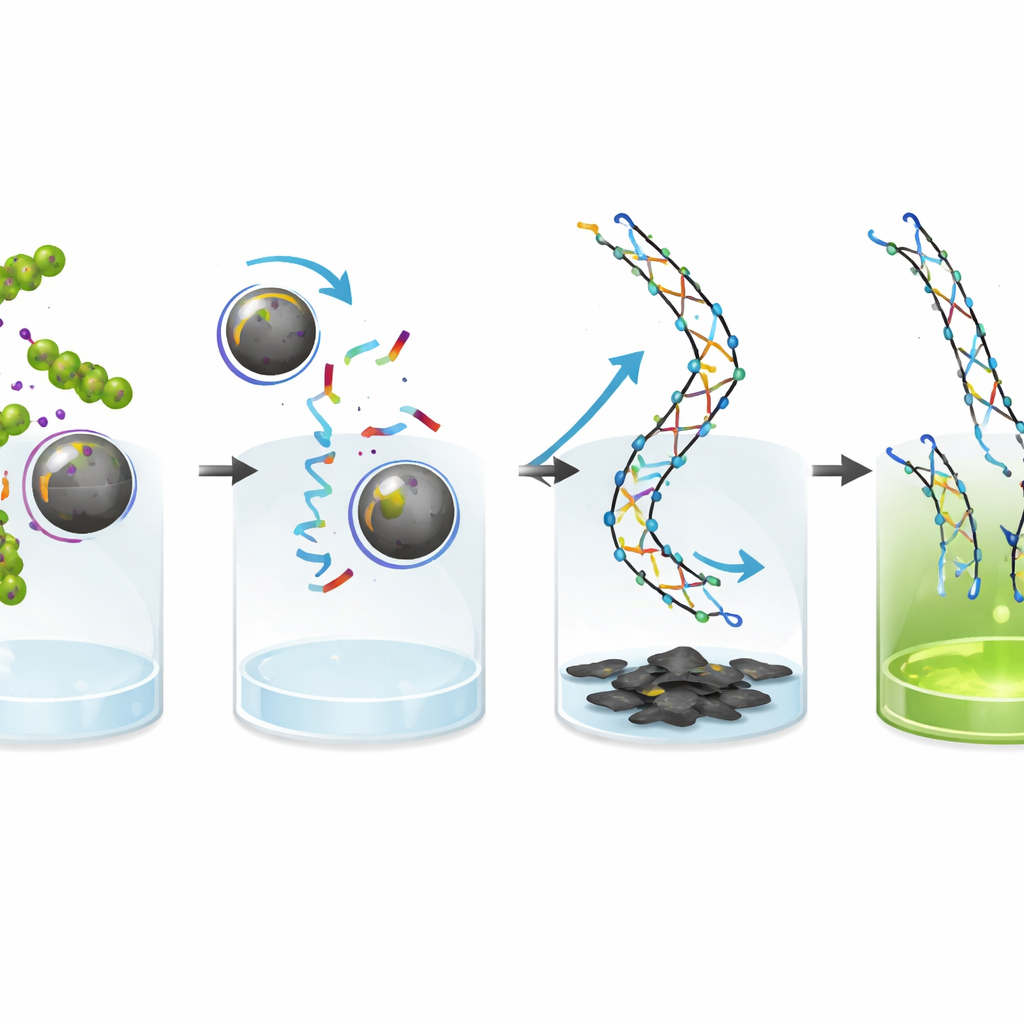
Deixando o brilho mais claro com um “apagador” de carbono
Para aprimorar ainda mais a leitura, a equipe usa óxido de grafeno, um material de carbono em folhas que adere fortemente a fitas soltas de DNA de fita simples e apaga eficientemente sua fluorescência. Fitas curtas não reagidas e fluorescentes são adsorvidas na superfície do óxido de grafeno e sua luz é efetivamente suprimida. Em contraste, os longos produtos rígidos de dupla fita da reação em cadeia não se ligam bem ao óxido de grafeno, por isso seu brilho permanece intenso. Essa combinação melhora muito o contraste entre “bactérias presentes” e “bactérias ausentes”, ajudando o sistema a detectar concentrações bacterianas muito baixas com confiança.
Desempenho do método em laboratório
Após otimizar condições como a carga de aptâmero nas esferas, tempos de reação e a quantidade de óxido de grafeno, os autores mostram que seu sistema reconhece especificamente B. cereus entre um painel de outras bactérias alimentares comuns. O sinal fluorescente de cepas verdadeiras de B. cereus é muito maior do que o de não‑alvos ou amostras em branco. Em suspensões bacterianas puras, o método detecta até cerca de 5,4 × 101 unidades formadoras de colônia por mililitro — comparável a muitos testes rápidos avançados disponíveis. Do manuseio inicial da amostra à leitura final, o processo completo leva cerca de duas horas, muito mais rápido que métodos baseados em cultivo e mais simples que muitas abordagens de amplificação de DNA.
Testando em leite comercial e olhando adiante
Para avaliar se o método funciona além de amostras limpas de laboratório, os pesquisadores adicionaram quantidades conhecidas de B. cereus a leite comercial e aplicaram o mesmo protocolo. Ainda observaram sinais fluorescentes fortes e dependentes da concentração em uma faixa semelhante à de cultura pura, demonstrando que a abordagem pode operar em uma matriz alimentar realista. Entretanto, a técnica detecta apenas bactérias vivas com superfícies celulares intactas e atualmente depende de um leitor de fluorescência de bancada, de modo que mais desenvolvimento é necessário para transformá‑la em um dispositivo portátil pronto para campo. Os autores sugerem que, trocando os aptâmeros, a mesma estrutura pode ser redirecionada para muitos outros patógenos alimentares.
O que isso significa para alimentos mais seguros
Em termos práticos, este trabalho demonstra um método laboratorial promissor que usa fechaduras de DNA inteligentes, esferas magnéticas e um sinal fluorescente auto‑montante para detectar quantidades muito pequenas de B. cereus de forma rápida e seletiva. Embora ainda não seja um teste de bolso, aponta para ferramentas futuras que poderiam rastrear alimentos como leite ou arroz em um par de horas em vez de dias, reduzindo a probabilidade de lotes perigosos chegarem aos consumidores. Com desenvolvimento e adaptação adicionais, estratégias semelhantes podem ajudar a criar uma nova geração de testes rápidos para controlar uma ampla gama de germes transmitidos por alimentos.
Citação: Song, X., Shi, C., Lv, Y. et al. Aptamer-functionalized magnetic beads combined with hybridization chain reaction for detection of Bacillus cereus. npj Sci Food 10, 124 (2026). https://doi.org/10.1038/s41538-026-00751-5
Palavras-chave: detecção de Bacillus cereus, segurança alimentar, biossensor de aptâmero, esferas magnéticas, reação em cadeia de hibridização