Clear Sky Science · fr
Billots magnétiques fonctionnalisés par aptamères combinés à une réaction en chaîne d’hybridation pour la détection de Bacillus cereus
Pourquoi cela importe pour nos repas quotidiens
Les intoxications alimentaires provoquées par du riz à emporter, du lait ou des plats prêts à consommer sont souvent attribuées à un micro-organisme résistant, Bacillus cereus. Les tests de laboratoire traditionnels pour repérer ce germe peuvent prendre plusieurs jours, ce qui est beaucoup trop lent pour des cuisines occupées, des entreprises alimentaires ou des inspecteurs de sécurité. Cette étude présente une méthode de laboratoire rapide et très sensible qui pourrait un jour contribuer à rendre des aliments comme le lait et le riz plus sûrs en détectant même de très faibles niveaux de B. cereus sans équipement coûteux ni procédures génétiques complexes.
La menace cachée dans des aliments courants
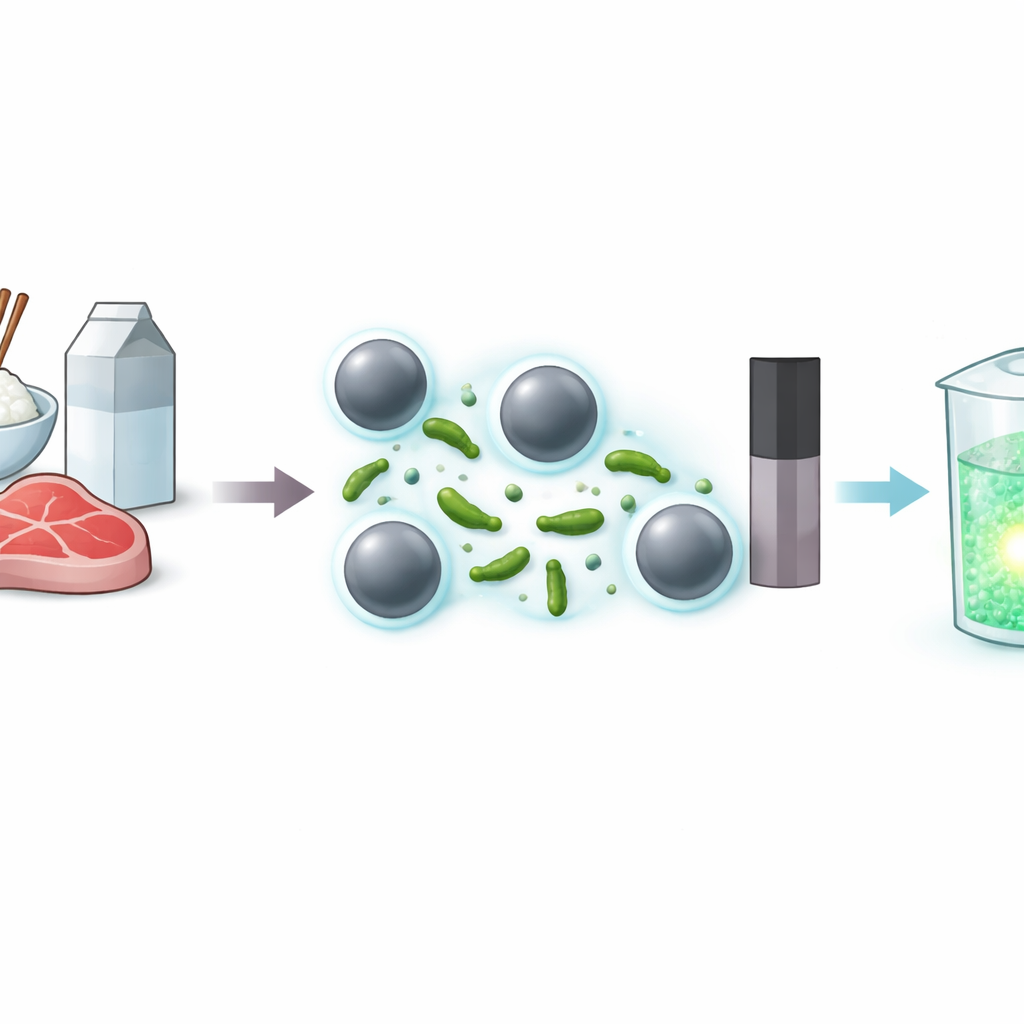
Bacillus cereus est répandu dans des aliments quotidiens tels que le riz, le lait et la viande. Il peut survivre à des conditions difficiles, former des spores résistantes et produire des toxines qui provoquent vomissements et diarrhée. La détection standard repose sur la culture des bactéries sur milieux, ce qui est précis mais lent et exigeant en main-d’œuvre, rendant la méthode peu pratique pour des contrôles rapides sur site. Les tests moléculaires comme la PCR sont plus rapides, mais ils nécessitent une extraction d’ADN soigneuse, des instruments spécialisés et un contrôle strict des contaminations. D’autres tests à base d’anticorps peuvent être plus rapides mais manquent souvent de sensibilité ou restent trop coûteux pour un dépistage de routine.
Utiliser des « serrures » intelligentes et de petits aimants
Les auteurs s’appuient sur une classe récente de « serrures » biologiques appelées aptamères — de courts brins d’ADN qui se replient en structures reconnaissant une cible spécifique, ici des cellules de B. cereus. Ces aptamères sont fixés sur des billes magnétiques, créant de minuscules particules capables d’extraire sélectivement les bactéries d’un échantillon complexe. Lorsqu’un mélange contenant B. cereus est ajouté, les bactéries se lient aux billes recouvertes d’aptamères. Après qu’un aimant a attiré les billes (et les bactéries capturées) sur un côté, le reste de l’échantillon peut être retiré, ce qui enrichit la cible et élimine une grande partie du fond perturbateur présent dans les aliments réels.
Transformer les bactéries capturées en un signal lumineux
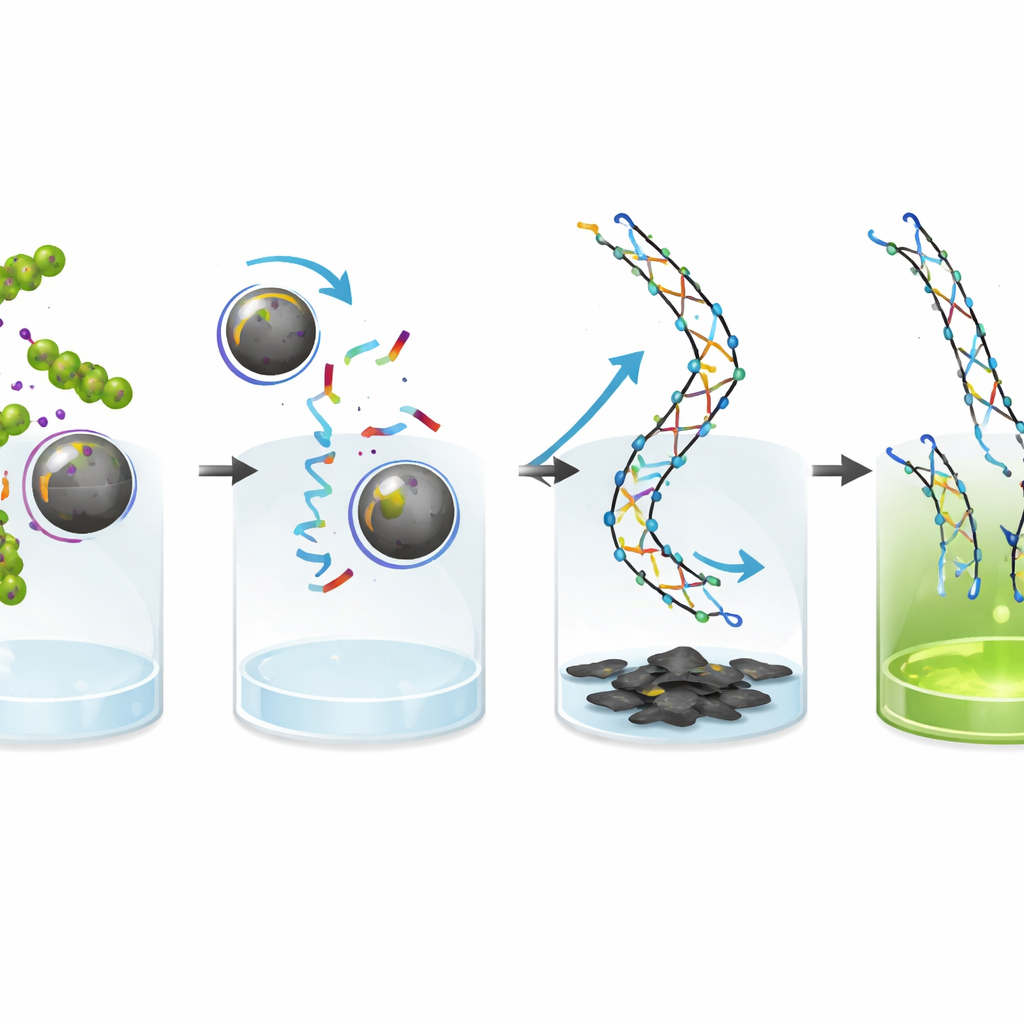
L’astuce ingénieuse consiste à convertir la présence des bactéries en une forte fluorescence. Un court brin d’ADN marqué par un colorant fluorescent est conçu pour rivaliser avec B. cereus pour le même aptamère sur la bille magnétique. En l’absence de bactéries, ce brin fluorescent reste principalement fixé aux billes et est enlevé avec elles, laissant peu de signal. Si des bactéries sont présentes, elles remportent la compétition et le brin est libéré dans la solution. Ce brin libéré déclenche alors une réaction en chaîne d’hybridation, dans laquelle deux séquences en épingle à cheveux s’ouvrent et s’enchaînent pour former de longues structures double brin portant de nombreuses molécules colorantes. Cela agit comme un amplificateur intégré, transformant un événement moléculaire minime en un signal lumineux mesurable et puissant.
Rendre la fluorescence plus nette avec une « gomme » carbone
Pour améliorer encore la lecture, l’équipe utilise du graphène oxyde, un matériau carboné en feuillets qui adhère fortement aux brins d’ADN simples libres et éteint efficacement leur fluorescence. Les courts brins fluorescents non réagis sont attirés à la surface du graphène oxyde et leur lumière est ainsi annulée. En revanche, les longs produits rigides double brin de la réaction en chaîne se lient mal au graphène oxyde, de sorte que leur fluorescence demeure vive. Cette combinaison augmente grandement le contraste entre « bactérie présente » et « bactérie absente », aidant le système à détecter des concentrations bactériennes très faibles avec confiance.
Performance de la méthode en laboratoire
Après avoir optimisé des conditions telles que la charge d’aptamère sur les billes, les temps de réaction et la quantité de graphène oxyde, les auteurs montrent que leur dispositif reconnaît spécifiquement B. cereus dans un panel d’autres bactéries d’origine alimentaire courantes. Le signal fluorescent des souches véritablement B. cereus est bien plus élevé que celui des non-cibles ou des échantillons témoins. Dans des suspensions bactériennes pures, la méthode peut détecter jusqu’à environ 5,4 × 10^1 unités formant colonie par millilitre — comparable à de nombreux tests rapides avancés sur le marché. De la préparation initiale de l’échantillon à la lecture finale, le procédé complet dure environ deux heures, bien plus rapide que les méthodes de culture et plus simple que de nombreuses approches d’amplification de l’ADN.
Essais dans du vrai lait et perspectives
Pour évaluer si la méthode fonctionne au-delà d’échantillons propres de laboratoire, les chercheurs ont épicé du lait commercial avec des quantités connues de B. cereus et appliqué le même protocole. Ils ont observé des signaux fluorescents forts dépendant de la concentration sur une plage similaire à celle obtenue en culture pure, montrant que l’approche peut fonctionner dans une matrice alimentaire réaliste. Cependant, la technique détecte uniquement des bactéries vivantes ayant une surface cellulaire intacte et repose actuellement sur un lecteur de fluorescence de paillasse, donc des développements supplémentaires sont nécessaires pour l’adapter en dispositifs portables et utilisables sur le terrain. Les auteurs suggèrent qu’en remplaçant les aptamères, le même cadre pourrait être redirigé vers de nombreux autres agents pathogènes d’origine alimentaire.
Ce que cela signifie pour une alimentation plus sûre
En termes simples, ce travail démontre une méthode de laboratoire prometteuse qui utilise des serrures d’ADN intelligentes, des billes magnétiques et un signal fluorescent auto-amplifié pour repérer rapidement et de manière sélective de très faibles quantités de B. cereus. Bien qu’il ne s’agisse pas encore d’un test de poche, cela ouvre la voie à des outils futurs capables de dépister des aliments comme le lait ou le riz en quelques heures plutôt qu’en plusieurs jours, réduisant ainsi le risque que des lots dangereux atteignent les consommateurs. Avec un développement et une adaptation supplémentaires, des stratégies similaires pourraient contribuer à une nouvelle génération de tests rapides pour mieux contrôler un large éventail d’agents pathogènes alimentaires.
Citation: Song, X., Shi, C., Lv, Y. et al. Aptamer-functionalized magnetic beads combined with hybridization chain reaction for detection of Bacillus cereus. npj Sci Food 10, 124 (2026). https://doi.org/10.1038/s41538-026-00751-5
Mots-clés: détection de Bacillus cereus, sécurité alimentaire, biosenseur à aptamère, magnetic beads, réaction en chaîne d’hybridation