Clear Sky Science · pt
Dispersão atômica mediada por radicais induzida por foto de nanopartículas de metais nobres
Transformando metais preciosos em catalisadores supereficientes
Metais nobres como paládio e platina estão no cerne de muitas tecnologias modernas, desde a limpeza de gases de escape de automóveis até a fabricação de medicamentos e plásticos. Mas esses metais são raros e caros, e grande parte do metal em catalisadores convencionais fica presa dentro de partículas minúsculas onde não pode atuar. Este estudo descreve um método suave, acionado por luz, que pode decompor essas partículas em átomos individuais, aumentando dramaticamente a eficiência de uso de cada átomo precioso e oferecendo uma maneira mais verde de melhorar e até reciclar catalisadores industriais.
Por que quebrar partículas metálicas importa
Catalisadores tradicionais costumam empregar nanopartículas de metais nobres dispersas sobre um suporte de óxido. Apenas os átomos na superfície de cada partícula participam ativamente das reações; átomos enterrados no interior ficam essencialmente desperdiçados. Há muito tempo os cientistas buscam "catalisadores de átomo único", em que cada átomo de metal está exposto e ancorado ao suporte, maximizando o desempenho por átomo. As formas existentes de criar esses materiais geralmente exigem altas temperaturas, atmosferas gasosas especiais ou tratamentos químicos complicados. Essas abordagens consomem muita energia, são caras e, às vezes, difíceis de escalar. Uma rota simples e de baixa temperatura que possa converter catalisadores em nanopartículas existentes em versões de átomo único seria portanto muito atraente para a indústria.
Usando a luz como um transformador suave
Os autores mostram que luz ultravioleta pode conduzir essa transformação em condições do dia a dia. Eles dispersam nanopartículas de paládio suportadas em dióxido de titânio (TiO2) em uma solução muito diluída de ácido clorídrico em acetonitrila e, em seguida, irradiam com UV à temperatura ambiente. Antes da iluminação, a microscopia eletrônica revela claramente aglomerados de partículas de paládio na superfície do TiO2. Após uma hora de exposição à luz, as partículas desaparecem visualmente, mas análises químicas mostram que o paládio ainda está presente e agora distribuído de forma uniforme pela superfície. Imagens avançadas capazes de "ver" átomos individuais confirmam que o metal foi convertido em átomos isolados de paládio ancorados ao óxido. Medidas espectroscópicas que acompanham como o monóxido de carbono se liga à superfície também mudam de assinaturas características de partículas para aquelas típicas de átomos únicos, corroborando essa mudança estrutural. 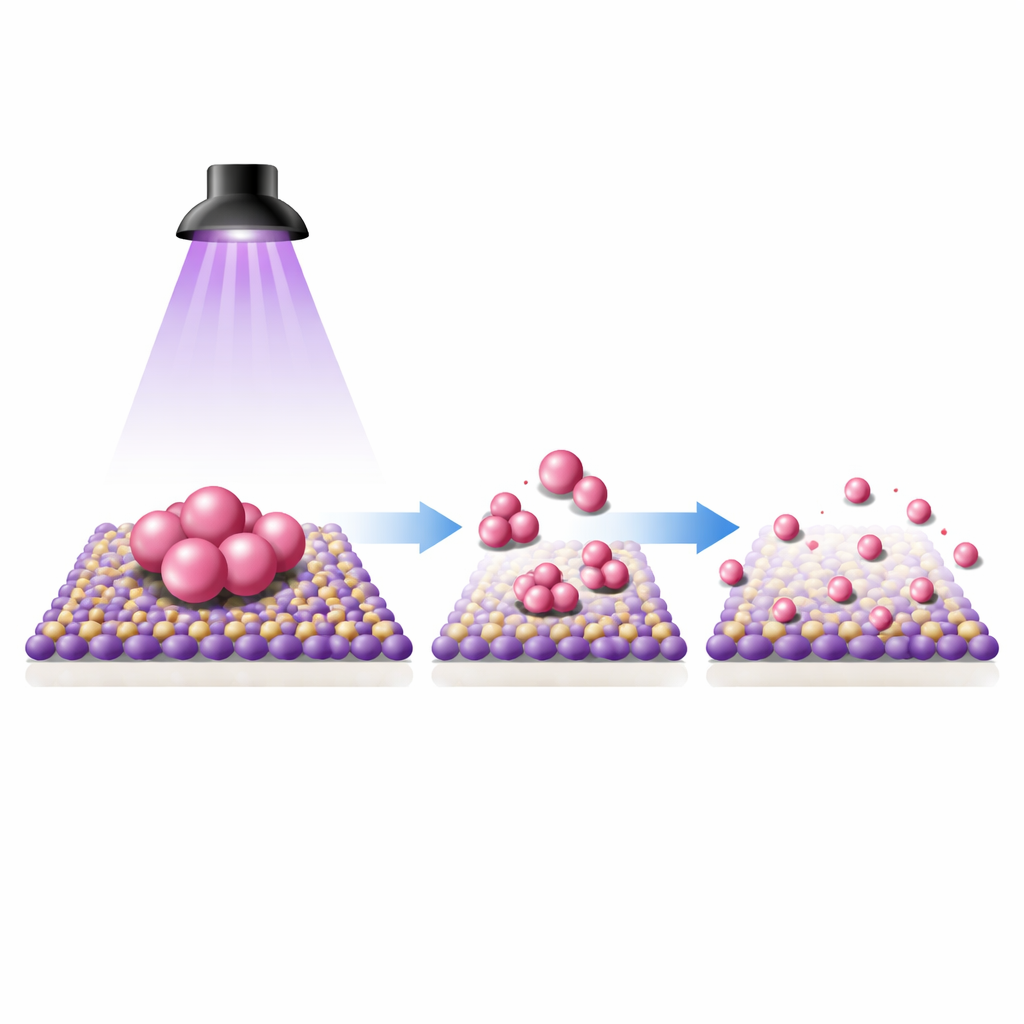
Como os radicais fazem o trabalho pesado
Para entender como essa remodelação acionada por luz ocorre, os pesquisadores investigam as espécies químicas formadas durante a iluminação e executam simulações baseadas em mecânica quântica. Quando a luz UV incide sobre o TiO2, ela cria elétrons energéticos e "lacunas" que migram para a superfície e reagem com a solução circundante. O oxigênio captura elétrons para formar radicais superóxido, enquanto a acetonitrila e os íons cloreto reagem com as lacunas para gerar radicais orgânicos e radicais de cloro. Experimentos que apagam seletivamente essas espécies de curta vida mostram que tanto os radicais de cloro quanto os de superóxido são essenciais para romper as ligações que mantêm os átomos de paládio unidos nas nanopartículas. Simulações revelam que os radicais de cloro primeiro se ligam ao metal, retirando densidade eletrônica e enfraquecendo as ligações paládio–paládio. O superóxido então ataca, e o cloreto da solução coordena os átomos liberados para formar um complexo intermediário móvel. Esse complexo é atraído eletrostaticamente para a superfície carregada positivamente do TiO2, onde perde cloreto e, com auxílio de radicais orgânicos e de sítios próximos de nitrogênio e oxigênio, se fixa no lugar como um átomo único de paládio ligado em um ambiente local estável.
Do mecanismo de laboratório a uma ferramenta versátil
Uma vez esclarecido o mecanismo, a equipe testou a abrangência da estratégia. Demonstraram que tratamentos semelhantes com luz podem converter não apenas paládio, mas também platina e ródio em átomos únicos sobre TiO2, e que o processo também funciona em outro suporte de óxido, o óxido de tungstênio (WO3). Partículas maiores de paládio preparadas por rotas convencionais de redução química também puderam ser decompostas sob exposição prolongada a UV. O mais importante para o uso prático é que catalisadores comerciais de paládio sobre carbono e até catalisadores industriais desperdiçados que haviam perdido atividade foram reativados com sucesso: após tratamento junto ao TiO2 sob luz UV, o paládio ficou disperso atomicamente e o desempenho dos catalisadores em uma reação padrão de hidrogenação aumentou quase 18 vezes para o material comercial e 26 vezes para o material de descarte. Esses catalisadores aprimorados também permaneceram altamente ativos ao longo de ciclos repetidos, e os autores demonstram que o processo pode ser realizado em um sistema de fluxo contínuo e até acionado pela luz solar.
Um caminho simples para catálise mais verde
Para não especialistas, a mensagem chave é que iluminar uma mistura cuidadosamente escolhida pode reorganizar metais preciosos de aglomerados para átomos individualmente ancorados, sem necessidade de altas temperaturas ou condições agressivas. Esse "desaglomeração" acionada por luz aumenta muito a eficácia de cada átomo metálico caro e pode dar nova vida a catalisadores industriais desgastados. Como o método funciona para vários metais importantes, diferentes suportes e materiais do mundo real, ele oferece uma rota promissora e ambientalmente amigável para processos catalíticos mais eficientes e sustentáveis nas indústrias química e de energia.
Citação: Chen, X., Zhao, Q., Zhang, J. et al. Photoinduced radical-mediated atomic dispersion of noble metal nanoparticles. Nat Commun 17, 3934 (2026). https://doi.org/10.1038/s41467-026-70742-3
Palavras-chave: catalisadores de átomo único, fotocatálise, nanopartículas de metais nobres, química verde, regeneração de catalisadores