Clear Sky Science · pl
Fotochemiczna, rodnikowo pośredniczona dyspergacja atomowa nanocząstek metali szlachetnych
Przekształcanie metali szlachetnych w superwydajne katalizatory
Metale szlachetne, takie jak pallad i platyna, są kluczowe dla wielu współczesnych technologii — od oczyszczania spalin samochodowych po produkcję leków i tworzyw sztucznych. Są jednak rzadkie i drogie, a w konwencjonalnych katalizatorach znaczna część metalu jest uwięziona wewnątrz drobnych cząstek i nie bierze udziału w reakcji. W tym badaniu opisano łagodną, napędzaną światłem metodę, która może rozbić te cząstki na pojedyncze atomy, radykalnie zwiększając efektywność wykorzystania każdego atomu metalu oraz oferując bardziej zielony sposób na modernizację i nawet recykling katalizatorów przemysłowych.
Dlaczego rozbijanie cząstek metalu ma znaczenie
Tradycyjne katalizatory często wykorzystują nanocząstki metali szlachetnych rozproszone na tlenkowym nośniku. Tylko atomy na powierzchni każdej cząstki aktywnie uczestniczą w reakcjach; atomy ukryte we wnętrzu są w zasadzie zmarnowane. Naukowcy od dawna dążą do stworzenia „katalizatorów jednoatomowych”, w których każdy atom metalu jest odsłonięty i zakotwiczony na nośniku, maksymalizując wydajność na atom. Istniejące metody wytwarzania takich materiałów zwykle wymagają wysokich temperatur, specjalnych atmosfer gazowych lub skomplikowanych zabiegów chemicznych. Podejścia te są energochłonne, kosztowne i czasami trudne do skalowania. Prosty, niskotemperaturowy sposób umożliwiający przekształcenie istniejących katalizatorów w wersje jednoatomowe byłby więc bardzo atrakcyjny dla przemysłu.
Użycie światła jako łagodnego przekształcacza
Autorzy pokazują, że ultrafioletowe światło może napędzać tę przemianę w warunkach codziennych. Rozpraszają nanocząstki palladu podparte na ditlenku tytanu (TiO2) w bardzo rozcieńczonym roztworze kwasu solnego w acetonitrylu, a następnie oświetlają mieszaninę UV w temperaturze pokojowej. Przed naświetlaniem mikroskopia elektronowa wyraźnie ukazuje skupione cząstki palladu na powierzchni TiO2. Po godzinie ekspozycji na światło cząstki wizualnie znikają, lecz analizy chemiczne wykazują, że pallad nadal jest obecny i teraz równomiernie rozproszony po powierzchni. Zaawansowane obrazowanie zdolne „zobaczyć” pojedyncze atomy potwierdza, że metal został przekształcony w izolowane atomy palladu zakotwiczone do tlenku. Pomiary spektroskopowe śledzące wiązanie tlenku węgla do powierzchni również przesuwają sygnatury z charakterystycznych dla cząstek na te typowe dla pojedynczych atomów, co wspiera tę zmianę strukturalną. 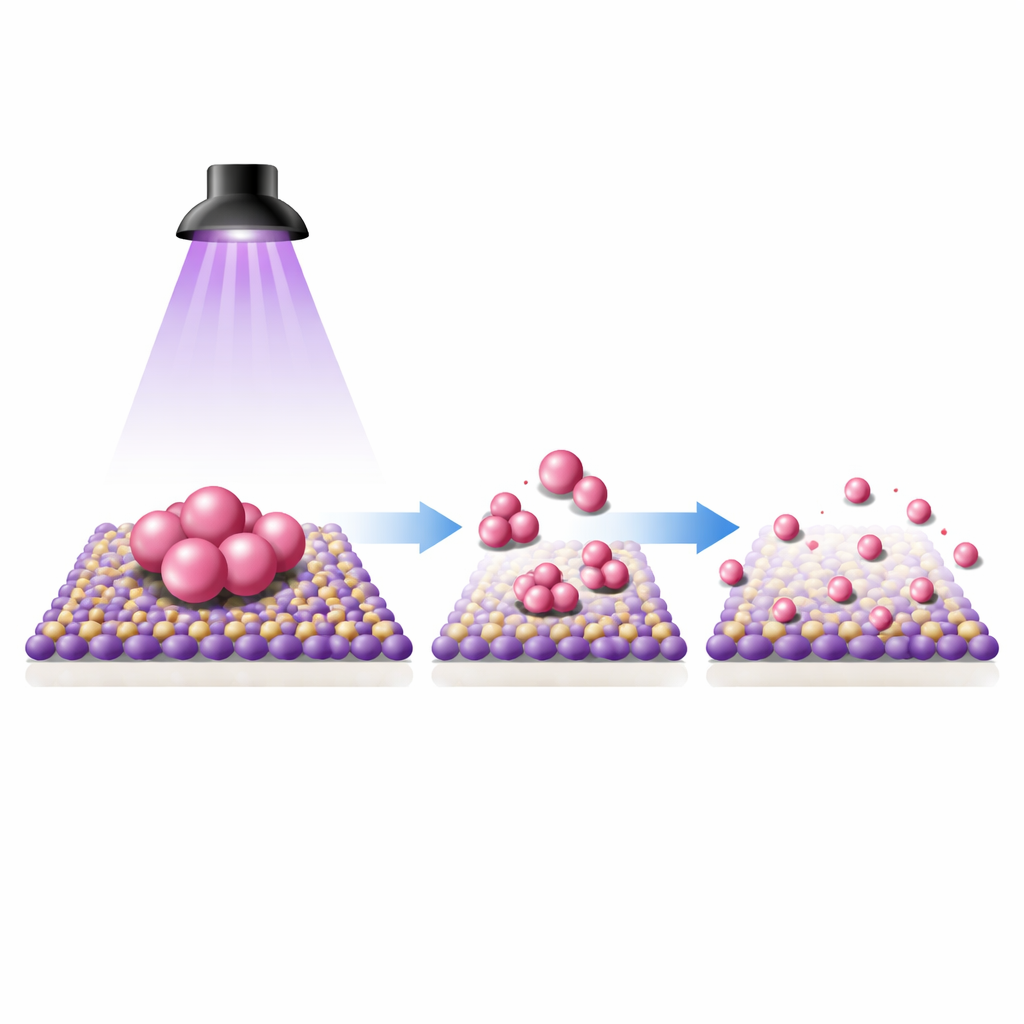
Jak rodniki wykonują ciężką pracę
Aby zrozumieć, jak zachodzi to światłozależne przeorganizowanie, badacze badają gatunki chemiczne powstające w trakcie naświetlania i przeprowadzają symulacje oparte na mechanice kwantowej. Gdy UV pada na TiO2, tworzy się para energetycznych elektronów i „dziur”, które przemieszczają się na powierzchnię i reagują z otaczającym roztworem. Tlen przechwytuje elektrony tworząc rodniki ponadtlenkowe, podczas gdy acetonitryl i jony chlorkowe reagują z dziurami, generując rodniki organiczne i rodniki chloru. Doświadczenia z selektywnym wygaszaniem tych krótkotrwałych gatunków pokazują, że zarówno rodniki chlorowe, jak i ponadtlenkowe są niezbędne do zerwania wiązań łączących atomy palladu w nanocząstkach. Symulacje ujawniają, że rodniki chloru najpierw przyłączają się do metalu, odciągając gęstość elektronową i osłabiając wiązania pallad–pallad. Następnie atakuje ponadtlenek, a chlorek z roztworu koordynuje uwolnione atomy, tworząc ruchomy kompleks pośredni. Ten kompleks jest elektrostatycznie przyciągany do dodatnio naładowanej powierzchni TiO2, gdzie traci chlorek i przy pomocy rodników organicznych oraz pobliskich miejsc zawierających azot i tlen, zakotwicza się jako pojedynczy atom palladu związany w stabilnym lokalnym środowisku.
Od mechanizmu w laboratorium do wszechstronnego narzędzia
Gdy mechanizm został wyjaśniony, zespół przetestował, jak szeroko stosowalna jest ta strategia. Pokazali, że podobne zabiegi świetlne mogą przekształcić nie tylko pallad, lecz także nanocząstki platyny i rodu w pojedyncze atomy na TiO2, a proces działa również na innym tlenkowym nośniku — tlenku wolframu (WO3). Większe cząstki palladu przygotowane konwencjonalną metodą redukcji chemicznej również można rozbić przy dłuższej ekspozycji na UV. Co najważniejsze z punktu widzenia zastosowań praktycznych, komercyjne katalizatory pallad na węglu oraz nawet przemysłowe odpadowe katalizatory, które utraciły aktywność, zostały pomyślnie odnowione: po obróbce razem z TiO2 pod światłem UV pallad stał się atomowo rozproszony, a wydajność katalizatorów w standardowej reakcji uwodorowania wzrosła prawie 18-krotnie dla materiału komercyjnego i 26-krotnie dla materiału odpadowego. Te ulepszone katalizatory pozostały też wysoce aktywne w kolejnych cyklach, a autorzy pokazują, że proces można prowadzić w układzie przepływowym i nawet napędzać światłem słonecznym. 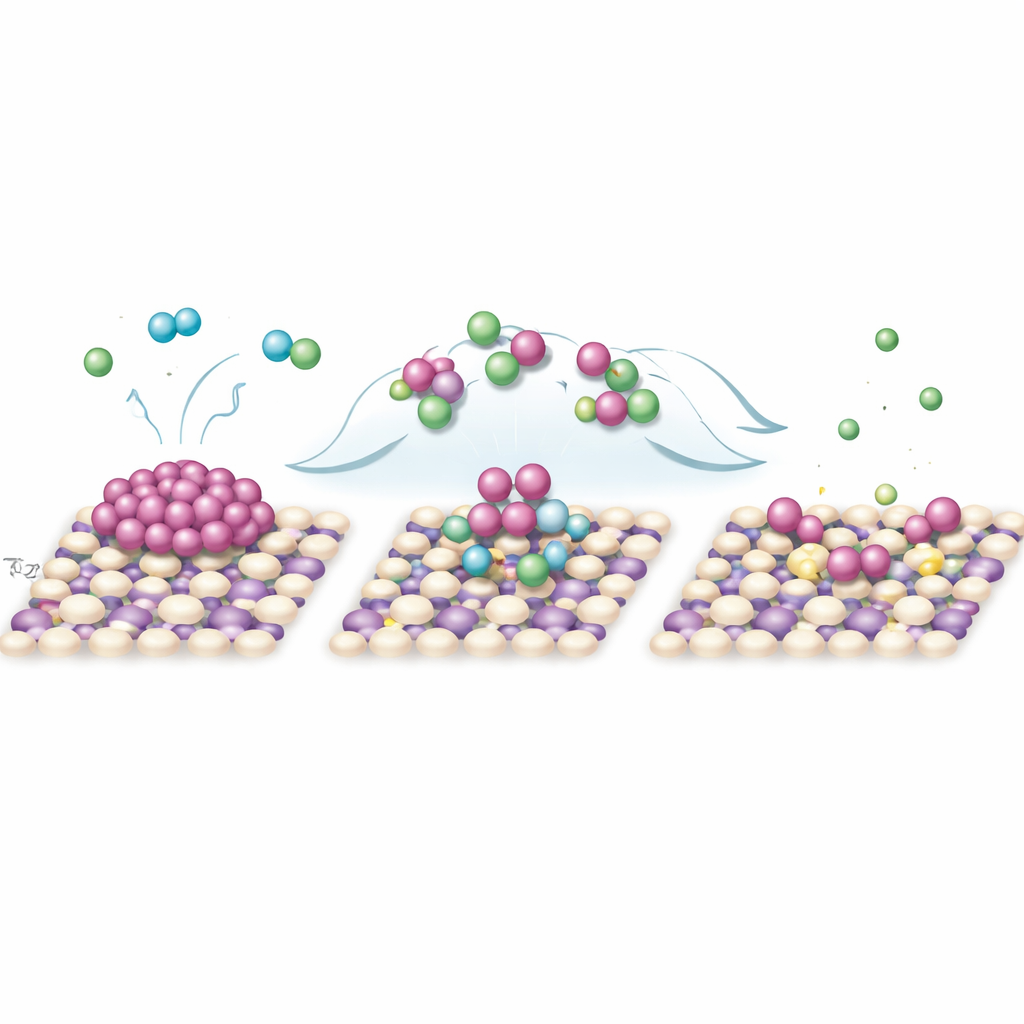
Prosta droga do bardziej ekologicznej katalizy
Dla czytelników nietechnicznych kluczowy przekaz jest taki: oświetlenie starannie dobranej mieszaniny może przeorganizować metale szlachetne ze skupisk w pojedynczo zakotwiczone atomy, bez konieczności stosowania wysokiej temperatury czy surowych warunków. To napędzane światłem „rozczłonkowanie” znacznie zwiększa efektywność wykorzystania każdego drogiego atomu metalu i może tchnąć nowe życie w zużyte katalizatory przemysłowe. Ponieważ metoda działa dla kilku ważnych metali, różnych nośników i rzeczywistych materiałów, oferuje obiecującą, przyjazną dla środowiska drogę do wydajniejszych i bardziej zrównoważonych procesów katalitycznych w przemyśle chemicznym i energetycznym.
Cytowanie: Chen, X., Zhao, Q., Zhang, J. et al. Photoinduced radical-mediated atomic dispersion of noble metal nanoparticles. Nat Commun 17, 3934 (2026). https://doi.org/10.1038/s41467-026-70742-3
Słowa kluczowe: katalizatory jednoatomowe, fotokataliza, nanocząstki metali szlachetnych, zielona chemia, regeneracja katalizatora