Clear Sky Science · pt
TYK2 media a neuroinflamação em cérebros com doença de Alzheimer e patologia TDP-43
Por que este estudo é importante para a saúde do cérebro
A doença de Alzheimer costuma ser descrita em termos de placas e emaranhados, mas muitos pacientes também apresentam um segundo tipo de dano, menos óbvio, envolvendo uma proteína chamada TDP-43 e inflamação cerebral persistente. Este estudo investiga como um interruptor imune específico, o TYK2, contribui para essa inflamação e perda de neurônios. Como já existem medicamentos que miram esse interruptor em outras doenças, o trabalho abre um caminho realista para tratamentos mais personalizados e focados na inflamação para um subconjunto de pessoas com Alzheimer e distúrbios relacionados.
Sinais de RNA ocultos em células cerebrais vulneráveis
Os autores concentraram-se numa molécula incomum chamada RNA de fita dupla encontrada no fluido de neurônios. Normalmente, nossas células usam RNA de fita simples como cópia de trabalho das instruções do DNA. Quando RNA de fita dupla aparece no lugar errado, a célula o trata como um sinal de perigo, parecido com um vírus. Ao examinar tecido cerebral de pessoas que tiveram Alzheimer, a equipe encontrou acúmulo desse RNA de fita dupla especificamente em neurônios que também continham agregados anormais de TDP-43 no corpo celular, em vez do núcleo onde essa proteína deveria estar. Esse pareamento não se sobrepôs aos sinais clássicos do Alzheimer — placas de amiloide e emaranhados de tau — sugerindo uma via adicional de dano que afeta apenas certos neurônios.
Inflamação amplificada por áreas do cérebro relacionadas ao pensamento
Para avaliar quão ampla poderia ser essa resposta de perigo, os pesquisadores analisaram grandes conjuntos de dados de atividade gênica de várias regiões cerebrais envolvidas na memória e no raciocínio. Eles descobriram que genes estimulados por interferon — genes ativados quando células detectam perigo do tipo viral — estavam consistentemente entre as vias mais fortemente ativadas em cérebros com Alzheimer em comparação com cérebros saudáveis. Regiões que se deterioram cedo na doença, como o giro parahipocampal e áreas frontais, mostraram ativação especialmente forte. Esse padrão apoia a ideia de que neurônios estão respondendo a sinais internos de estresse, incluindo RNA de fita dupla, e que a ativação crônica desse programa antiviral pode contribuir para inflamação cerebral contínua e degeneração.
Identificando quem pode se beneficiar dos medicamentos existentes
Como nem todas as pessoas com Alzheimer exibem os mesmos padrões moleculares, a equipe desenvolveu um pipeline refinado de aprendizado de máquina para prever quais pacientes poderiam responder a medicamentos que atenuam a sinalização por interferon. Eles usaram “marcas” sutis no RNA chamadas exons crípticos — pedaços extras de sequência que aparecem quando o TDP-43 deixa de cumprir sua função normal de processamento do RNA — como um indicador de problema com TDP-43 no cérebro. Pacientes cujas amostras cerebrais continham múltiplos exons crípticos foram rotulados como portadores de patologia TDP-43. Nesse subgrupo, mas não em outros, o modelo previu que dois medicamentos existentes — baricitinibe e ruxolitinibe, ambos inibidores de Janus quinase já aprovados para outras condições — tinham maior probabilidade de retardar mudanças moleculares relacionadas à doença. Isso sugere que futuros ensaios clínicos deveriam direcionar esses medicamentos especificamente a pacientes cuinas assinaturas moleculares indiquem inflamação associada ao TDP-43.
Um interruptor central: TYK2 e um bloqueador mais preciso
Para entender o mecanismo, os pesquisadores recriaram o sinal nocivo do RNA de fita dupla em vários modelos celulares neurais humanos. Em seguida, usaram uma triagem CRISPR em escala genômica — desligando sistematicamente genes por todo o genoma — para ver quais perdas mantinham as células vivas apesar do estresse por RNA. Uma quinase, TYK2, surgiu como um dos principais alvos ao lado de receptores de interferon e fatores regulatórios, colocando-a firmemente no centro da resposta tóxica. Quando os níveis de TYK2 foram reduzidos geneticamente, as células ficaram em grande parte protegidas da morte induzida por RNA de fita dupla. A equipe então testou deucravacitinibe, uma pílula altamente seletiva que bloqueia o TYK2 e foi aprovada recentemente para psoríase. Em múltiplos tipos celulares com características neuronais, esse medicamento preveniu a resposta danosa em doses muito menores do que inibidores JAK mais amplos, e suprimiu a sinalização inflamatória a jusante em análises ao nível proteico.
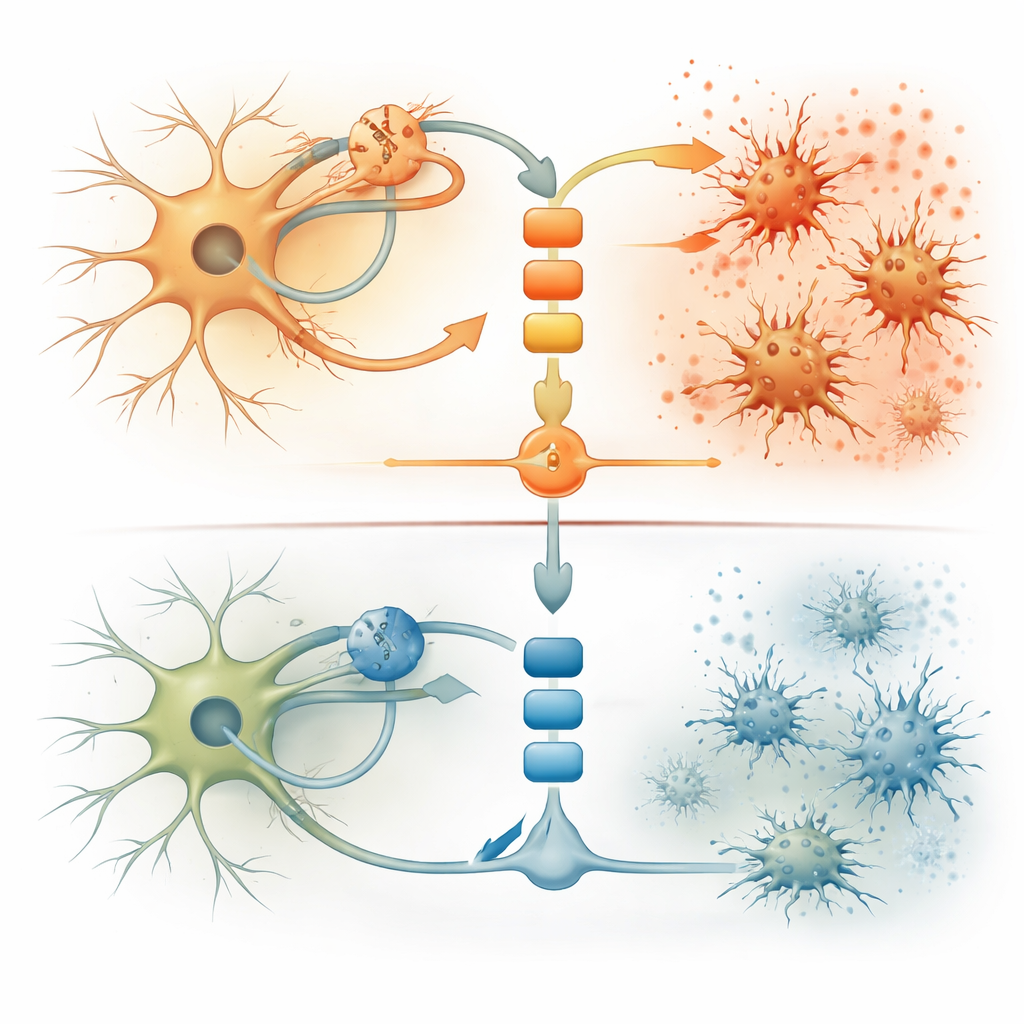
Encontrando uma pista simples no sangue para um processo cerebral complexo
Para que qualquer terapia futura seja direcionada às pessoas certas, os médicos precisarão de um marcador que reflita esse tipo particular de inflamação cerebral. Os pesquisadores recorreram a grandes conjuntos de dados genéticos e de proteínas sanguíneas de dezenas de milhares de voluntários. Pessoas que naturalmente carregam uma variante de perda parcial de função no gene TYK2 — essencialmente um regulador embutido que reduz a atividade desse interruptor imune — apresentaram níveis sanguíneos mais baixos de uma quimiocina chamada CXCL10. Em seus modelos celulares, o RNA de fita dupla aumentou fortemente a liberação de CXCL10, enquanto medicamentos que miravam o TYK2 reduziram esses níveis. Mesmo quando o TDP-43 foi experimentalmente deslocado do núcleo para agregados, o CXCL10 aumentou e foi melhor normalizado pelo inibidor seletivo de TYK2. Isso posiciona o CXCL10 no sangue ou no líquido cefalorraquidiano como um biomarcador promissor e testável para pacientes cuja neurodegeneração é impulsionada por essa via.
O que isso significa para tratamentos futuros
No conjunto, o estudo apoia uma visão na qual certos cérebros com Alzheimer — e aqueles com condições relacionadas como a ELA — desenvolvem um acúmulo lento de RNA de fita dupla associado à disfunção do TDP-43. Isso, por sua vez, aciona cronicamente um alarme antiviral dentro dos neurônios, com o TYK2 atuando como um botão de controle chave, levando finalmente à inflamação e morte celular. Ao combinar tecido cerebral humano, modelos celulares avançados, genética CRISPR, medições proteicas em grande escala e dados populacionais, os autores apresentam um argumento forte de que o TYK2 é um alvo viável para modificar a doença. Embora os medicamentos atuais contra o TYK2 possam não atravessar a barreira sangue–cérebro de forma eficiente ainda, o trabalho estabelece a base para inibidores de TYK2 com penetração cerebral e testes baseados em CXCL10 que poderiam inaugurar terapias mais precisas e personalizadas para um subgrupo definido de pessoas com Alzheimer e patologia TDP-43.
Citação: König, L.E., Rodriguez, S., Hug, C. et al. TYK2 mediates neuroinflammation in Alzheimer’s disease brains with TDP-43 pathology. Nat Commun 17, 3967 (2026). https://doi.org/10.1038/s41467-026-70243-3
Palavras-chave: Doença de Alzheimer, neuroinflamação, TDP-43, TYK2, RNA de fita dupla