Clear Sky Science · pt
Deconvolução dupla em microscopia de iluminação estruturada multiphotônica para imagem de super-resolução em tecidos profundos
Vendo mais fundo em tecidos vivos
A biologia moderna frequentemente depende de visualizar os menores detalhes dentro de pedaços espessos de tecido, como fatias de cérebro ou embriões em desenvolvimento. Infelizmente, à medida que a luz percorre esses ambientes densos, ela se dobra e se embaralha, tornando as imagens turvas justamente quando os cientistas mais desejam vistas nítidas. Este artigo apresenta uma maneira de “desembaçar” digitalmente essas imagens, permitindo que um microscópio avançado padrão revele estruturas extremamente finas no interior do tecido sem acrescentar hardware caro e complexo.
Por que a imagem em profundidade é tão difícil
Microscópios de fluorescência permitem aos pesquisadores marcar moléculas específicas e observar como células e tecidos são montados e comportam-se. Nas últimas décadas, vários métodos de “super-resolução” superaram os limites tradicionais de nitidez, revelando detalhes bem abaixo de 200 nanômetros. Contudo, a maioria desses métodos funciona bem apenas perto da superfície da amostra. Em tecidos espessos, como o cérebro de camundongo, tanto a luz usada para excitar os marcadores fluorescentes quanto a luz emitida de volta ao detector são distorcidas por pequenas variações na estrutura do tecido. Essas distorções, chamadas aberrações, borram o foco do microscópio e apagam informações de alto detalhe, especialmente em profundidades maiores do que algumas dezenas de micrômetros.
De correções por hardware para uma solução por software
Uma maneira popular de combater as aberrações é a óptica adaptativa baseada em hardware, que usa espelhos móveis ou outros dispositivos para remodelar a frente de onda da luz e restaurar um foco nítido. Embora poderosa, essa tecnologia é cara, tecnicamente exigente e frequentemente corrige distorções apenas para uma cor ou uma direção de propagação da luz por vez. Os autores propõem, em vez disso, uma abordagem computacional que funciona com um tipo de microscópio já comum em muitos laboratórios: o microscópio multiphotônico de varredura a laser. Ao substituir o detector de luz único usual por uma câmera, eles registram uma pilha rica de imagens varridas que codifica como tanto a excitação incidente quanto a fluorescência emitida foram distorcidas pelo tecido.
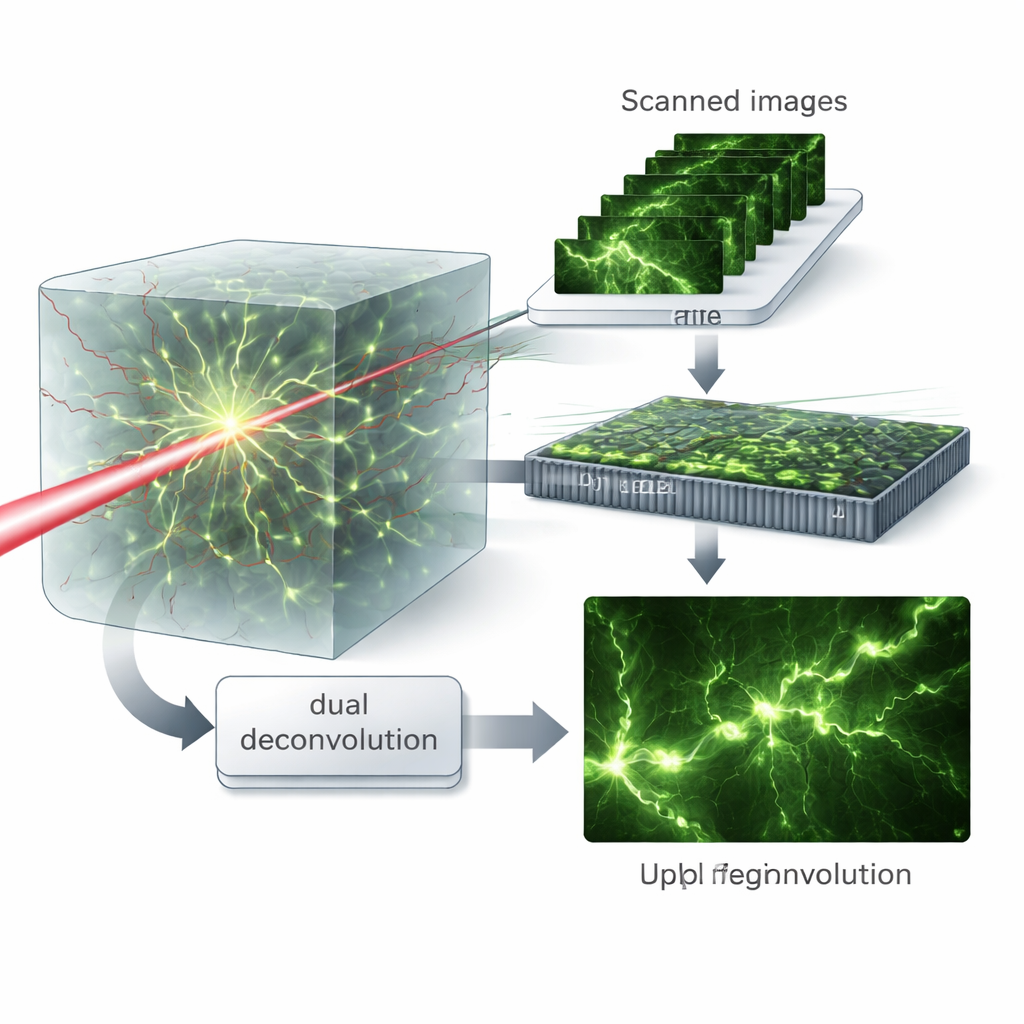
Padrões virtuais e limpeza dupla
O insight-chave é tratar as imagens varridas como se a amostra tivesse sido iluminada com muitos padrões finos diferentes de luz, um conceito que os autores chamam de iluminação estruturada virtual. Recombinar matematicamente esses dados no domínio da frequência permite separar os papéis dos processos de excitação e de emissão. Eles então introduzem um algoritmo de “deconvolução dupla” que estima e corrige alternadamente o borramento de cada lado — a luz que entra e a luz que sai — em vez de juntá-los em um único borrão efetivo. Esse tratamento baseado em matrizes preserva mais detalhes de alta frequência e permite que o algoritmo recupere estruturas finas mesmo quando as aberrações são intensas.
Vistas mais nítidas em simulações e amostras reais
Para testar seu método, a equipe primeiro usou simulações computacionais de microscopia por dois fótons, uma técnica de imagem em profundidade que utiliza pares de fótons de menor energia para excitar fluorescência apenas no ponto de foco. Sob distorções simuladas severas, as reconstruções convencionais por dois fótons e por iluminação estruturada padrão produziram imagens visivelmente borradas. Em contraste, a deconvolução dupla restaurou padrões nítidos cuja resolução se aproximou de um quarto do comprimento de onda da fluorescência — cerca de 130 nanômetros — correspondendo às previsões teóricas. Os autores então montaram um sistema dois-fótons personalizado com uma câmera científica e aplicaram seu algoritmo a amostras reais, incluindo esferas fluorescentes, padrões de teste escondidos atrás de camadas de espalhamento, células cultivadas, tecido cerebral de camundongo e zebrafish em montagens inteiras. Repetidamente, estruturas que apareciam borradas ou dobradas em imagens convencionais emergiram como feições claramente separadas após o processamento, e elementos neuronais finos, como espinhas dendríticas, permaneceram resolvíveis em profundidades de até 180 micrômetros no cérebro de camundongo.
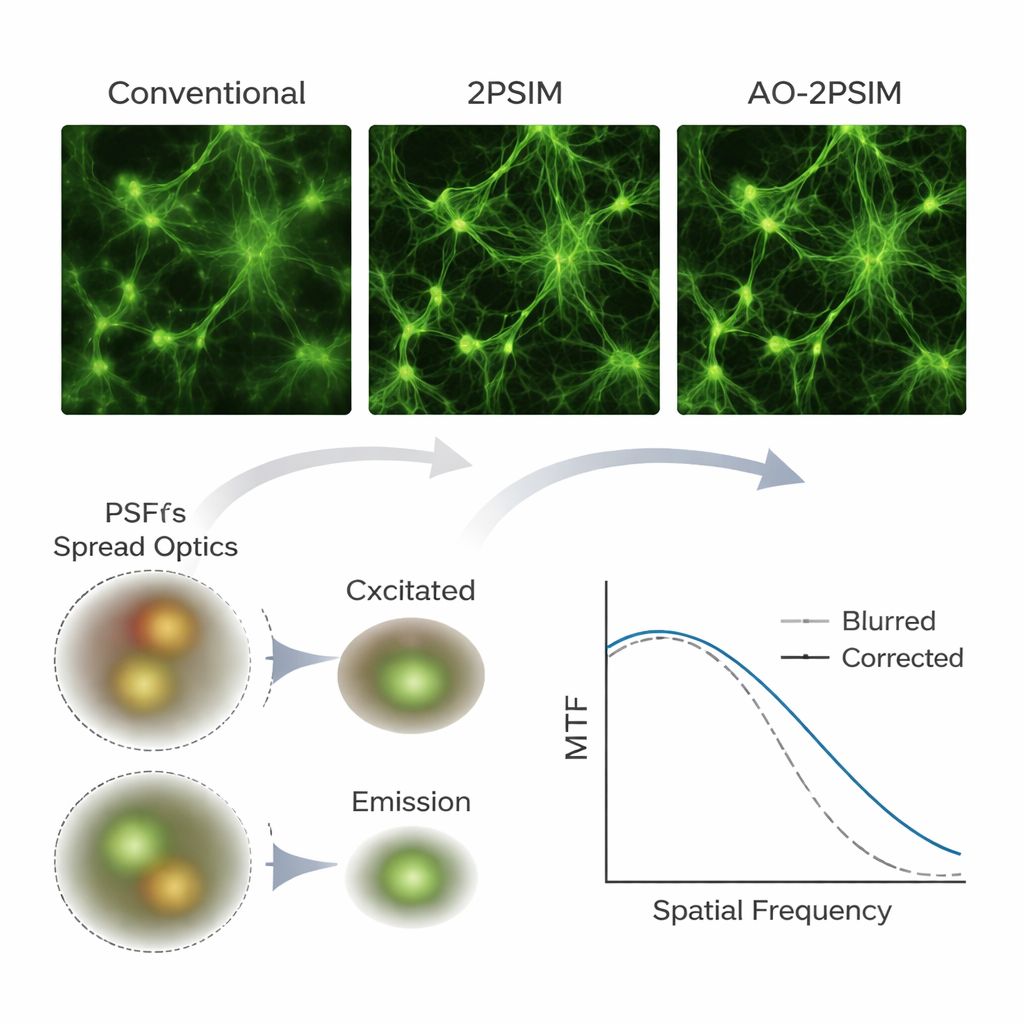
O que isso significa para a imagem biológica
Para não-especialistas, a mensagem principal é que os autores demonstraram como transformar microscópios multiphotônicos existentes em ferramentas de imagem de tecidos profundos muito mais potentes usando principalmente software e uma atualização para câmera. Ao modelar e corrigir cuidadosamente como os tecidos curvam a luz tanto na entrada quanto na saída, sua abordagem de deconvolução dupla dobra o limite usual de resolução em amostras espessas e desafiadoras sem depender de espelhos adaptativos complexos. Embora o método ainda dependa da coleta de sinal suficiente e atualmente exija varredura relativamente lenta, ele oferece um caminho prático e econômico rumo a vistas rotineiras ultranítidas do cérebro e de outros órgãos em três dimensões, abrindo portas para estudos mais detalhados sobre como estruturas biológicas são organizadas e mudam ao longo do tempo.
Citação: Lim, S., Kang, S., Hong, J.H. et al. Dual deconvolution in multiphoton structured illumination microscopy for deep-tissue super-resolution imaging. Nat Commun 17, 2123 (2026). https://doi.org/10.1038/s41467-026-69798-y
Palavras-chave: microscopia de super-resolução, imagens por dois fótons, óptica adaptativa, imagem em tecidos profundos, imagem computacional