Clear Sky Science · pt
Hidrogenação geral e seletiva catalisada por rutênio de amidas primárias a aminas primárias em condições brandas
Transformando ligações resistentes em blocos de construção úteis
Químicos dependem de aminas — pequenas moléculas que contêm nitrogênio — para fabricar desde medicamentos e agroquímicos até corantes e plásticos. Um enorme e pouco explorado reservatório de aminas potenciais está aprisionado dentro das amidas, as ligações químicas robustas que também mantêm as proteínas unidas. Este estudo apresenta uma nova maneira de “destrancar” suavemente uma grande variedade de amidas primárias e convertê‑las em aminas primárias valiosas usando gás hidrogênio, oferecendo uma rota mais limpa e versátil para muitos produtos cotidianos e de alta tecnologia. 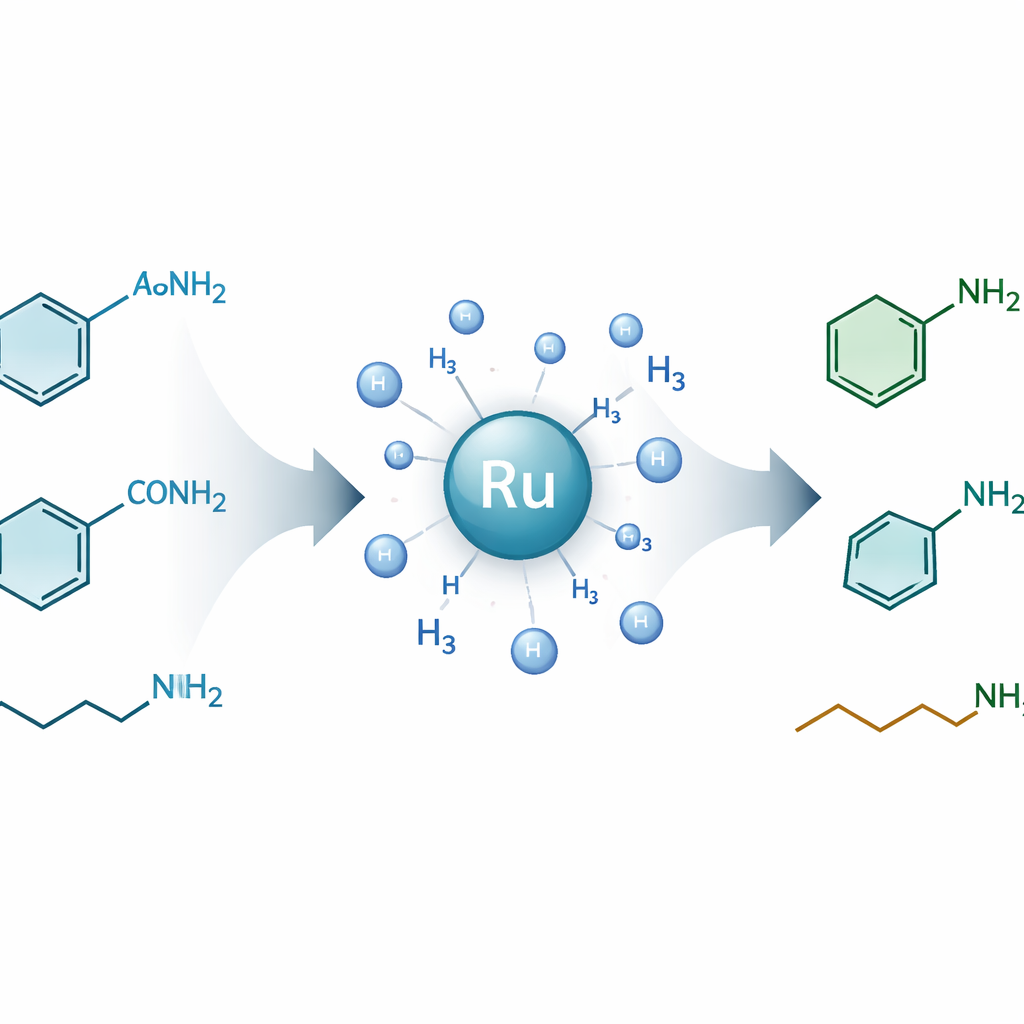
Por que quebrar amidas é tão difícil
Amidas estão entre as ligações mais resistentes na química orgânica, razão pela qual a natureza as usa para construir proteínas e a indústria as emprega em materiais duráveis. Essa mesma força, contudo, torna‑as notoriamente difíceis de modificar. Converter amidas em aminas parece simples — basta remover oxigênio e adicionar hidrogênio —, mas na prática a reação pode seguir muitos caminhos secundários, fragmentando a molécula ou reunindo pedaços de formas indesejadas. Métodos existentes costumam funcionar apenas para um conjunto restrito de amidas, exigem temperaturas e pressões muito altas ou produzem misturas de produtos difíceis de separar.
Um novo auxiliar para o hidrogênio
Os autores enfrentaram esse problema de longa data projetando um catalisador molecular específico à base do metal rutênio emparelhado com um ligante fosfina trifurcado personalizado contendo grupos metoxi (Triphos(p‑anisole)). Esse catalisador, formado in situ a partir de componentes baratos, ativa o gás hidrogênio e o direciona para as ligações corretas dentro da amida. Crucialmente, a reação é conduzida sob condições comparativamente brandas para uma tarefa tão difícil — cerca de 115 °C e pressão de hidrogênio de 10 bar, assistida por uma quantidade modesta de amônia e um solvente com forte capacidade de formar ligações de hidrogênio. Juntos, esses ingredientes permitem que o catalisador quebre a resistente ligação carbono–oxigênio da amida ao mesmo tempo em que preserva a frágil ligação carbono–nitrogênio que define a amina desejada.
De moléculas simples a medicamentos e materiais
Usando esse sistema catalítico, a equipe demonstrou sistematicamente que uma ampla gama de amidas primárias pode ser transformada em suas correspondentes aminas primárias com rendimentos de bons a excelentes. Amidas aromáticas, que contêm fragmentos em anel comuns em farmacêuticos, foram convertidas em aminas benzílicas, incluindo variantes decoradas com halogênios, éteres e outros grupos úteis. Amidas heteroaromáticas — aquelas que contêm nitrogênio ou oxigênio no anel — também deram aminas heterocíclicas importantes na descoberta de fármacos e na química de coordenação. O método funciona igualmente para amidas alifáticas de cadeia linear e cíclica, permitindo a preparação de aminas biogênicas como dopamina, tiramina, fenetilamina e histamina, que desempenham papéis-chave como neurotransmissores e moléculas de sinalização no organismo. 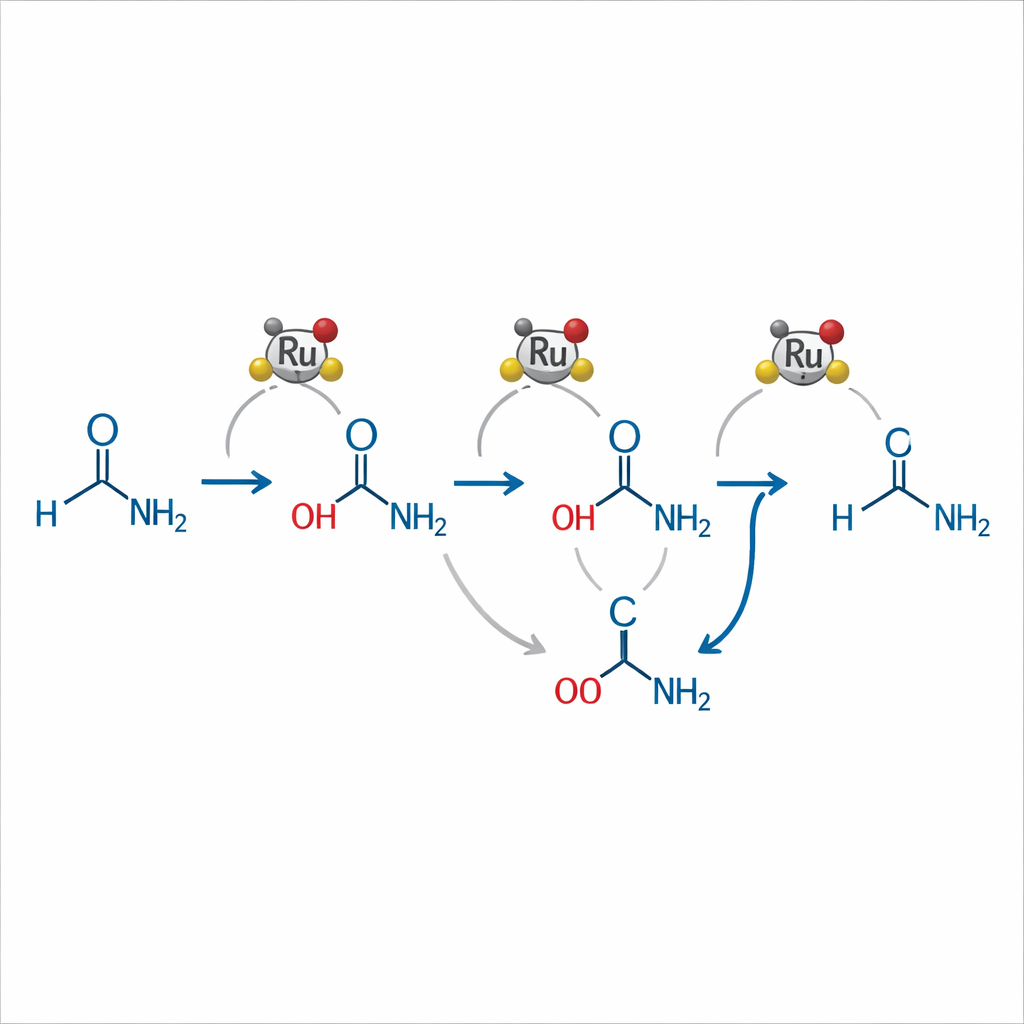
Novo acesso a moléculas funcionais do dia a dia
Além de pequenas moléculas bioativas, o catalisador pode converter amidas gordurosas — derivadas de óleos e gorduras naturais — em aminas graxas de cadeia longa. Esses compostos são agentes de grande utilidade na vida moderna, usados como surfactantes, amaciantes de tecido, inibidores de corrosão e aditivos em asfalto e outros materiais. A nova rota oferece uma alternativa complementar à prática industrial atual de partir de nitrilas, potencialmente permitindo um uso mais flexível de matérias‑primas renováveis, como óleos vegetais. Os pesquisadores também mostraram que seu catalisador se comporta de forma diferente com amidas secundárias e terciárias, favorecendo amidas primárias e ressaltando sua seletividade.
Como o catalisador orienta a reação
Para entender como seu sistema funciona, os autores combinaram estudos cuidadosos dos produtos com experimentos de ressonância magnética nuclear em alta pressão. Eles propõem que o complexo de rutênio primeiro forma uma espécie di-hidreto que adiciona hidrogênio através da amida, gerando um intermediário instável do tipo «hemiaminal». A partir daí, dois caminhos principais são possíveis: desidratação até um imina que é então reduzida à amina, ou clivagem que forma brevemente um álcool, o qual é convertido de volta em uma imina e, finalmente, na amina. A amônia desempenha um papel sutil porém central — deslocando equilíbrios de reação para longe de produtos de acoplamento indesejados, promovendo a conversão de álcoois em iminas e estabilizando um estado de repouso do catalisador que pode ser reativado pelo hidrogênio.
Um passo rumo a uma fabricação química mais verde
Em termos práticos, este trabalho fornece uma ferramenta geral e seletiva para transformar amidas robustas em aminas primárias versáteis usando gás hidrogênio, um agente redutor limpo que produz água como único subproduto. Ao operar sob condições significativamente mais brandas do que métodos anteriores e tolerar muitas estruturas moleculares diferentes, o catalisador rutênio–Triphos(p‑anisole) abre novas possibilidades para a síntese sustentável de produtos farmacêuticos, químicos especiais, polímeros e materiais à base de aminas graxas a partir de precursores de amida abundantes.
Citação: Kuloor, C., Goyal, V., Ma, Z. et al. General and selective ruthenium-catalyzed hydrogenation of primary amides to primary amines under mild conditions. Nat Commun 17, 3525 (2026). https://doi.org/10.1038/s41467-026-69794-2
Palavras-chave: hidrogenação de amidas, catálise por rutênio, aminas primárias, química verde, aminas graxas