Clear Sky Science · de
Allgemeine und selektive Ruthenium‑katalysierte Hydrierung von primären Amiden zu primären Aminen unter milden Bedingungen
Harte Bindungen in nützliche Bausteine verwandeln
Chemikerinnen und Chemiker verlassen sich auf Amine – kleine, stickstoffhaltige Moleküle –, um alles von Arzneimitteln und Pflanzenschutzmitteln bis zu Farbstoffen und Kunststoffen herzustellen. Ein großes und bislang wenig genutztes Reservoir potenzieller Amine ist in Amiden gebunden, den stabilen chemischen Verknüpfungen, die auch Proteine zusammenhalten. Diese Studie stellt eine neue Methode vor, um eine breite Palette primärer Amide schonend „aufzuschließen“ und mit Wasserstoffgas in wertvolle primäre Amine umzuwandeln. Das bietet einen saubereren, vielseitigeren Weg zu vielen Alltags‑ und Hightech‑Produkten. 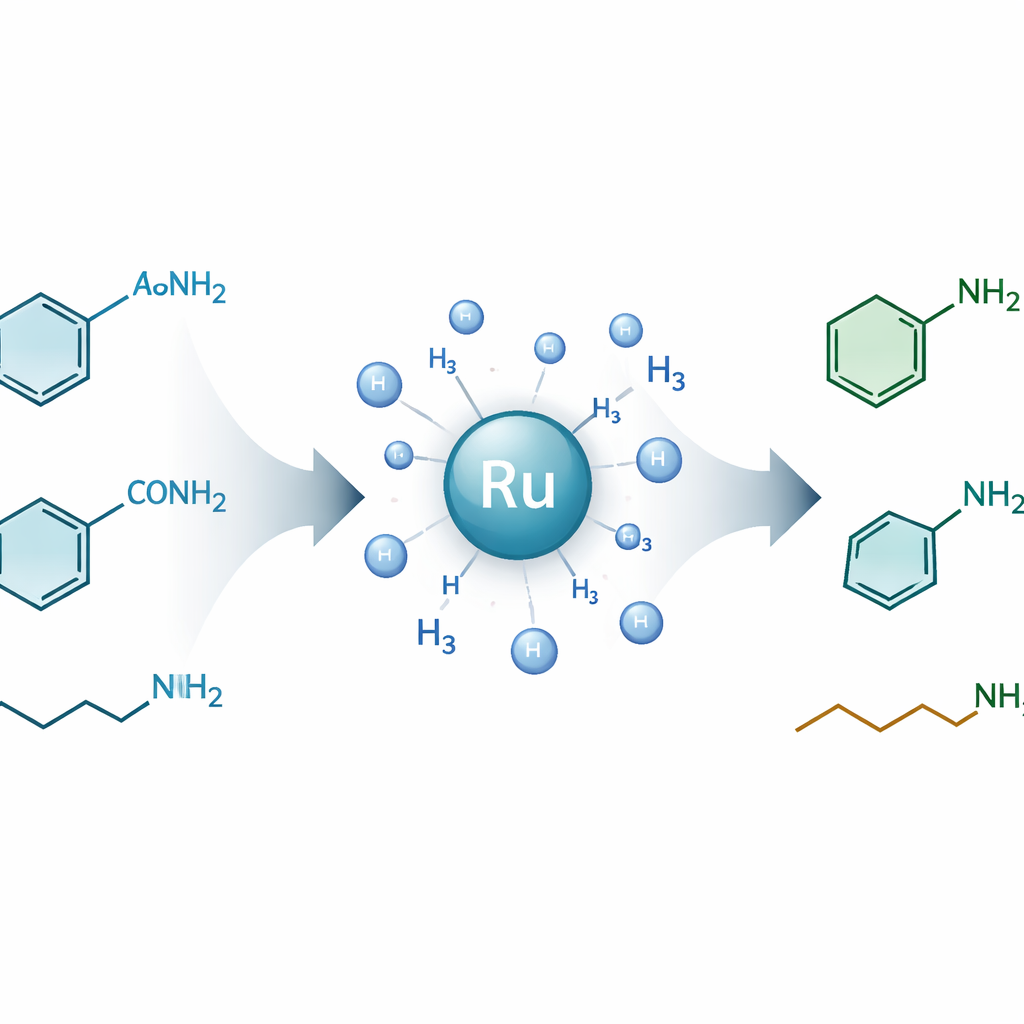
Warum das Brechen von Amiden so schwer ist
Amide zählen zu den widerstandsfähigsten Bindungen in der organischen Chemie, weshalb die Natur sie zum Aufbau von Proteinen nutzt und die Industrie sie in langlebigen Materialien einsetzt. Dieselbe Stärke macht sie jedoch berüchtigt schwer zu verändern. Amide in Amine umzuwandeln klingt einfach – Sauerstoff entfernen und Wasserstoff hinzufügen – in der Praxis kann die Reaktion aber in viele Nebenwege abgleiten, das Molekül zerschneiden oder Fragmente unerwünscht aneinanderheften. Bestehende Methoden funktionieren meist nur für eine enge Auswahl von Amiden, erfordern sehr hohe Temperaturen und Drücke oder liefern Produktgemische, die schwer zu trennen sind.
Ein neuer Helfer für Wasserstoff
Die Autoren gingen dieses langjährige Problem an, indem sie einen spezifischen molekularen Katalysator auf Basis des Metalls Ruthenium mit einem maßgeschneiderten, dreifach verankerten Phosphinliganden mit Methoxygruppen (Triphos(p‑anisol)) entwickelten. Dieser Katalysator, in situ aus kostengünstigen Komponenten gebildet, aktiviert Wasserstoffgas und lenkt ihn auf die richtigen Bindungen im Amid. Entscheidend ist, dass die Reaktion unter vergleichsweise milden Bedingungen für eine so schwierige Aufgabe abläuft – etwa 115 °C und ein Wasserstoffdruck von 10 bar, unterstützt durch eine moderate Menge Ammoniak und ein stark wasserstoffbrückenbildendes Lösungsmittel. Zusammengenommen erlauben diese Zutaten dem Katalysator, die harte Kohlenstoff‑Sauerstoff‑Verbindung im Amid zu spalten und gleichzeitig die empfindliche Kohlenstoff‑Stickstoff‑Bindung zu erhalten, die das gewünschte Amin ausmacht.
Von einfachen Molekülen zu Arzneimitteln und Materialien
Mithilfe dieses Katalysatorsystems zeigten die Forschenden systematisch, dass eine breite Palette primärer Amide in gute bis ausgezeichnete Ausbeuten in die entsprechenden primären Amine überführt werden kann. Aromatische Amide, die ringförmige Fragmente enthalten, wie sie in Pharmawirkstoffen häufig vorkommen, wurden zu benzylicen Aminen umgewandelt, einschließlich Varianten mit Halogenen, Ether‑Gruppen und anderen nützlichen Substituenten. Heteroaromatische Amide – solche mit Stickstoff oder Sauerstoff im Ring – lieferten entsprechend heterocyclische Amine, die in der Wirkstoffforschung und Koordinationschemie wichtig sind. Die Methode funktioniert auch für geradkettige und cyclische aliphatische Amide und ermöglicht die Herstellung biogener Amine wie Dopamin, Tyramin, Phenethylamin und Histamin, die als Neurotransmitter und Signalmoleküle im Körper zentrale Rollen spielen. 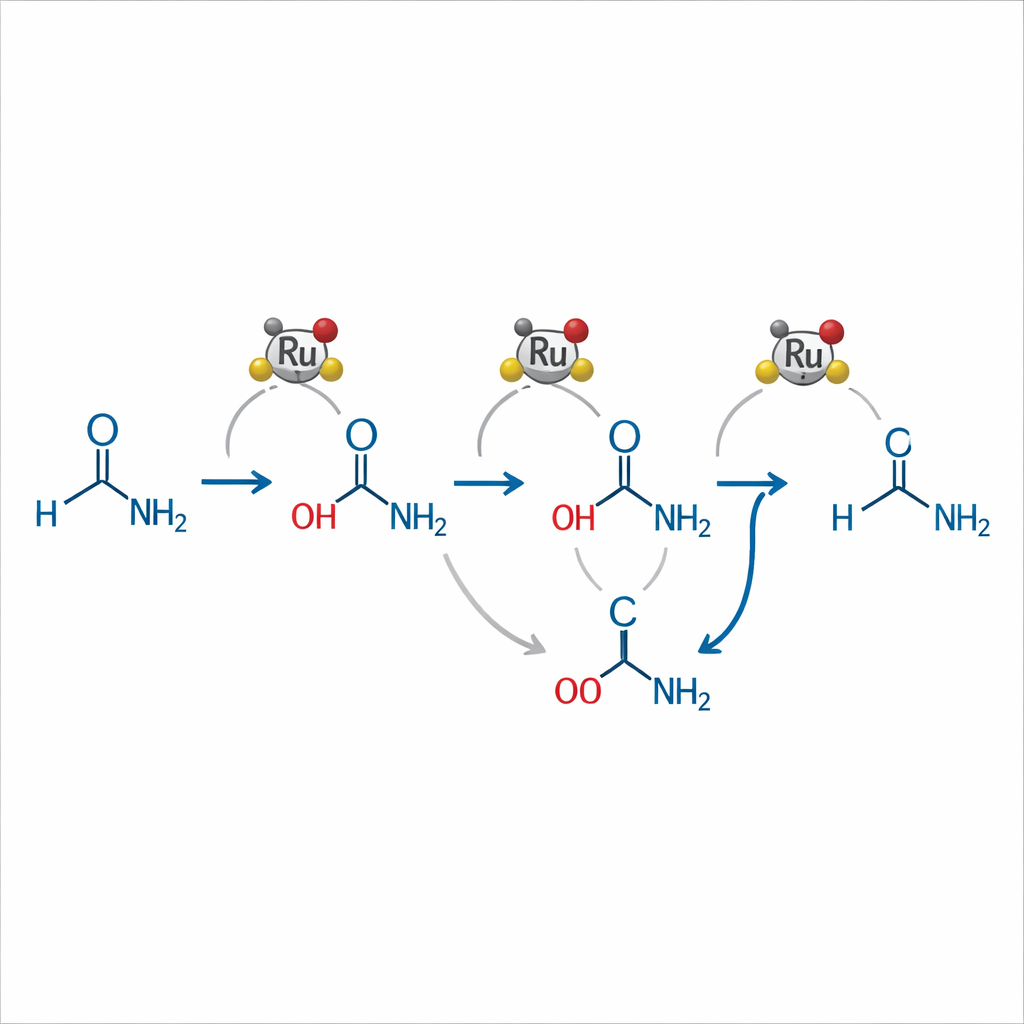
Neuer Zugang zu alltäglichen Funktionsmolekülen
Über kleine bioaktive Moleküle hinaus kann der Katalysator fetthaltige Amide – gewonnen aus natürlichen Ölen und Fetten – in langkettige Fettamine umwandeln. Diese Verbindungen sind Alltagshelfer der modernen Welt: Sie werden als Tenside, Weichmacher für Textilien, Korrosionsinhibitoren und als Zusatzstoffe in Asphalt und anderen Materialien eingesetzt. Der neue Weg bietet eine komplementäre Alternative zur derzeitigen industriellen Praxis, die oft bei Nitrilen beginnt, und ermöglicht potenziell eine flexiblere Nutzung erneuerbarer Rohstoffe wie Pflanzenöle. Die Forschenden zeigten außerdem, dass ihr Katalysator sich bei sekundären und tertiären Amiden anders verhält, wobei primäre Amide bevorzugt werden und damit seine Selektivität unterstrichen wird.
Wie der Katalysator die Reaktion steuert
Um zu verstehen, wie ihr System funktioniert, kombinierten die Autoren sorgfältige Produktanalysen mit Hochdruck‑NMR‑Experimenten. Sie schlagen vor, dass das Rutheniumkomplex zunächst eine Dihydrid‑Spezies bildet, die Wasserstoff über das Amid addiert und ein instabiles „Hemiaminal“‑Intermediat liefert. Von dort sind zwei Hauptwege möglich: Dehydratation zu einem Imin, das anschließend zum Amin reduziert wird, oder eine Spaltung, die kurzzeitig einen Alkohol bildet, welcher wieder in ein Imin und schließlich in das Amin überführt wird. Ammoniak spielt eine subtile, aber zentrale Rolle – es verschiebt Reaktionsgleichgewichte weg von unerwünschten Kopplungsprodukten, fördert die Umwandlung von Alkoholen zu Iminen und stabilisiert einen Ruhezustand des Katalysators, der durch Wasserstoff reaktivierbar ist.
Ein Schritt zu grünerer chemischer Herstellung
Praktisch liefert diese Arbeit ein allgemeines, selektives Werkzeug, um robuste Amide mit Wasserstoffgas – einem sauberen Reduktionsmittel, das als einziges Nebenprodukt Wasser erzeugt – in vielseitige primäre Amine zu überführen. Durch das Arbeiten unter deutlich milderen Bedingungen als frühere Methoden und die Verträglichkeit mit vielen unterschiedlichen Molekülstrukturen eröffnet der Ruthenium–Triphos(p‑anisol)‑Katalysator neue Möglichkeiten für eine nachhaltige Synthese von Arzneimitteln, Spezialchemikalien, Polymeren und auf fettsäurebasierten Aminen beruhenden Materialien aus leicht verfügbaren Amidvorstufen.
Zitation: Kuloor, C., Goyal, V., Ma, Z. et al. General and selective ruthenium-catalyzed hydrogenation of primary amides to primary amines under mild conditions. Nat Commun 17, 3525 (2026). https://doi.org/10.1038/s41467-026-69794-2
Schlüsselwörter: Amid‑Hydrierung, Ruthenium‑Katalyse, primäre Amine, grüne Chemie, fettsäurebasierte Amine