Clear Sky Science · pt
Formação rápida mediada por interface de derivados tóxicos de ésteres ftálicos
Perigos ocultos em gotas cotidianas
Muitos dos plásticos que tornam a vida moderna conveniente liberam silenciosamente substâncias chamadas ésteres ftálicos para o ar e a água. Essas substâncias já são conhecidas por prejudicar os pulmões, o fígado e o desenvolvimento infantil, e há muito tempo são consideradas poluentes persistentes que se degradam muito lentamente. Este estudo revela uma reviravolta surpreendente: nas superfícies de minúsculas gotículas de água em suspensão — como as de nuvens, aerossóis marinhos ou umidificadores domésticos — os ftalatos podem se transformar em minutos em novos compostos que frequentemente são ainda mais tóxicos do que os originais.
Por que gotículas minúsculas importam
Tendemos a imaginar a poluição como algo diluído em grandes volumes de ar ou água, mas uma enorme quantidade de química ocorre exatamente onde o ar e a água se encontram. O mundo está repleto de gotículas microscópicas: em névoa e nuvens, no spray marinho sobre os oceanos e na névoa de umidificadores ultrassônicos em ambientes internos. A área de superfície combinada dessas gotículas é colossal — somente as gotas de nuvem oferecem ordens de magnitude mais área de superfície do que toda a terra e os oceanos do planeta. Ainda assim, a maioria dos modelos de poluição assume que as substâncias se comportam como se estivessem em ar ou água homogêneos, negligenciando o que acontece nessas peles interfaciais finas.
Uma fábrica de reações de ação rápida na superfície
Os pesquisadores construíram um reator “sem contato” que imita o princípio de funcionamento de um umidificador ultrassônico doméstico. Eles pulverizaram água contendo vários ftalatos comuns em uma câmara selada, gerando microgotículas de dezenas de micrômetros de diâmetro. Ao amostrar o líquido ao longo do tempo e analisá‑lo por cromatografia de alta resolução e espectrometria de massas, acompanharam quão rapidamente um ftalato representativo, o diisobutilftalato (DiBP), desaparecia e em que se convertia. Nas superfícies das gotas, cerca de 97% do DiBP se degradou em 12 minutos, com meia‑vida de apenas 2,4 minutos — uma aceleração assombrosa de 4 a 11 ordens de magnitude em comparação com a degradação típica em água ou ar em massa, onde esses compostos podem persistir por anos.
Como as superfícies aquosas turboalimentam as reações
A chave para essa transformação rápida está em como os ftalatos e a água se organizam na superfície da gota. Simulações por computador mostraram que o DiBP prefere se posicionar na fronteira ar–água, onde suas partes hidrofílicas e hidrofóbicas podem ser parcialmente satisfeitas. Ao mesmo tempo, a superfície da gota gera espontaneamente radicais hidroxila extremamente reativos — pequenos agentes oxidantes que se formam sem a necessidade de luz, aquecimento ou adição de químicos externos. Experimentos que “inativaram” seletivamente diferentes espécies reativas, junto com medições de spin eletrônico, confirmaram que esses radicais hidroxila dominam a reação. Eles atacam as partes expostas das moléculas de ftalato, rompendo ligaduras e adicionando oxigênio de forma sequencial. Cálculos mecânico‑quânticos detalhados revelaram que esses passos habilitados pela superfície exigem muito menos energia do que as mesmas reações em água em massa, explicando a enorme aceleração.
De poluente a algo pior
Ao combinar medições experimentais com buscas automatizadas de estruturas, a equipe identificou um conjunto de produtos de transformação. O ftalato parental primeiro perde trechos de suas cadeias laterais e ganha grupos hidroxila, sendo então convertido principalmente em produtos “carboxilados”, incluindo monoisobutilftalato e ácido ftálico. Usando ferramentas avançadas de previsão toxicológica, os autores compararam os riscos à saúde desses produtos com o DiBP original. O padrão foi preocupante: para diversos desfechos de saúde humana, os produtos carboxilados mostraram‑se muito mais nocivos, com previsões de toxicidade hepática até 37,5 vezes maiores, potencial de dano respiratório 4,5 a 15 vezes superior e poder corrosivo ocular substancialmente mais forte. Mesmo os intermediários hidroxilados exibiram aumento no potencial de sensibilização cutânea, apesar de toxicidade aguda aquática um pouco menor.
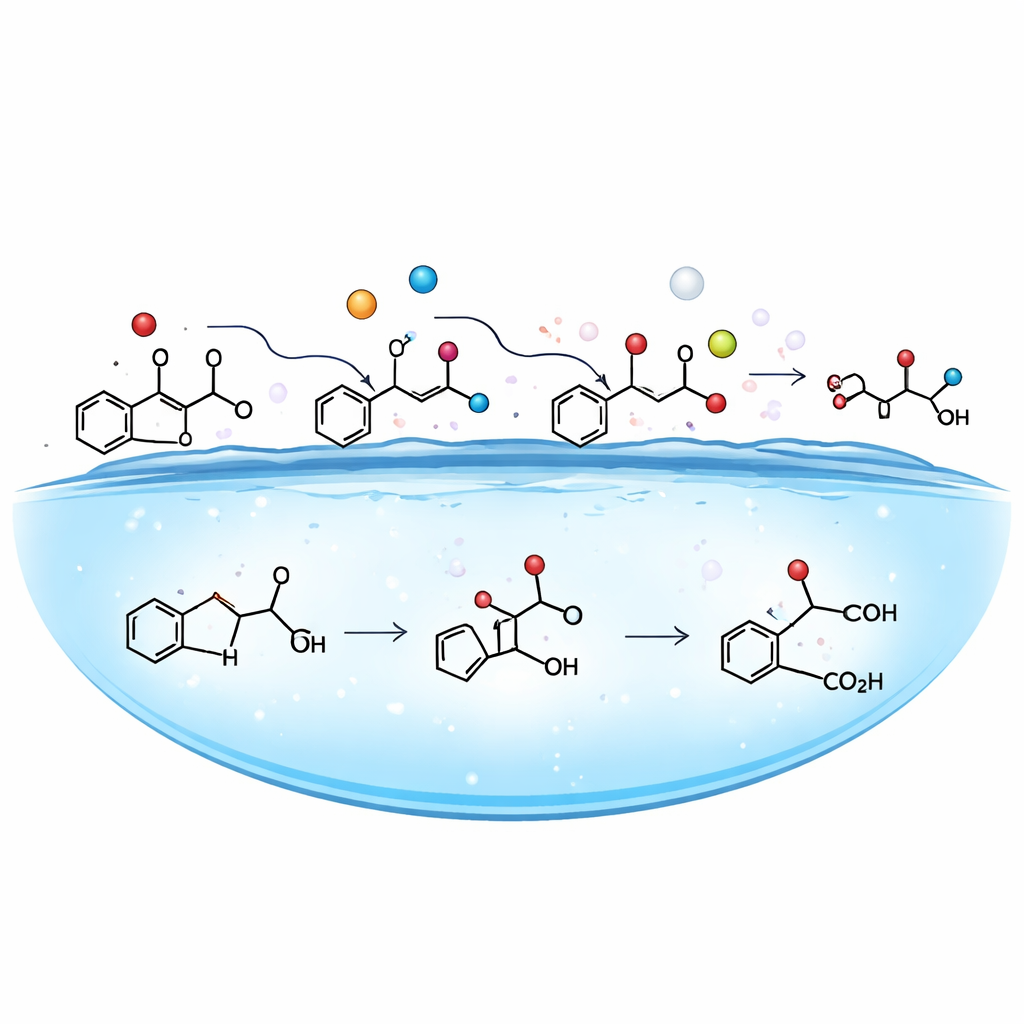
Implicações para residências, nuvens e políticas
Como as microgotículas têm vidas curtas — de segundos em névoas internas a horas em nevoeiros — a degradação completa dos ftalatos até produtos finais inofensivos é improvável antes da evaporação das gotas. Em vez disso, pessoas e ecossistemas têm maior probabilidade de serem expostos aos produtos intermediários, que este trabalho mostra poderem ser mais perigosos que os compostos‑pais. Em ambientes internos, onde as pessoas passam cerca de 90% do tempo, umidificadores ultrassônicos funcionam de maneira semelhante ao reator experimental, acelerando a transformação de ftalatos justamente onde se respira. Isso ajuda a explicar por que usuários podem apresentar níveis mais baixos dos ftalatos originais, mas ainda assim enfrentar risco aumentado devido a seus derivados mais tóxicos. O estudo argumenta que modelos ambientais e regulamentações devem ir além de tratar ftalatos — e, por extensão, muitos outros compostos contendo ésteres — apenas em termos de sua lenta decaída em fase de massa. Em vez disso, devem considerar a química rápida dirigida por superfícies em microgotículas onipresentes e avaliar explicitamente a toxicidade dos produtos gerados ao longo do processo.
Citação: Li, X., Jiang, Q., Xia, D. et al. Interfacial-mediated fast formation of toxic derivatives of phthalate esters. Nat Commun 17, 2823 (2026). https://doi.org/10.1038/s41467-026-69495-w
Palavras-chave: ésteres ftálicos, microgotículas, interface ar–água, produtos de transformação, saúde ambiental