Clear Sky Science · es
Formación rápida mediada por la interfaz de derivados tóxicos de ésteres ftálicos
Peligros ocultos en gotas cotidianas
Muchos de los plásticos que hacen la vida moderna más cómoda liberan silenciosamente sustancias llamadas ésteres ftálicos al aire y al agua. Ya se sabe que estas sustancias dañan los pulmones, el hígado y el desarrollo infantil, y durante mucho tiempo se han considerado contaminantes persistentes que se degradan solo muy despacio. Este estudio revela un giro sorprendente: en las superficies de diminutas gotas de agua en suspensión —como las de las nubes, la bruma marina o los humidificadores domésticos— los ftalatos pueden transformarse en minutos en nuevos compuestos que a menudo son incluso más tóxicos que los originales.
Por qué importan las microgotas
Solemos imaginar la contaminación como algo diluido en grandes volúmenes de aire o agua, pero una enorme cantidad de química ocurre realmente donde el aire y el agua se encuentran. El mundo está lleno de gotas microscópicas: en la niebla y las nubes, en la bruma sobre los océanos y en el vapor de los humidificadores ultrasónicos en interiores. La superficie combinada de estas gotas es enorme: solo las gotas de las nubes ofrecen decenas de veces más área superficial que toda la tierra y los océanos del planeta. Sin embargo, la mayoría de los modelos de contaminación siguen asumiendo que las sustancias se comportan como si estuvieran en aire o agua homogéneos, pasando por alto lo que sucede en estas finas pieles interfaciales.
Una fábrica de reacciones de acción rápida en la superficie
Los investigadores construyeron un reactor “sin contacto” que imita el principio de funcionamiento de un humidificador ultrasónico doméstico. Pulverizaron agua que contenía varios ftalatos comunes dentro de una cámara sellada, generando microgotas de decenas de micrómetros de diámetro. Al muestrear el líquido con el tiempo y analizarlo mediante cromatografía de alta resolución y espectrometría de masas, siguieron la rapidez con que un ftalato representativo, el diisobutil ftalato (DiBP), desaparecía y en qué se transformaba. En las superficies de las gotas, aproximadamente el 97 % del DiBP se descompuso en 12 minutos, con una vida media de solo 2,4 minutos—una aceleración asombrosa de 4 a 11 órdenes de magnitud en comparación con la degradación típica en agua o aire a granel, donde estos compuestos pueden persistir durante años.
Cómo las superficies acuosas supercargan las reacciones
La clave de esta rápida transformación radica en cómo se disponen los ftalatos y el agua en la superficie de la gota. Las simulaciones por ordenador mostraron que el DiBP prefiere situarse en la frontera aire–agua, donde sus partes hidrófilas e hidrófobas pueden quedar parcialmente satisfechas. Al mismo tiempo, la superficie de la gota genera espontáneamente radicales hidroxilo extremadamente reactivos—pequeños agentes oxidantes que se forman sin necesidad de luz, calor o reactivos externos. Experimentos que “apagaron” selectivamente distintas especies reactivas, junto con mediciones de espín electrónico, confirmaron que estos radicales hidroxilo dominan la reacción. Atacan las partes expuestas de las moléculas de ftalato, rompiendo enlaces y añadiendo oxígeno de forma escalonada. Cálculos mecánico‑cuánticos detallados revelaron que estos pasos facilitados por la superficie requieren mucha menos energía que las mismas reacciones en agua a granel, lo que explica la enorme aceleración.
De contaminante a algo peor
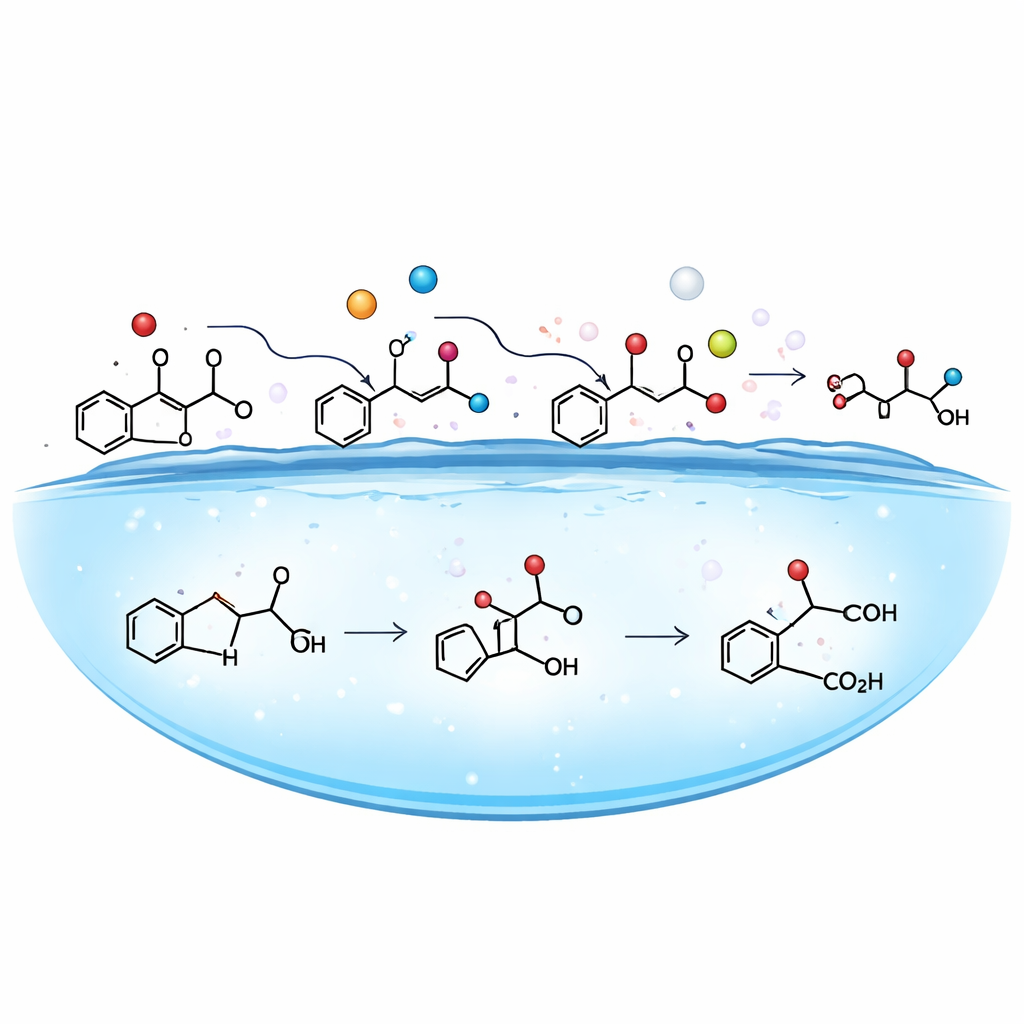
Combinando mediciones experimentales con búsquedas automatizadas de estructuras, el equipo identificó una serie de productos de transformación. El ftalato parental primero pierde fragmentos de sus cadenas laterales y gana grupos hidroxilo, y luego se convierte principalmente en productos “carboxilados”, incluidos monoisobutil ftalato y ácido ftálico. Usando herramientas avanzadas de predicción toxicológica, los autores compararon los riesgos para la salud de estos productos con los del DiBP original. El patrón fue preocupante: para varios indicadores de salud humana, los productos carboxilados resultaron mucho más dañinos, mostrando hasta 37,5 veces mayor toxicidad hepática predicha, de 4,5 a 15 veces más potencial de dañar el sistema respiratorio y una capacidad de corroer los ojos sustancialmente mayor. Incluso los intermedios hidroxilados mostraron un mayor potencial sensibilizante cutáneo, pese a una toxicidad aguda algo menor para organismos acuáticos.
Implicaciones para hogares, nubes y políticas
Dado que las microgotas tienen vidas cortas—desde segundos en nieblas interiores hasta horas en la niebla—es improbable que la degradación completa de los ftalatos hasta productos finales inocuos ocurra antes de que las gotas se evaporen. En cambio, las personas y los ecosistemas tienen más probabilidades de encontrarse con los productos intermedios, que este trabajo muestra pueden ser más peligrosos que los compuestos parentales. En interiores, donde las personas pasan alrededor del 90 % de su tiempo, los humidificadores ultrasónicos actúan de forma muy parecida al reactor experimental, acelerando la transformación de ftalatos justo donde se respira. Esto ayuda a explicar por qué los usuarios pueden presentar niveles más bajos de los ftalatos originales pero aun así enfrentar un riesgo aumentado por sus derivados más tóxicos. El estudio sostiene que los modelos ambientales y las regulaciones deben ir más allá de tratar a los ftalatos —y por extensión a muchos otros compuestos que contienen ésteres— únicamente en términos de su lenta degradación en fase a granel. En su lugar, deben tener en cuenta la química rápida impulsada por las superficies en microgotas ubicuas y considerar explícitamente la toxicidad de los productos que se generan en el proceso.
Cita: Li, X., Jiang, Q., Xia, D. et al. Interfacial-mediated fast formation of toxic derivatives of phthalate esters. Nat Commun 17, 2823 (2026). https://doi.org/10.1038/s41467-026-69495-w
Palabras clave: ésteres ftálicos, microgotas, interfaz aire–agua, productos de transformación, salud ambiental