Clear Sky Science · pl
Optymalizacja interfejsów neuroprotetycznych oparta na biofizycznych i zastępczych cyfrowych bliźniakach
Przeprogramowywanie ciała za pomocą inteligentniejszych implantów
Od łagodzenia bólu przewlekłego po przywracanie wzroku i ruchu po paraliżu — małe urządzenia elektryczne komunikujące się z naszymi nerwami cicho przekształcają medycynę. Jednak dziś wiele systemów neuroprotetycznych jest konfigurowanych metodą prób i błędów przy łóżku pacjenta. Artykuł wyjaśnia, jak „cyfrowe bliźniaki” — komputerowe repliki nerwów i mózgu pacjenta — mogą zamienić to zgadywanie w precyzyjniejszą naukę, czyniąc implanty bezpieczniejszymi, skuteczniejszymi i łatwiejszymi do dopasowania do indywidualnych potrzeb.
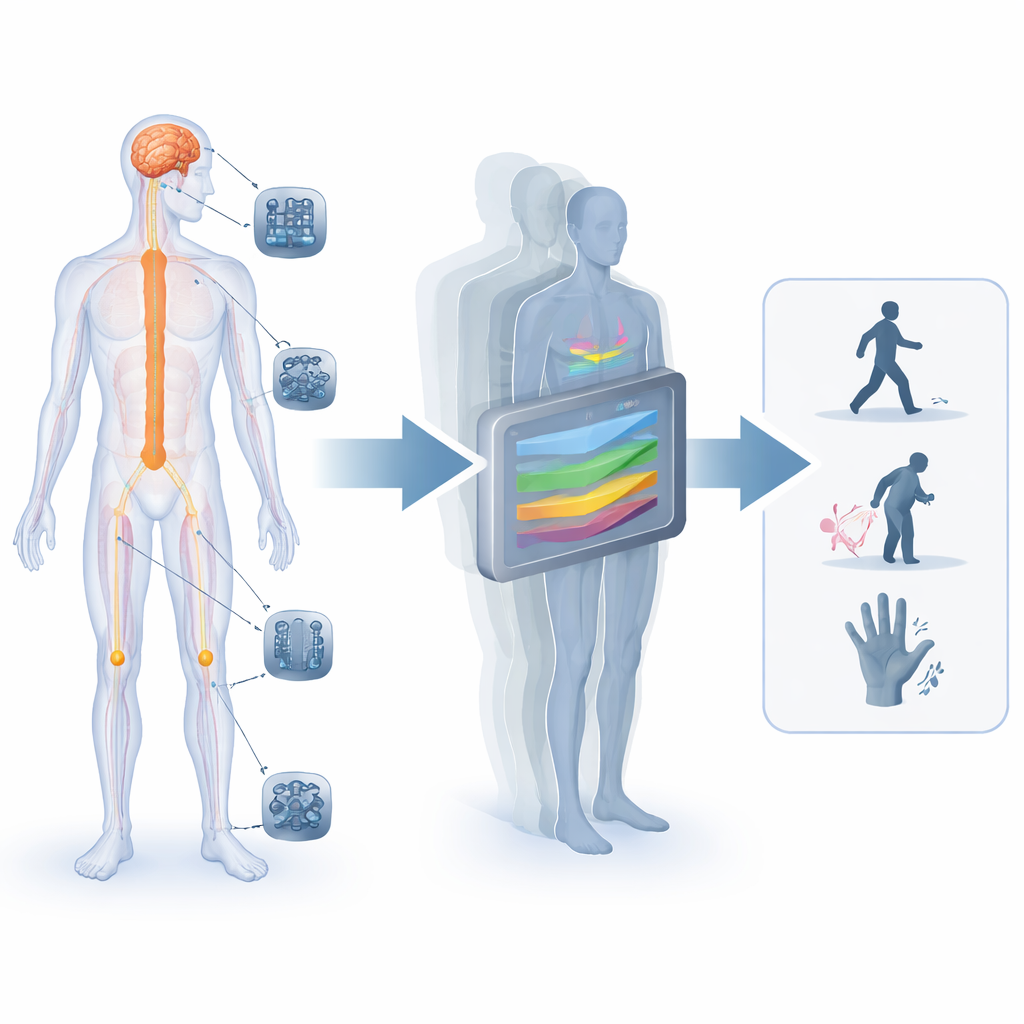
Jak elektryczność rozmawia z nerwami
Nasz układ nerwowy to elektryczna sieć komunikacyjna łącząca mózg, rdzeń kręgowy, organy i kończyny. Nowoczesne implanty sięgają do tej sieci na różne sposoby: stymulatory rdzenia kręgowego zmniejszające ból lub pomagające osobom z urazami kręgosłupa chodzić; głębokie stymulatory mózgu łagodzące objawy choroby Parkinsona; implanty siatkówki i nerwu wzrokowego przywracające część widzenia; oraz urządzenia na nerwach obwodowych przywracające dotyk lub kontrolę mięśni. Każda technologia musi znaleźć delikatną równowagę: sygnały na tyle silne, by wywołać użyteczne odczucia lub ruchy, ale nie tak silne ani źle skierowane, by powodować skutki uboczne — od chrypki przy stymulacji nerwu błędnego po nieprzyjemne mrowienie przy stymulacji rdzenia.
Budowanie wirtualnej kopii pacjenta
Ponieważ testowanie każdego projektu elektrody czy wzorca stymulacji bezpośrednio na ludziach jest niemożliwe i nieetyczne, badacze zwracają się ku szczegółowym modelom komputerowym. Te „biofizyczne cyfrowe bliźniaki” używają obrazów medycznych i danych anatomicznych do odtwarzania nerwów, rdzenia kręgowego, mózgu lub siatkówki pacjenta w trzech wymiarach. Równania oparte na prawach fizyki szacują, jak prąd elektryczny płynie przez tkanki, jak reagują poszczególne włókna nerwowe i jak ta aktywność może przełożyć się na odczucie, skurcz mięśnia lub zmianę funkcji organu. Chociaż ten sam ogólny schemat stosuje się w różnych obszarach ciała, można go dostosować, by uchwycić unikalną strukturę nerwu obwodowego, rdzenia, siatkówki czy jądra głębokiego mózgu.
Od symulacji do optymalizacji
Kiedy cyfrowy bliźniak potrafi przewidzieć, jak nerwy reagują na stymulację, staje się polem doświadczalnym dla udoskonaleń. Zamiast ręcznie próbować kilku ustawień, algorytmy komputerowe mogą automatycznie przeszukiwać tysiące możliwości, dostosowując sterowalne parametry, takie jak które elektrody są aktywne, jak silne są impulsy czy jak często są podawane. Celem może być obejęcie jak największej liczby korzystnych włókien przy unikaniu tych, które wywołują ból lub niepożądane ruchy, albo ukształtowanie pola elektrycznego ściśle skupionego na docelowym obszarze mózgu. W niektórych przypadkach rutyny optymalizacyjne dostrajają także ukryte aspekty samego modelu — na przykład wewnętrzne okablowanie pęczka nerwowego — tak, by przewidywane odpowiedzi zgadzały się z obserwacjami klinicznymi.
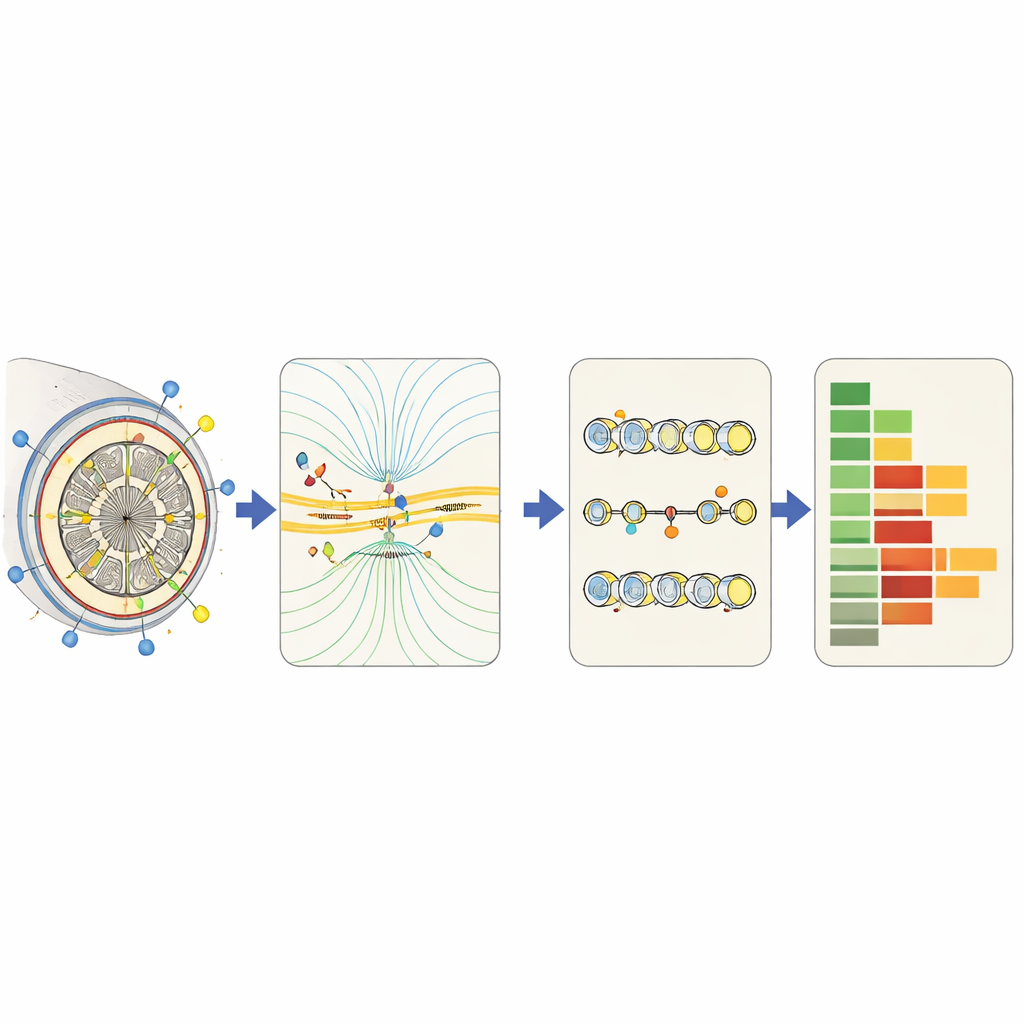
Uczynienie ciężkich obliczeń wystarczająco szybkimi
Bardzo szczegółowe symulacje mogą być wolne, zwłaszcza gdy każda zmiana ustawień wymaga obliczenia pól elektrycznych i wyładowań tysięcy włókien nerwowych. Aby proces był praktyczny, badacze budują modele „zastępcze”: uproszczone predyktory, które uczą się z wielu pełnych symulacji, jak wzorce pola elektrycznego odnoszą się do aktywności nerwowej. Niektóre opierają się na uproszczonej fizyce; inne wykorzystują uczenie maszynowe do klasyfikacji, czy włókno wystrzeli, albo do oszacowania jego częstości wyładowań na podstawie zwartego zbioru cech. Podejścia o mniejszej rozdzielczości śledzą średnią aktywność w regionach tkanki lub w całym mózgu — to mniej precyzyjne, ale wystarczająco szybkie, by badać duże przestrzenie projektowe i łączyć stymulację z efektami wysokiego poziomu, takimi jak angażowanie konkretnych obwodów mózgowych.
Pozwalanie implantom uczyć się na danych
Nawet najlepszy cyfrowy bliźniak jest tylko przybliżeniem, a rzeczywiści pacjenci zmieniają się w czasie, gdy tkanki goją się, adaptują lub bliznienią. Aby nadążyć za zmianami, wiele zespołów uzupełnia metody oparte na modelu optymalizacją „opartą na danych”, która uczy się bezpośrednio z reakcji ciała. Tutaj implant testuje różne ustawienia, podczas gdy czujniki rejestrują sygnały nerwowe, aktywność mięśni, ruch, tętno lub nawet subiektywne odczucia pacjenta. Algorytmy statystyczne, takie jak optymalizacja Bayesowska, proponują następny zestaw ustawień do przetestowania, godząc ostrożną eksplorację z chęcią szybkiego osiągnięcia skutecznej, komfortowej stymulacji. W przyszłości modele biofizyczne i uczące się na danych mogą być połączone: model dostarcza inteligentnych punktów startowych, a warstwa oparta na danych precyzyjnie je dopasowuje do konkretnej osoby.
Z wirtualnego laboratorium do codziennej medycyny
Artykuł konkluduje, że cyfrowe bliźniaki i ich szybsze, zastępcze odpowiedniki mogą radykalnie zmienić sposób projektowania i stosowania urządzeń neuroprotetycznych. Przewidując wyniki przed operacją, zawężając zakres bezpiecznych i obiecujących ustawień oraz nieustannie adaptując się do pacjenta, te narzędzia mogą ograniczyć zależność od testów na zwierzętach i długich, ręcznych sesji strojenia. Pozostają istotne przeszkody — zatwierdzenia regulacyjne, integracja w zatłoczonych klinikach oraz potrzeba przewidywania znaczących wyników, takich jak ruch i odczuwanie, a nie tylko aktywacja nerwów. Mimo to autorzy twierdzą, że jeśli będą rozwijane i weryfikowane w sposób przejrzysty, modelowanie obliczeniowe stanie się kluczowym partnerem klinicystów, pomagając technologiom neuroprotetycznym dostarczać bardziej niezawodne, spersonalizowane korzyści osobom żyjącym z chorobami i urazami neurologicznymi.
Cytowanie: Verardo, C., Fossati, V., Toni, L. et al. The optimization of neuroprosthetic interfaces relying on biophysical and surrogate digital twins. npj Biomed. Innov. 3, 28 (2026). https://doi.org/10.1038/s44385-026-00076-8
Słowa kluczowe: neuroprotetyka, cyfrowe bliźniaki, stymulacja nerwowa, modelowanie komputerowe, optymalizacja Bayesowska