Clear Sky Science · nl
De optimalisatie van neuroprothetische interfaces gebaseerd op biofysische en surrogate digitale tweelingen
Het lichaam herbekabelen met slimmere implantaten
Van het verlichten van chronische pijn tot het herstellen van zicht en beweging na verlamming: kleine elektrische apparaten die met onze zenuwen communiceren veranderen stilletjes de geneeskunde. Toch worden veel van deze neuroprothetische systemen vandaag de dag nog bed-side bijgesteld op basis van vallen en opstaan. Dit artikel legt uit hoe "digitale tweelingen"—computerreplica's van iemands zenuwen en hersenen—dat giswerk kunnen omzetten in een meer precieze wetenschap, waardoor implantaten veiliger, effectiever en makkelijker op het individu af te stemmen worden.
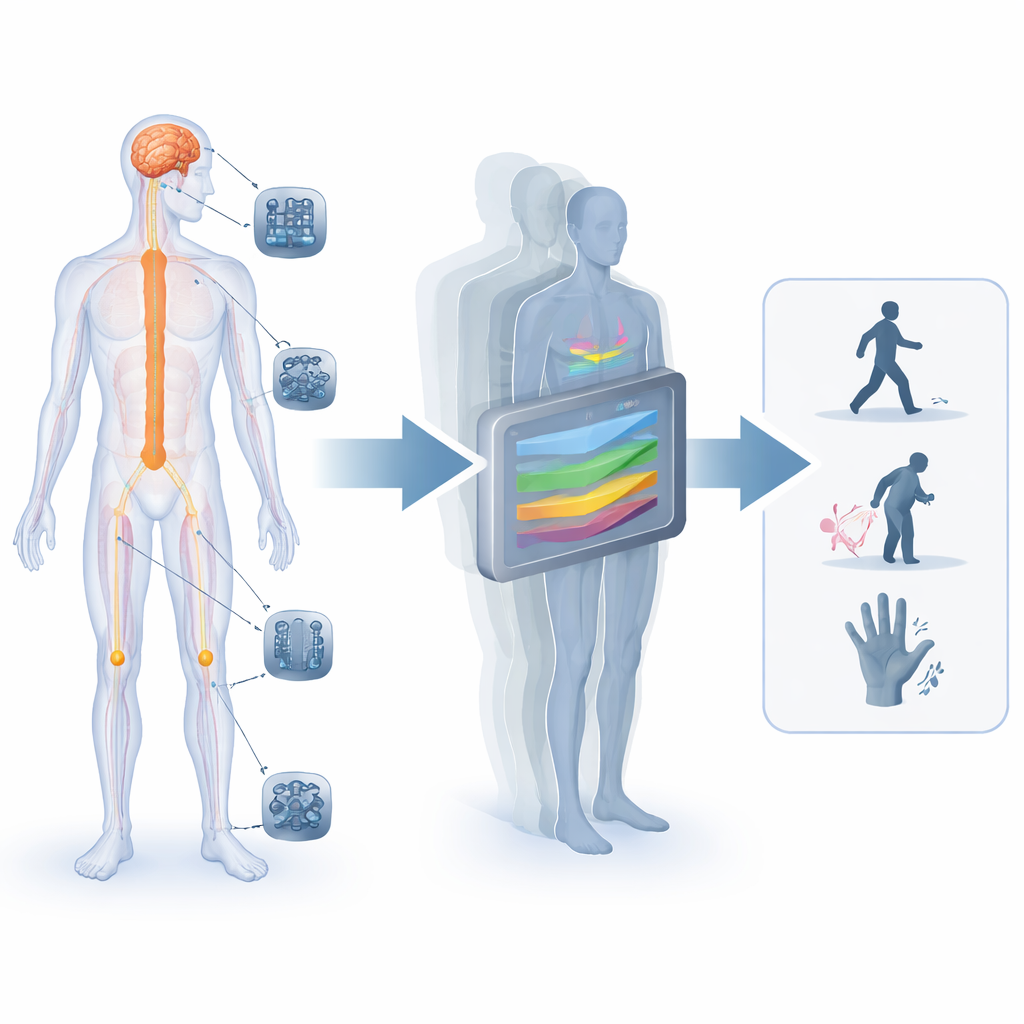
Hoe elektriciteit met zenuwen spreekt
Ons zenuwstelsel is een elektrisch communicatienetwerk dat hersenen, ruggenmerg, organen en ledematen verbindt. Moderne implantaten tappen op verschillende manieren in op dit netwerk: ruggenmergstimulatoren om pijn te verminderen of mensen met ruggenmergletsels te helpen lopen; diepe-hersenstimulatoren om de symptomen van Parkinson te verlichten; retina- en oogzenuwimplantaten om deels zicht te herstellen; en apparaten op perifere zenuwen om tast terug te geven of spieren aan te sturen. Elke technologie moet een fijne balans vinden: signalen sterk genoeg om bruikbare sensaties of bewegingen op te wekken, maar niet zo sterk of slecht gericht dat ze bijwerkingen veroorzaken, van heesheid tijdens vaguszenuwstimulatie tot onaangenaam tintelen bij wervelkolomstimulatie.
Een virtuele kopie van de patiënt bouwen
Aangezien het onmogelijk — en onethisch — is om elk elektrodeontwerp of stimulatiepatroon direct op mensen te testen, wenden onderzoekers zich tot gedetailleerde computermodellen. Deze "biofysische digitale tweelingen" gebruiken medische beelden en anatomische gegevens om de zenuwen, het ruggenmerg, de hersenen of het netvlies van de patiënt driedimensionaal te reconstrueren. Vervolgens schatten natuurkundige vergelijkingen hoe elektrische stroom door weefsel loopt, hoe individuele zenuwvezels reageren, en hoe die activiteit kan vertalen naar een sensatie, een spiercontractie of een verandering in orgaanfunctie. Hoewel hetzelfde algemene raamwerk in verschillende lichaamsregio's wordt gebruikt, kan het worden aangepast om de unieke structuren van een perifere zenuw, ruggenmerg, netvlies of diepe hersenkern vast te leggen.
Van simulatie naar optimalisatie
Zodra een digitale tweeling kan voorspellen hoe zenuwen op stimulatie reageren, wordt het een testomgeving voor verbetering. In plaats van handmatig een handvol instellingen te proberen, kunnen computeralgoritmen automatisch door duizenden mogelijkheden zoeken en bestuurbare knoppen aanpassen, zoals welke elektroden actief zijn, hoe sterk de pulsen zijn of hoe vaak ze worden toegediend. Het doel kan zijn zoveel mogelijk nuttige vezels te rekruteren terwijl diegene die pijn of ongewenste bewegingen veroorzaken worden vermeden, of een elektrisch veld te vormen dat strak gefocust is op een doelgebied in de hersenen. In sommige gevallen stemmen deze optimalisatieroutines ook verborgen aspecten van het model zelf af — zoals de interne bedrading van een zenuwbundel — zodat de voorspelde reacties overeenkomen met wat artsen in de kliniek waarnemen.
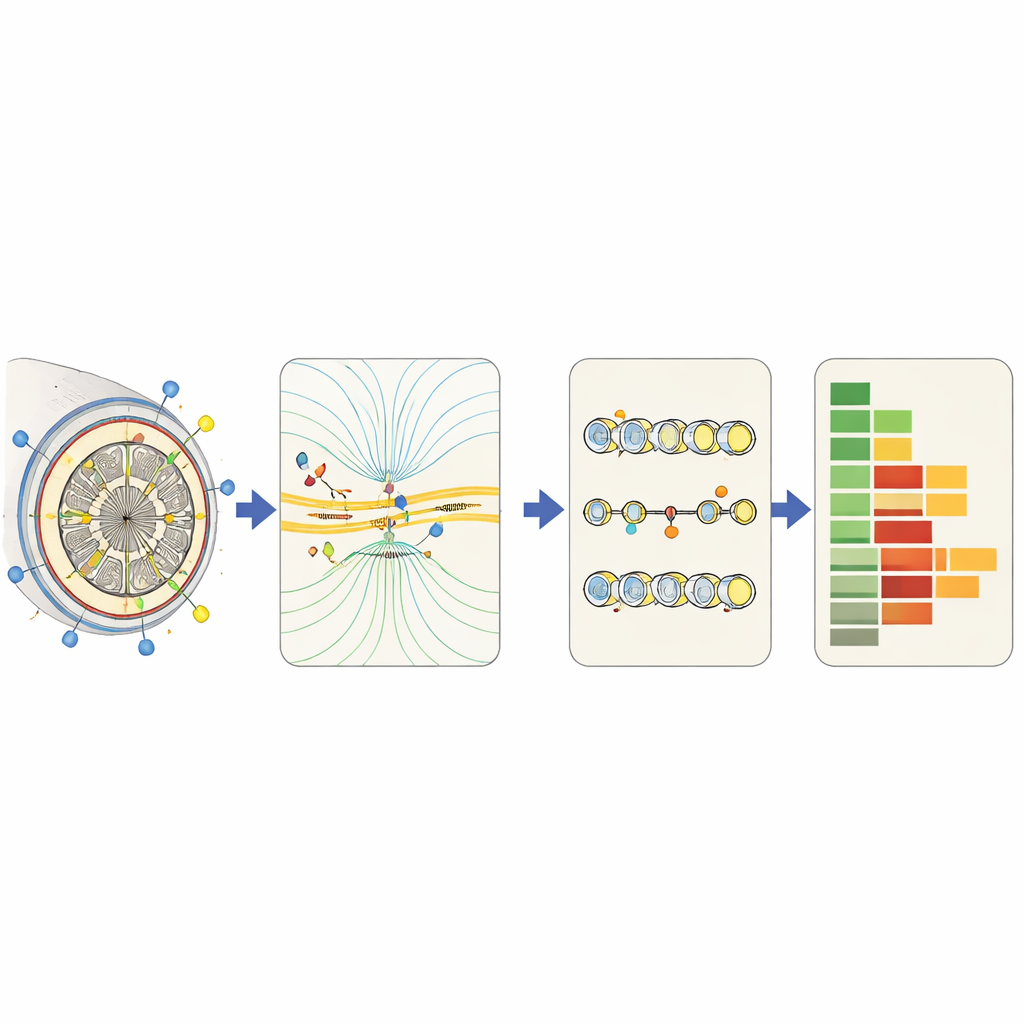
Rekenintensieve berekeningen snel genoeg maken
Zeer gedetailleerde simulaties kunnen traag zijn, vooral wanneer elke wijziging in instellingen het berekenen van elektrische velden en het vuren van duizenden zenuwvezels vereist. Om het proces praktisch te maken bouwen onderzoekers "surrogate"-modellen: gestroomlijnde voorspellers die, geleerd uit veel volledige simulaties, aangeven hoe patronen van elektrische velden samenhangen met zenuwactiviteit. Sommigen zijn gebaseerd op vereenvoudigde natuurkunde; anderen gebruiken machine learning om te classificeren of een vezel zal vuren, of om het vuurritme te schatten uit een compacte set kenmerken. Grofkorreligere benaderingen volgen gemiddelde activiteit in weefselgebieden of over de hele hersenen, wat minder precies is maar snel genoeg om grote ontwerpruimten te verkennen en stimulatie te koppelen aan hoog-niveau effecten zoals het betrekken van specifieke hersencircuits.
Implantaten laten leren van data
Zelfs de beste digitale tweeling is slechts een benadering, en echte patiënten veranderen in de loop van de tijd naarmate weefsels genezen, zich aanpassen of verkalken. Om bij te blijven vullen veel teams modelgebaseerde methoden aan met "data-gedreven" optimalisatie die rechtstreeks leert van de reacties van het lichaam. Hierbij probeert het implantaat verschillende instellingen uit terwijl sensoren zenuwsignalen, spieractiviteit, beweging, hartslag of zelfs door patiënten gerapporteerde sensaties registreren. Statistische algoritmen zoals Bayesiaanse optimalisatie doen vervolgens voorstellen voor de volgende reeks te testen instellingen, en wegen behoedzame exploratie af tegen de wens om snel effectieve, comfortabele stimulatie te bereiken. In de toekomst kunnen biofysische modellen en data-gedreven leerders worden gecombineerd, waarbij het model slimme startpunten levert en de data-gedreven laag deze verfijnt voor elk individu.
Van virtueel laboratorium naar alledaagse geneeskunde
Het artikel concludeert dat digitale tweelingen en hun snellere surrogate-verwanten de manier waarop neuroprothetische apparaten worden ontworpen en gebruikt diepgaand zouden kunnen veranderen. Door uitkomsten vóór de operatie te voorspellen, het bereik van veilige en veelbelovende instellingen te verkleinen en continu aan te passen aan de patiënt, kunnen deze hulpmiddelen de afhankelijkheid van dierproeven en langdurige handmatige afstemsessies verminderen. Belangrijke hindernissen blijven bestaan — regelgeving, integratie in drukke klinieken en de noodzaak betekenisvolle uitkomsten zoals beweging en sensatie te voorspellen in plaats van alleen zenuwactivatie. Toch betogen de auteurs dat, mits transparant ontwikkeld en gevalideerd, computationele modellering een sleutelpartner van clinici zal worden en neuroprothetische technologieën betrouwbaardere, gepersonaliseerde voordelen kan bieden aan mensen met neurologische ziekte en letsel.
Bronvermelding: Verardo, C., Fossati, V., Toni, L. et al. The optimization of neuroprosthetic interfaces relying on biophysical and surrogate digital twins. npj Biomed. Innov. 3, 28 (2026). https://doi.org/10.1038/s44385-026-00076-8
Trefwoorden: neuroprothetiek, digitale tweelingen, neurale stimulatie, computationele modellering, Bayesiaanse optimalisatie