Clear Sky Science · pl
Przebudowa błon lipidowych przez leczenie kwasem mirystynowym odwraca fenotypy α-synukleiny związane z chorobą Parkinsona w neuronach pacjentów
Dlaczego tłuszcze w mózgu mają znaczenie dla choroby Parkinsona
Choroba Parkinsona kojarzy się zwykle z drżeniem rąk i sztywnymi ruchami, ale u podstaw problemów w mózgu często leżą drobne zmiany w tłuszczach i białkach. W tym badaniu zbadano, jak określony tłuszcz dietetyczny — kwas mirystynowy, występujący w oleju kokosowym i palmowym — może przeorganizować tłuszczową zewnętrzną powłokę komórek mózgowych od osób z chorobą Parkinsona i w efekcie złagodzić zachowanie kluczowego białka związanego z chorobą, zwanego alfa-synukleiną. Wyniki sugerują, że precyzyjne dostrojenie składu tłuszczów mózgowych mogłoby w przyszłości stać się nowym sposobem zapobiegania lub spowalniania tego powszechnego schorzenia neurodegeneracyjnego.
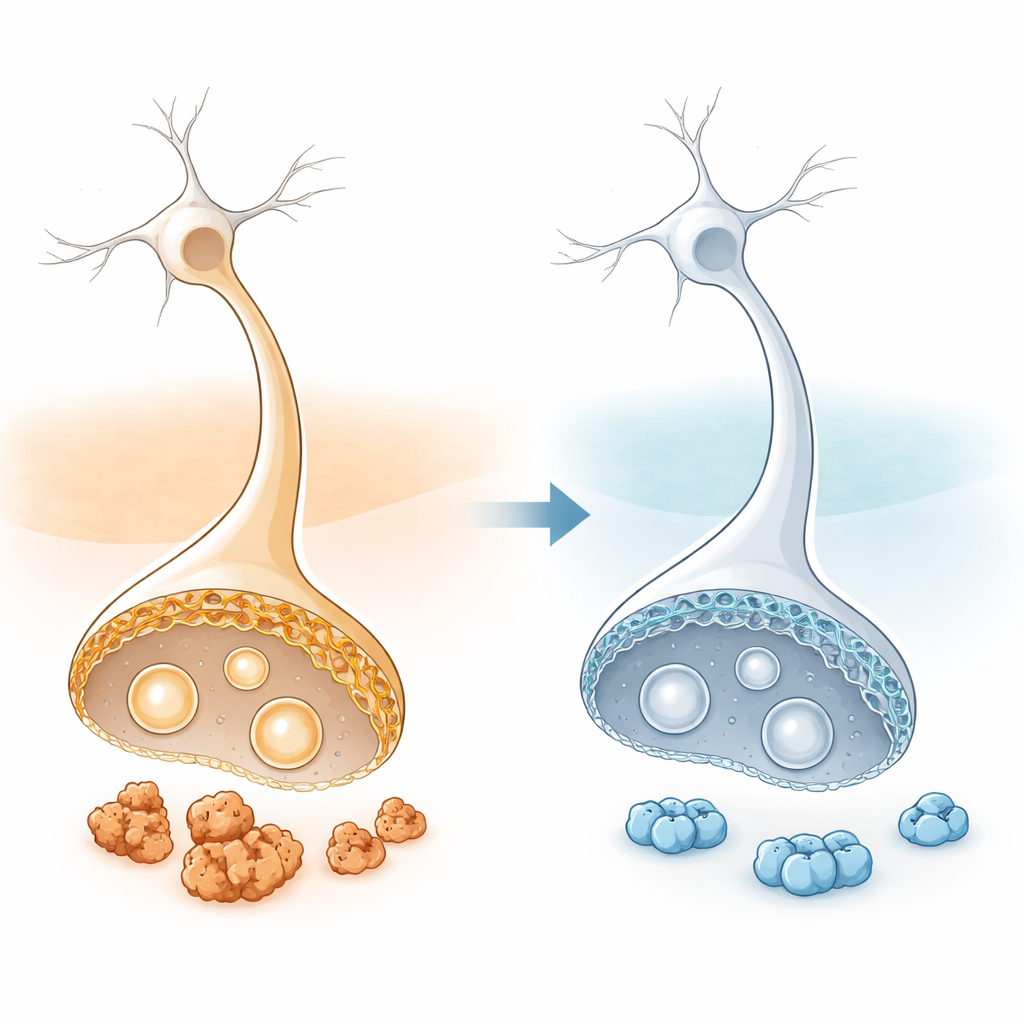
Klejące się białko spotyka zmiękczającą błonę
W chorobie Parkinsona i schorzeniach pokrewnych alfa-synukleina, białko które normalnie pomaga neuronom zarządzać uwalnianiem sygnałów chemicznych, staje się „klejące” i tworzy skupiska zwane ciałami Lewy’ego. Skupiska te są wymieszane z fragmentami uszkodzonych tłuszczowych błon. Wcześniejsze badania wykazały, że gdy błony neuronów są bogate w długie, elastyczne, nienasycone kwasy tłuszczowe (szczególnie oleinowy), alfa-synukleina jest do nich przyciągana, zbyt długo przy nich pozostaje i ma większą skłonność do nieprawidłowego fałdowania i tworzenia grudek. W zdrowych warunkach białko krótko odwiedza niewielkie, zakrzywione fragmenty błon, wykonuje swoją funkcję, a następnie powraca do bezpieczniejszej, nieagregującej formy wewnątrz komórki.
Krótszy tłuszcz o zaskakującym efekcie
Naukowcy sprawdzili, czy dodanie krótszego, nasyconego kwasu mirystynowego (C14:0) może przywrócić równowagę w tym systemie. W ludzkich komórkach przypominających neurony, zaprojektowanych tak, by ujawniać silne cechy Parkinsona, wzrost poziomu kwasu oleinowego zwiększał liczbę okrągłych inkluzji bogatych w alfa-synukleinę i podnosił poziom chemicznego znacznika związanego z chorobą (zsfosforylowana alfa-synukleina „pSer129”). Gdy zamiast tego dodano kwas mirystynowy, te szkodliwe inkluzje zmalały, a znacznik chorobowy obniżył się — bez negatywnego wpływu na przeżywalność komórek. Co więcej, gdy oba tłuszcze były obecne jednocześnie, kwas mirystynowy przeciwdziałał negatywnemu efektowi oleinowego, przywracając tworzenie inkluzji i nieprawidłowe fosforylacje w kierunku poziomów bliższych normie.
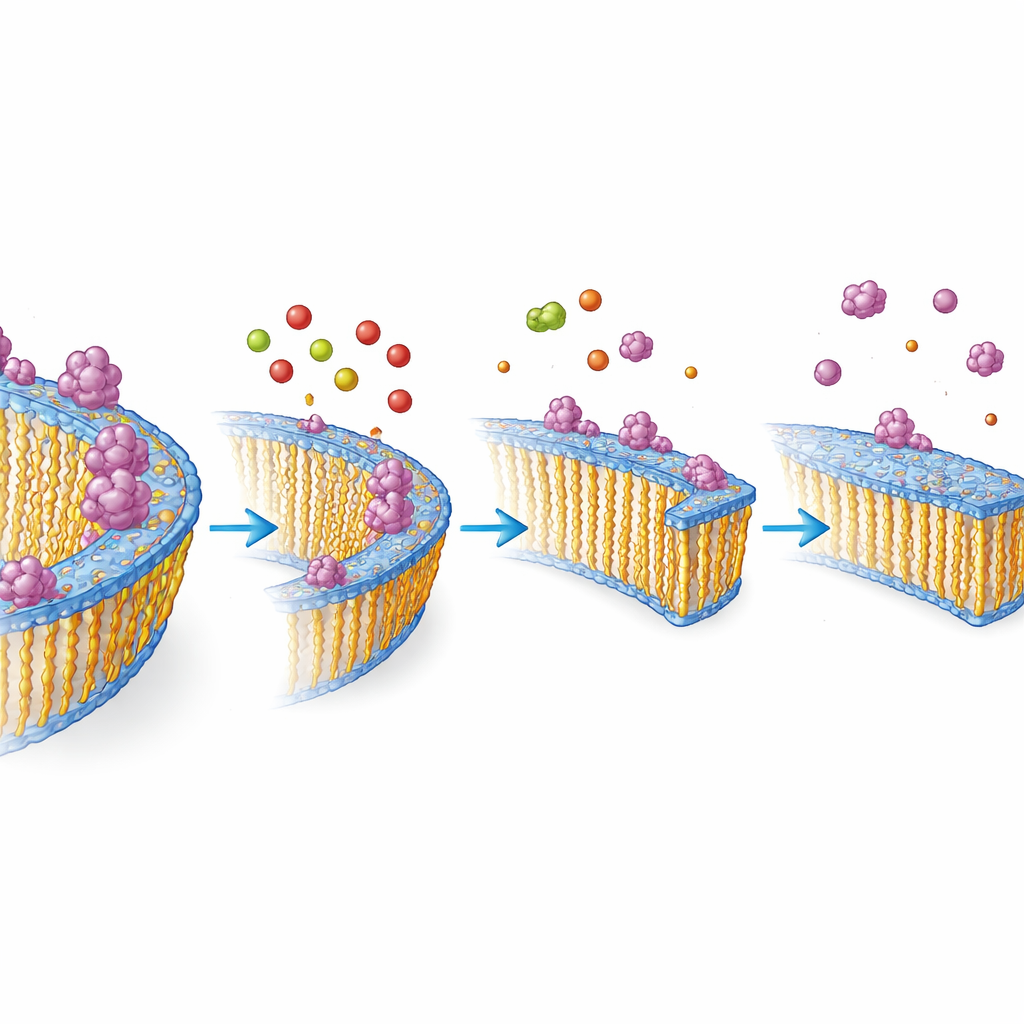
Obserwowanie interakcji białek i tłuszczów z bliska
Aby zrozumieć mechanizm na poziomie fizycznym, zespół odtworzył w laboratorium małe pęcherzyki błonowe zbudowane albo z długich nienasyconych kwasów, albo z krótszych nasyconych, albo z mieszaniny obu. Za pomocą spektroskopii jądrowego rezonansu magnetycznego zaobserwowano, że alfa-synukleina silnie wiązała się z pęcherzykami bogatymi w kwas oleinowy, a znacznie słabiej z tymi wykonanymi z kwasu mirystynowego. Gdy do błon z oleinowym dodano więcej mirystynowego, wiązanie białka spadło, a niezależne testy wykazały, że agregacja alfa-synukleiny przebiegała wolniej. Innymi słowy, skrócenie i ściślejsze upakowanie łańcuchów tłuszczowych w błonach utrzymywało więcej białka w formie rozpuszczalnej, gdzie jest ono mniej skłonne do tworzenia szkodliwych agregatów.
Resetowanie neuronów pacjentów przez przebudowę ich tłuszczów
Zespół następnie przeszedł do neuronów hodowanych z komórek pacjentów z dziedziczną postacią Parkinsona, którzy nosili dodatkowe kopie genu alfa-synukleiny i naturalnie gromadzili więcej tego białka oraz więcej lipidów bogatych w kwas oleinowy. Leczenie tych neuronów pochodzących od pacjentów kwasem mirystynowym zmniejszyło chorobowo związaną formę alfa-synukleiny fosforylowanej, przesunęło białko z powrotem z błon do wodnistego wnętrza komórki i przywróciło zdrowszą równowagę między jego normalną czterocząsteczkową (tetramerową) formą a jednołańcuchową (monomerową) formą skłonną do agregacji. Szczegółowe „odciski palców” chemiczne lipidów komórek wykazały, że kwas mirystynowy był aktywnie włączany do wielu rodzin tłuszczów, zwiększając udział krótszych, bardziej nasyconych cząsteczek w błonach i lipidach magazynujących oraz zmniejszając niektóre z nadmiernie długich i silnie nienasyconych gatunków powiązanych z chorobą.
Co to może oznaczać dla przyszłych terapii
W sumie te wyniki wspierają prostą, lecz silną ideę: subtelne przeformułowanie mieszanki tłuszczów w błonach neuronów — w szczególności zwiększenie udziału krótszych, bardziej nasyconych łańcuchów, takich jak kwas mirystynowy — może osłabić szkodliwe interakcje między alfa-synukleiną a błonami, które przyczyniają się do początku patologii Parkinsona. Choć badanie przeprowadzono na komórkach, a nie u pacjentów, i dawkowanie oraz skutki uboczne będą wymagać dokładnego przetestowania, wykazano już, że kwas mirystynowy może docierać do mózgu. To otwiera możliwość, że spersonalizowane strategie żywieniowe lub leki ukierunkowane na „przebudowę” błon mogłyby uzupełniać inne terapie, pomagając utrzymać równowagę białkową w neuronach i spowalniać postęp choroby Parkinsona.
Cytowanie: Pacheco, J.A., Sauli, G., Fonseca-Ornelas, L. et al. Lipid membrane remodeling by myristic acid treatment reverses Parkinson’s disease α-synuclein phenotypes in patient neurons. npj Metab Health Dis 4, 15 (2026). https://doi.org/10.1038/s44324-026-00110-8
Słowa kluczowe: choroba Parkinsona, alfa-synukleina, lipidy mózgowe, kwas mirystynowy, błony neuronów