Clear Sky Science · he
שיקום ממברנת שומן על ידי טיפול בחומצה מיצרית תמנע ותהפוך פנוטיפים של חלבון α‑synuclein במחלת פרקינסון בתאי עצב של מטופלים
למה שומנים במוח חשובים בפרקינסון
מחלת פרקינסון מזוהה בדרך כלל עם רעידות בידיים ותנועות קפויות, אך עמוק במוח הבעיה לעתים מתחילה בשינויים זעירים בשומנים ובחלבונים. המחקר בוחן כיצד שומן תזונתי מסוים, חומצה מיצרית—הנמצאת בקוקוס ובשמן דקל—יכול לשנות את ציפוי השומנים החיצוני של תאי מוח של אנשים עם פרקינסון ובכך להרגיע חלבון מרכזי הקשור למחלה בשם אלפא‑סינוקלאין. הממצאים מצביעים על כך שסידור מדוד של שומני המוח עשוי יום אחד להפוך לגישה חדשה למניעה או להאטה של מחלה נוירודגנרטיבית נפוצה זו.
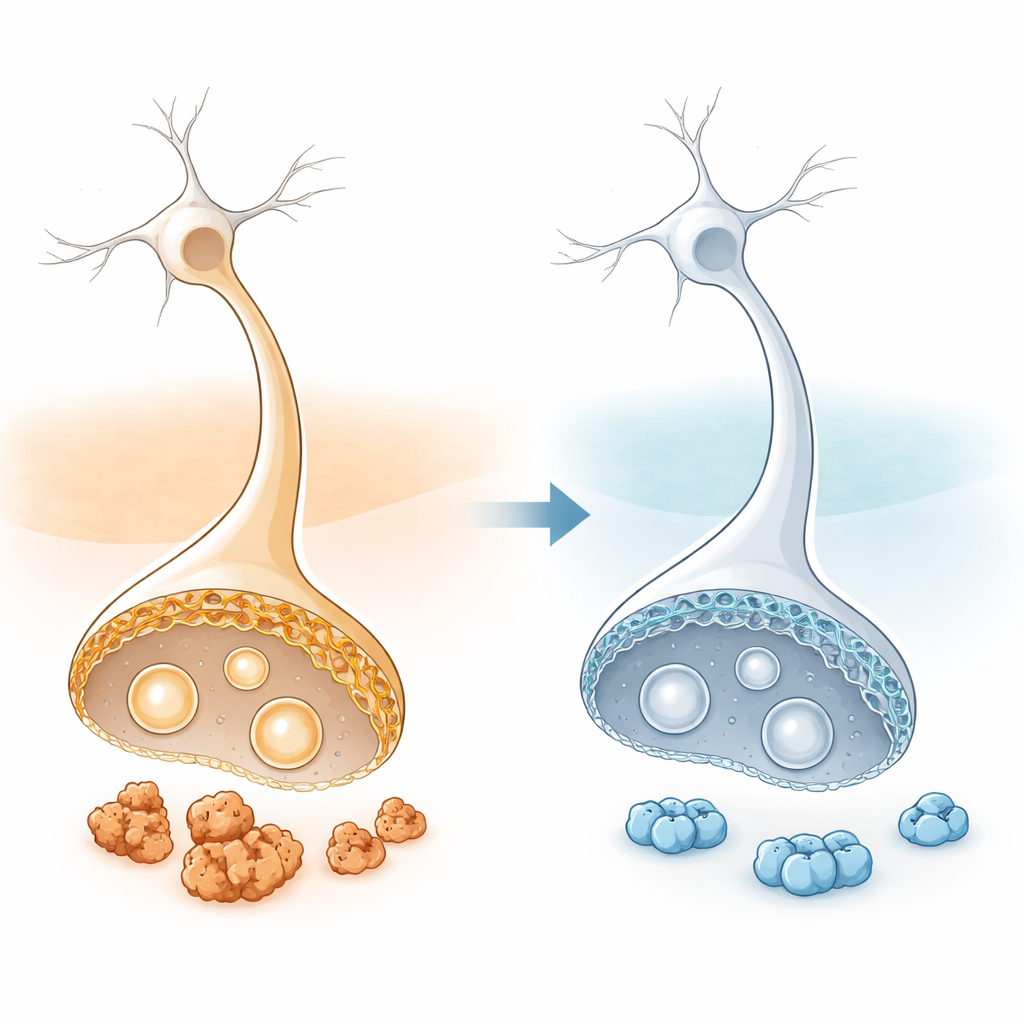
חלבון דביק פוגש ממברנה שמתרככת
בפרקינסון ומצבים קרובים, אלפא‑סינוקלאין—חלבון שמסייע בדרך כלל לתאי עצב לנהל שחרור של מוליכים כימיים—נהיה דביק ומתחיל להתגבש למבנים הידועים כגופי לווי. קונגלומרטים אלה משולבים עם שברי ממברנות שומניות. מחקרים קודמים הראו שכאשר ממברנות תאי העצב עשירות בחומצות שומן ארוכות וגמישות בלתי רוויות (במיוחד חומצה אולאית), אלפא‑סינוקלאין נמשך אליהן, נשאר שם זמן רב מדי, וסביר להניח שיתעוות ויתגבש. בתנאים בריאים החלבון מבקר לזמן קצר בממברנות מעוקלות קטנות, מבצע את תפקידו ואז חוזר לצורה הפנימית והיציבה בתא שאינה נוטה להתגבש.
חומצת שומן קצרה עם השפעה מפתיעה
החוקרים בדקו האם הוספת שומן קצר יותר, רווי, שנקרא חומצה מיצרית (C14:0) יכולה לאזן מחדש את המערכת. בתאי עצב דמו‑אנושיים המונדסים להציג תכונות פרקינסון חזקות, עלייה בחומצה האולאית הגדילה את מספר ההכללות העגולות העשירות באלפא‑סינוקלאין והגבירה סימון כימי הקשור למחלה (אלפא‑סינוקלאין מזורחן בפורמט "pSer129"). כאשר הוסיפו חומצה מיצרית במקום זאת, ההכללות המזיקות ירדו וסימון המחלה צנח—בלי לפגוע בהישרדות התאים. עוד בולט: כאשר שניהם נוכחים, חומצה מיצרית נטרלה את ההשפעה השלילית של החומצה האולאית והחזירה את היווצרות ההכללות וההזרחון החריג לכיוון רמות תקינות.
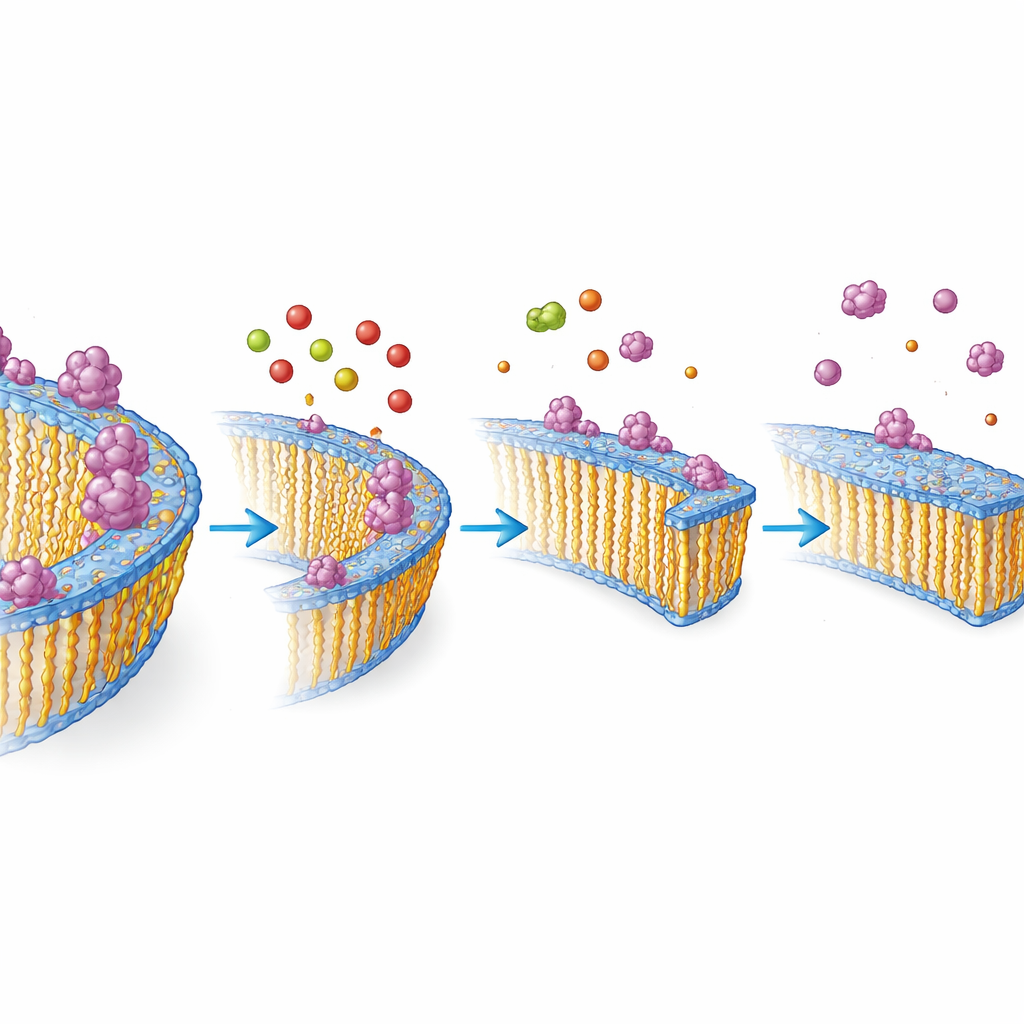
צפייה באינטראקציה בין חלבונים ושומנים מקרוב
כדי להבין את המנגנון הפיזיקלי הבסיסי, הצוות שיחזר במבחנה בועיות ממברנה זעירות שכל אחת בנויה מחומצות שומן ארוכות בלתי רוויות, מחומצות שומן קצרות רוויות, או מתערובת של השניים. בעזרת תהודה מגנטית גרעינית (NMR) הם ראו שאלפא‑סינוקלאין נקשר בחוזקה לבועיות עשירות בחומצה אולאית אך הרבה פחות לבועיות המבוססות על חומצה מיצרית. כשהוסיפו יותר חומצה מיצרית לממברנות האולאיות, הקישור של החלבון פחת, וניסויים נפרדים הראו שהתגבשות החלבון התרחשה בקצב איטי יותר. במילים אחרות, קיצור ושיפור הדחיסה של הממברנות שמרו על רוב החלבון בצורתו החופשית, שם הוא פחות נוטה ליצור אגגרגטים מזיקים.
איפוס תאי עצב של מטופלים על ידי שיקום השומנים שלהם
הצוות עבר אז לתאים עצביים שגודלו ממטופלים עם צורה תורשתית של פרקינסון שנושאים העתקים נוספים של גן אלפא‑סינוקלאין ובדרך טבעית צוברים יותר מהחלבון ושליפידים עשירים באולאית. טיפול בתאי עצב אלו בחומצה מיצרית הקטין את הצורה המזורחנת הקשורה למחלה של אלפא‑סינוקלאין, הזיז את החלבון מהממברנות חזרה לתוך החלל המימי של התא, והשיב איזון בריא יותר בין צורתו הטטרמרית הרגילה (ארבע‑חלקית) ובין הצורה המונומרית (חד‑שנקית) הנוטה להצטבר. טביעת אצבע כימית מפורטת של השומנים בתאים הראתה שחומצה מיצרית נשזרה באופן פעיל לתוך משפחות שומנים רבות, הגדילה את השפע של מולקולות קצרות ורוויות יותר בממברנות ובמאגרי השומן, והקטינה חלק מהמינים הארוכים והחריפים ברוויות שקשורים למחלה.
מה המשמעות של זה עבור טיפולים עתידיים
ביחד, הממצאים תומכים ברעיון פשוט אך חזק: על‑ידי עיצוב עדין של תערובת השומנים בממברנות תאי העצב—ובפרט באמצעות הגברת שרשרות קצרות ורוויות כמו חומצה מיצרית—ניתן להפחית את האינטראקציות המזיקות בין אלפא‑סינוקלאין לממברנות שמקודמות את פתיחת פתולוגיית הפרקינסון. המחקר נערך בתאים ולא בחולים, ודרושות בדיקות קפדניות לקביעת מינון בטוח ותופעות לוואי, אך כבר הוכח שחומצה מיצרית יכולה להגיע למוח. זה מעלה את האפשרות שאסטרטגיות תזונתיות ממוקדות או תרופתיות שמטרתן "שיקום ממברנות" עשויות להשלים טיפולים אחרים לשמירה על מאזן החלבונים בתאים ועיכוב התקדמות מחלת הפרקינסון.
ציטוט: Pacheco, J.A., Sauli, G., Fonseca-Ornelas, L. et al. Lipid membrane remodeling by myristic acid treatment reverses Parkinson’s disease α-synuclein phenotypes in patient neurons. npj Metab Health Dis 4, 15 (2026). https://doi.org/10.1038/s44324-026-00110-8
מילות מפתח: מחלת פרקינסון, אלפא‑סינוקלאין, שומנים מוחיים, חומצה מיצרית, ממברנות עצביות