Clear Sky Science · pl
Candidozyma auris — zakażone larwy Galleria mellonella: wpływ humanizowanego przeciwciała monoklonalnego Dia-T51 i jego synergii z amfoterycyną B
Dlaczego nowe narzędzie przeciw infekcjom grzybiczym ma znaczenie
Śmiertelne zakażenia grzybicze stają się narastającym problemem w szpitalach na całym świecie, zwłaszcza u pacjentów z osłabionym układem odpornościowym. Jednym z najbardziej niepokojących sprawców jest Candida auris, drożdżak oporny na wiele standardowych leków, który może szybko rozprzestrzeniać się na oddziałach intensywnej terapii. W tym badaniu analizowano nową terapię biologiczną — humanizowane przeciwciało nazwane Dia-T51 — oraz sprawdzono, czy potrafi ono chronić organizmy żywe przed C. auris i zwiększać skuteczność istniejącego leku przeciwgrzybiczego, wykorzystując larwy owada jako model zakażenia przypominający infekcję u ludzi.
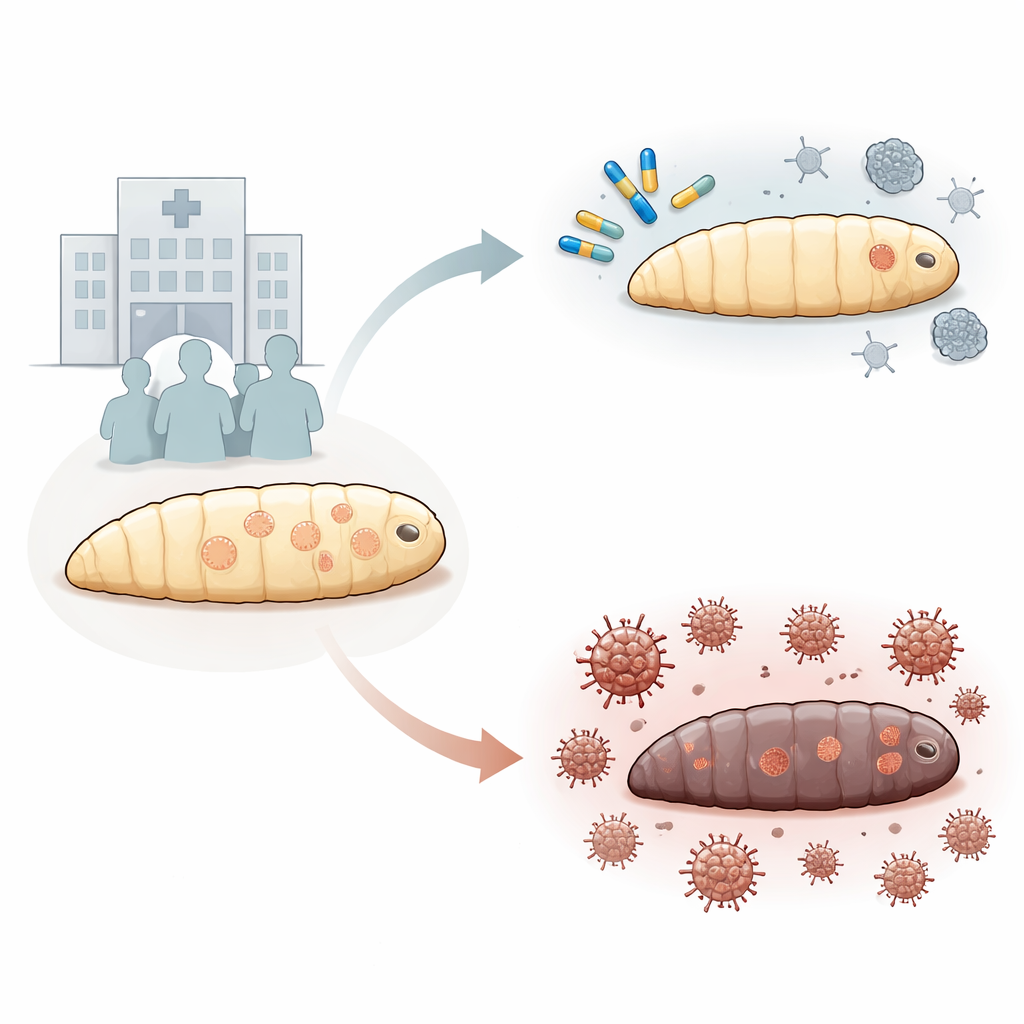
Niebezpieczny grzyb w szybkim wzroście
Candida auris szybko stała się priorytetowym globalnym zagrożeniem zdrowotnym, ponieważ jest trudna do wykrycia, ciężka do leczenia i potrafi przetrwać na powierzchniach szpitalnych. Wielu pacjentów z zakażeniami krwiobiegu wywołanymi przez ten grzyb umiera, częściowo dlatego, że organizm często wykazuje oporność jednocześnie na kilka klas leków. Jednocześnie nasz arsenał leków przeciwgrzybiczych jest ograniczony, a wysokie dawki silnych leków, takich jak amfoterycyna B, mogą uszkadzać narządy, zwłaszcza nerki. Taka sytuacja skłoniła badaczy do poszukiwania mądrzejszych terapii, które nie opierałyby się tylko na coraz większych dawkach leków.
Zaprojketowane przeciwciało z jasnym celem
Naukowcy skupili się na strukturze wspólnej dla wielu grzybów, a nieobecnej u ludzi: cukrowym elemencie budulcowym zwanym beta-1,3-glukanem, będącym częścią ściany komórkowej grzyba. Wcześniej opracowali Dia-T51 — „humanizowane” przeciwciało monoklonalne, które silnie wiąże się z tą strukturą, przyczepiając się do powierzchni grzyba bez reakcji na komórki ludzkie. Badania laboratoryjne wykazały, że Dia-T51 może spowalniać wzrost grzyba i ułatwiać komórkom odpornościowym fagocytozę C. auris. Sugerowano również, że połączenie przeciwciała z amfoterycyną B może być skuteczniejsze niż każde z tych działań osobno, lecz optymalna strategia dawkowania i rzeczywisty efekt w organizmach żywych wymagały dalszych testów.
Testy w prostym modelu żywym
Aby ocenić bezpieczeństwo i skuteczność, zespół użył larw moli woskowych Galleria mellonella, szeroko akceptowanego modelu do badań nad zakażeniami u ludzi. Larwy te mają wrodzony układ odpornościowy, który w wielu aspektach działa podobnie do naszej pierwszej linii obrony, w tym komórki pożerające drobnoustroje i reakcję pigmentacyjną związaną z zapaleniem. Najpierw naukowcy potwierdzili, że Dia-T51 i amfoterycyna B nie były toksyczne dla larw przy zastosowanych dawkach. Następnie zakażono larwy C. auris i leczono je przeciwciałem samym, lekiem samym lub oboma jednocześnie. Dia-T51 samoistnie znacząco zwiększyło przeżywalność po śmiertelnym zakażeniu i sprawdziło się szczególnie dobrze, gdy podano je przed ekspozycją na grzyba — chroniło ponad 90% larw i zapobiegało intensywnemu ściemnieniu związanemu z ciężkim zapaleniem.
Silniej razem: synergia przeciwciała i leku
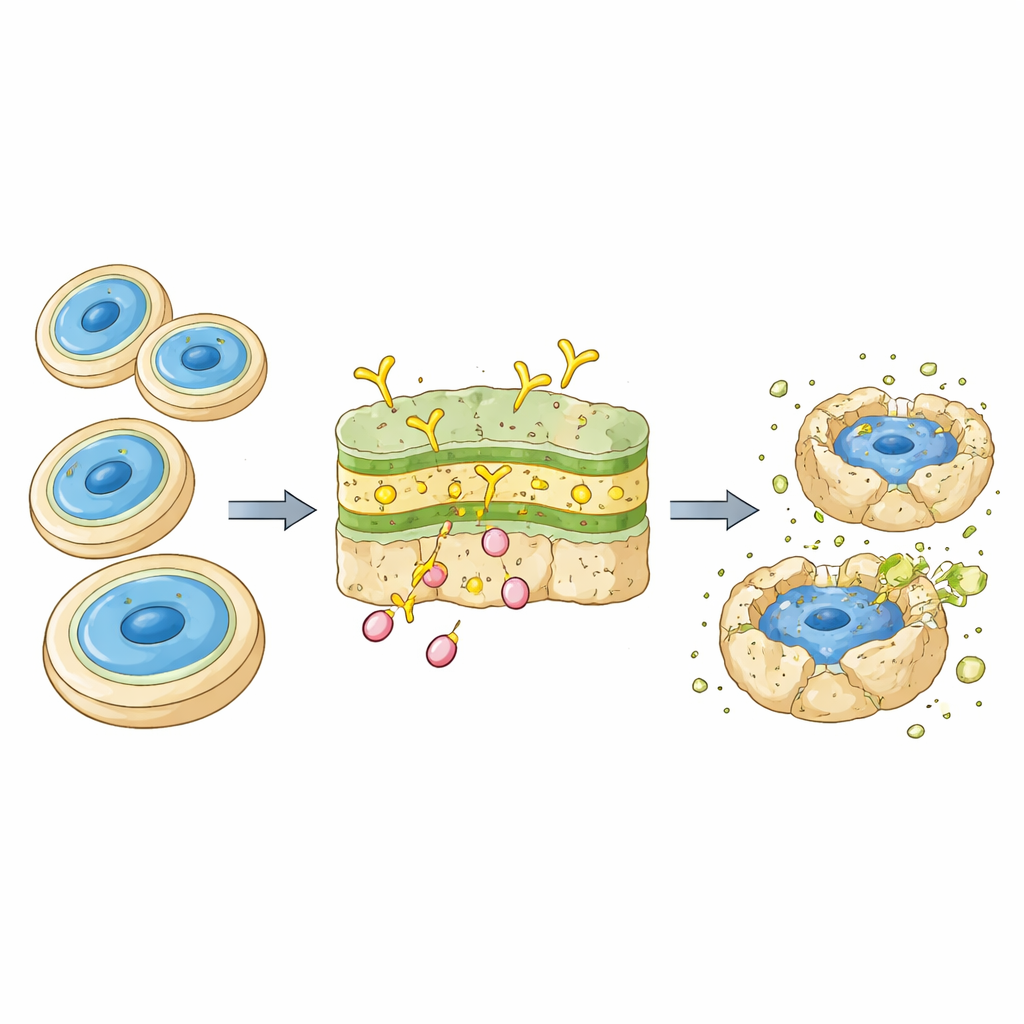
Gdy zespół zbadał kombinację Dia-T51 i amfoterycyny B, wyniki były uderzające. W eksperymentach probówkowych dodanie Dia-T51 pozwoliło osiągnąć ten sam poziom zabijania grzyba przy dawkach amfoterycyny B czterokrotnie do ośmiokrotnie niższych. U zakażonych larw dawka amfoterycyny B, która sama w sobie była nieskuteczna, nagle stała się wysoce ochronna, gdy zastosowano ją razem z Dia-T51, osiągając wskaźniki przeżycia przewyższające te obserwowane przy znacznie wyższych, potencjalnie szkodliwych dawkach leku. Pomiary komórek grzyba w hemolimfie larw pokazały, że kombinacja szybciej i skuteczniej usuwała grzyba niż każde leczenie osobno, a zapalenie ustępowało szybciej. Wyniki sugerują, że Dia-T51 pomaga odsłonić lub osłabić ścianę komórkową grzyba w sposób, który zwiększa wrażliwość na amfoterycynę B, jednocześnie modulując odpowiedź odpornościową tak, by była skuteczna, ale nie nadmiernie szkodliwa.
Co to może znaczyć dla pacjentów
Chociaż larwy owadów nie są ludźmi i nie odzwierciedlają pełnej złożoności chorób ludzkich, stanowią silny wstępny test zachowania nowych terapii w żywym organizmie. Badanie pokazuje, że Dia-T51 jest bezpieczne in vivo, może bezpośrednio chronić przed śmiertelnym zakażeniem C. auris i, co kluczowe, potrafi przekształcić niską, w przeciwnym razie nieskuteczną dawkę amfoterycyny B w potężne, długotrwałe leczenie. Dla pacjentów oznacza to perspektywę, w której przeciwciała takie jak Dia-T51 mogłyby ratować zawodzące leki przeciwgrzybicze, pozwalając klinicystom stosować niższe dawki z mniejszą liczbą skutków ubocznych, jednocześnie pokonując oporne grzyby. Jeśli potwierdzą to modele ssacze i badania kliniczne, takie partnerstwa przeciwciało–lekowe mogą stać się ważną nową linią obrony przeciw trudnym do leczenia zakażeniom grzybiczym w szpitalach.
Cytowanie: Vanzolini, T., Fiori, V. & Magnani, M. Candidozyma auris-infected Galleria mellonella larvae: the effect of the humanized monoclonal antibody Dia-T51 and its synergy with amphotericin B. npj Antimicrob Resist 4, 25 (2026). https://doi.org/10.1038/s44259-026-00198-4
Słowa kluczowe: Candida auris, oporność na leki przeciwgrzybicze, przeciwciało monoklonalne, synergia z amfoterycyną B, model Galleria mellonella