Clear Sky Science · pl
Nowa strategia cyfrowego bliźniaka do badania implikacji randomizowanych badań klinicznych dla populacji rzeczywistych
Dlaczego to ma znaczenie dla codziennych pacjentów
Kiedy lekarze czytają wyniki dużego badania klinicznego, pozostaje uciążliwe pytanie: czy te wyniki naprawdę będą miały zastosowanie do pacjentów siedzących przede mną? Badanie to przedstawia nowy sposób odpowiedzi na to pytanie, wykorzystując „cyfrowe bliźniaki” badań klinicznych — komputerowo odtworzone kopie rzeczywistych badań, które można odtwarzać w różnych populacjach pacjentów, w tym pochodzących z elektronicznych rekordów medycznych. Praca koncentruje się na badaniach dotyczących ciśnienia krwi, ale podejście to ostatecznie mogłoby pomóc dopasować dowody z prawie każdego badania do ludzi, którzy rzeczywiście zgłaszają się do klinik i szpitali.
Problem uniwersalnych badań dla wszystkich
Randomizowane badania kliniczne są złotym standardem ustalania, czy leczenie działa, ale zwykle prowadzi się je w starannie wyselekcjonowanych grupach pacjentów. Wielu codziennych pacjentów — osoby starsze, chorzy przewlekle czy osoby z niedostatecznie reprezentowanych społeczności — może nie przypominać osób, które zgłosiły się do pierwotnych badań. W rezultacie lekarze często muszą się domyślać, na ile zaufać wynikom badania w odniesieniu do swoich pacjentów. Problem ten staje się szczególnie poważny, gdy różne badania dotyczące pozornie tego samego leczenia dochodzą do sprzecznych wniosków, co pozostawia klinicystów i autorów wytycznych w niepewności co do rekomendacji.
Zagadkowy rozbieżność między dwoma badaniami nad ciśnieniem
Naukowcy skupili się na dobrze znanym dylemacie. Jedno duże badanie, SPRINT, wykazało, że agresywne obniżanie ciśnienia skurczowego (cel poniżej 120 mmHg) wyraźnie zmniejszało duże zdarzenia sercowo-naczyniowe w porównaniu z opieką standardową (cel poniżej 140 mmHg). Inne badanie, ACCORD, przetestowało tę samą agresywną strategię u osób z cukrzycą typu 2 i nie stwierdziło wyraźnej korzyści. Proponowano wiele wyjaśnień, w tym różnice w doborze uczestników i częstości występowania zdarzeń, lecz nie istniał rygorystyczny sposób na „przeniesienie” wyniku z populacji jednego badania do drugiej i sprawdzenie, czy efekt by się zmienił.
Budowanie cyfrowego bliźniaka badania
Aby to rozwiązać, zespół stworzył RCT-Twin-GAN, ramy głębokiego uczenia, które budują cyfrowego bliźniaka randomizowanego badania. Metoda wykorzystuje rodzaj modelu generatywnego, który uczy się, jak różne cechy pacjentów — takie jak wiek, funkcja nerek, tętno, wcześniejsze choroby serca i stosowanie leków — odnoszą się do siebie i do wyników badania. Wiedza kliniczna jest wbudowana poprzez skierowaną mapę zależności przyczynowo-skutkowych, która kieruje model, aby skupiał się na połączeniach mających sens medyczny i unikał przypadkowych wzorców. Po wytrenowaniu na pierwotnym badaniu model może zostać „uwarunkowany” na drugą populację: przyjmuje profil tej nowej grupy i generuje syntetyczną wersję badania tak, jakby zostało przeprowadzone w tych pacjentach, zachowując jednocześnie randomizację między ramionami leczenia i kontroli.
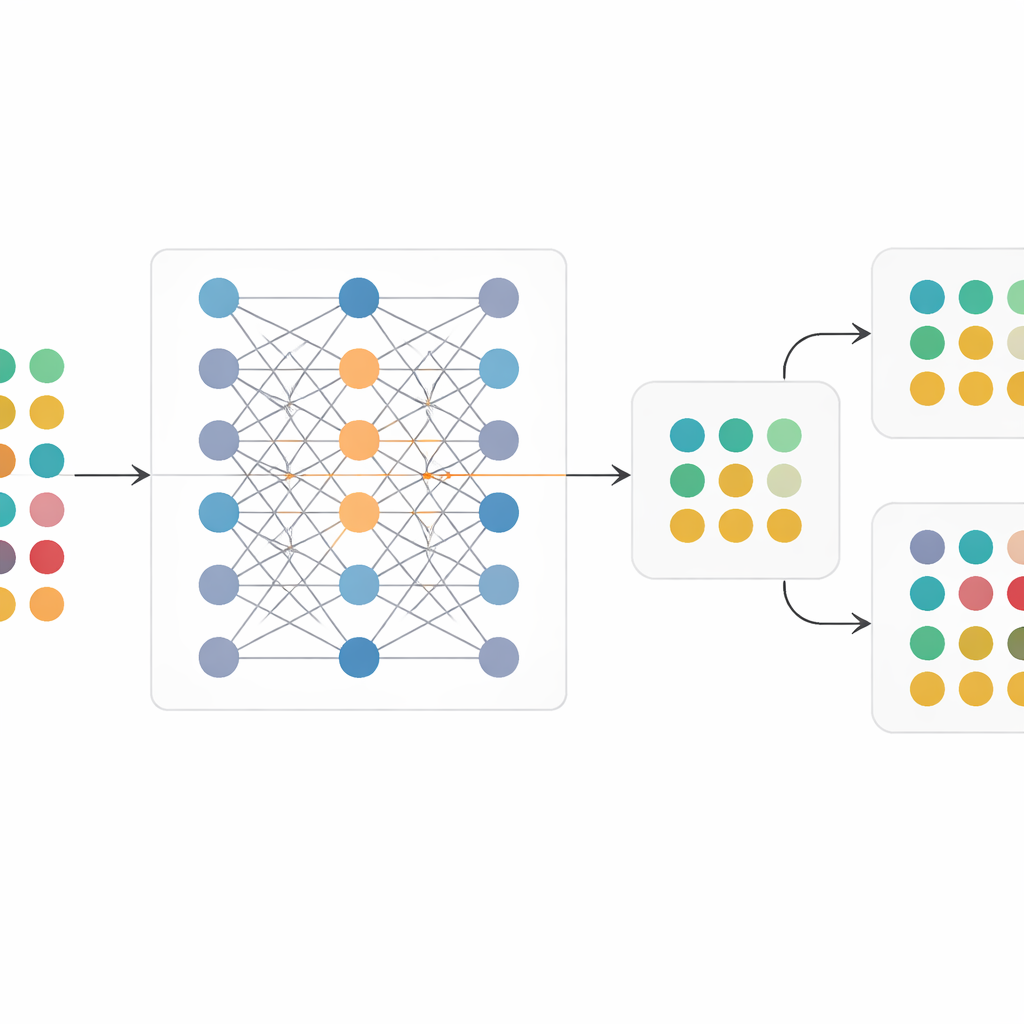
Odtwarzanie badań w nowych populacjach pacjentów
Autorzy najpierw sprawdzili, czy ich cyfrowy bliźniak wiernie odtwarza oryginalne badania SPRINT i ACCORD. Wersje syntetyczne bardzo dobrze odpowiadały rzeczywistym badaniom w cechach wyjściowych, relacjach między zmiennymi i, co istotne, w wielkości korzyści z leczenia — lub jej braku — zaobserwowanej w każdym badaniu. Następnie przeprowadzili eksperyment myślowy: wytrenowali model na SPRINT, ale uwarunkowali go na populację ACCORD, i odwrotnie. Gdy SPRINT został odtworzony w populacji ACCORD, cyfrowy bliźniak nie wykazał wyraźnej przewagi intensywnej kontroli ciśnienia, odzwierciedlając rzeczywisty wynik ACCORD. Gdy ACCORD został odtworzony w populacji podobnej do SPRINT, cyfrowy bliźniak wykazał istotną korzyść, przypominając SPRINT. Na koniec uwarunkowali model na rzeczywistych pacjentach z elektronicznych rekordów dużego systemu ochrony zdrowia, tworząc bliźniaki badań odzwierciedlające lokalne profile pacjentów i szacując, co interwencje SPRINT i ACCORD mogłyby osiągnąć w tych szerszych grupach.
Co to oznacza dla opieki i przyszłych badań
Dla laika wniosek jest taki, że sprzeczne wyniki SPRINT i ACCORD prawdopodobnie wynikają bardziej z różnic w badanych populacjach niż ze strategii obniżania ciśnienia samej w sobie. To samo leczenie może wyglądać na pomocne w jednej mieszance pacjentów, a obojętne w innej. RCT-Twin-GAN oferuje sposób ilościowego zbadania takich scenariuszy „co by było, gdyby”, bez ponownego przeprowadzania kosztownych i czasochłonnych badań. Chociaż oszacowania dla populacji z elektronicznych rekordów medycznych nie są jeszcze gotowe, by kierować indywidualną opieką, wskazują one, gdzie wyniki badań mogą, a gdzie nie muszą się uogólniać. Z czasem podejścia tego typu mogą pomóc systemom ochrony zdrowia i regulatorom przewidywać, jak nowe terapie sprawdzą się u pacjentów w rzeczywistych warunkach i projektować przyszłe badania lepiej dopasowane do ludzi, którzy najbardziej potrzebują odpowiedzi.
Cytowanie: Thangaraj, P.M., Shankar, S.V., Huang, S. et al. A novel digital twin strategy to examine the implications of randomized clinical trials for real-world populations. npj Digit. Med. 9, 329 (2026). https://doi.org/10.1038/s41746-026-02464-1
Słowa kluczowe: cyfrowe bliźniaki, badania kliniczne, ciśnienie krwi, elektroniczne rekordy medyczne, generatywna AI