Clear Sky Science · pl
Opracowanie i optymalizacja metody RP-HPLC wspomaganej projektem Box–Behnken do jednoczesnego oznaczania czterech leków przeciwwirusowych w postaciach farmaceutycznych
Dlaczego sprawdzanie leków ma znaczenie
Gdy pojawiają się nowe choroby, lekarze często sięgają po istniejące leki przeciwwirusowe, zamiast czekać kilka lat na zupełnie nowe preparaty. Zanim jednak takie leki trafiają do pacjentów, laboratoria muszą potwierdzić, że każda tabletka czy ampułka zawiera właściwą ilość substancji czynnej. W artykule opisano, jak naukowcy opracowali szybki, niezawodny i bardziej zrównoważony test laboratoryjny do pomiaru czterech ważnych leków przeciwwirusowych stosowanych w kontekście COVID-19, wszystko w jednym przebiegu.
Czterech przeciwników wirusów w jednym teście
Badanie koncentruje się na czterech lekach przeciwwirusowych: favipirawirze, sofosbuwirze, ledipaswirze i remdesiwirze. Każdy z tych leków atakuje wirusy wykorzystujące RNA jako materiał genetyczny, tak jak koronawirus wywołujący COVID-19. Ponieważ są już zatwierdzone do leczenia innych zakażeń, takich jak wirusowe zapalenie wątroby typu C czy grypa, stały się kandydatami do ponownego zastosowania w czasie pandemii. Laboratoria kontroli jakości zwykle jednak analizują każdy lek oddzielnie, co wiąże się z większym zużyciem czasu, rozpuszczalników i pracy. Badacze postawili sobie za cel opracowanie jednej metody laboratoryjnej, która dokładnie zmierzy wszystkie cztery substancje jednocześnie w rzeczywistych produktach farmaceutycznych.
Jak działa skan laboratoryjny
Zespół zastosował szeroko stosowaną technikę separacji zwaną wysokosprawną chromatografią cieczową (HPLC), którą można porównać do zaawansowanego filtra umieszczonego w kolumnie. Ciecz niosąca rozpuszczone leki przepływa przez upakowaną rurkę, a każda substancja porusza się z własną prędkością w zależności od siły oddziaływania z wypełnieniem kolumny i fazą ruchomą. Detektor zapisuje moment, w którym każda substancja opuszcza kolumnę jako oddzielny pik na wykresie. Naukowcy wybrali standardowy typ kolumny i prostą mieszaninę cieczy składającą się z buforu na bazie wody oraz acetonitrylu, powszechnego rozpuszczalnika organicznego, aby utrzymać metodę praktyczną dla rutynowych laboratoriów szpitalnych i zakładowych.
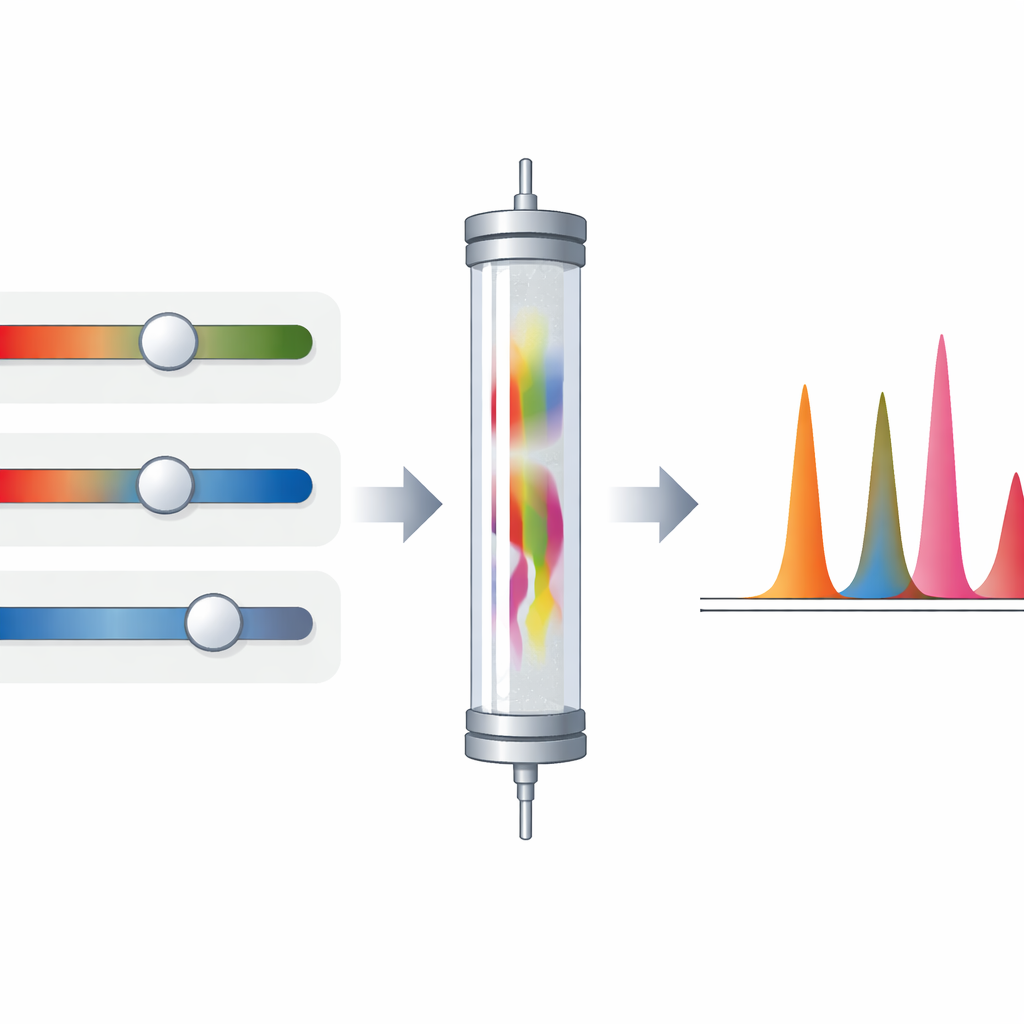
Inteligentne strojenie warunków
Zamiast regulować pojedyncze parametry metodą prób i błędów, badacze zastosowali statystyczne narzędzie planowania eksperymentu znane jako projekt Box–Behnken, będący częścią szerszej filozofii „jakość przez projektowanie”. Skupili się na trzech kluczowych regulatorach warunków wpływających na jakość rozdziału oraz czas analizy: kwasowości buforu, udziale acetonitrylu i prędkości przepływu fazy ruchomej. Przeprowadzając zaledwie piętnaście starannie dobranych eksperymentów, zbudowali równania matematyczne opisujące, jak te parametry wpływają na ostrość rozdzielenia między parami substancji oraz całkowity czas analizy. Wykresy komputerowe tych równań pomogły im ustalić warunki, które utrzymują wszystkie cztery piki dobrze rozdzielone przy zachowaniu rozsądnego czasu przebiegu.
Potwierdzenie wiarygodności i bezpieczeństwa
Po wyborze optymalnych ustawień zespół gruntownie sprawdził, czy metoda spełnia wymagania praktyczne. Wykazali, że sygnał detektora rośnie liniowo wraz ze wzrostem stężenia leku w użytecznych zakresach, że otrzymywane wartości są bardzo zbliżone do wartości rzeczywistych oraz że powtarzalne analizy dają niemal identyczne wyniki. Metoda potrafi wykryć niskie stężenia substancji i odróżnić je od innych składników w tabletkach i preparatach do wstrzykiwań. Poza wydajnością autorzy ocenili również aspekt środowiskowy i praktyczny procedury, stosując współczesne narzędzia punktowania mierzące „zieloność”, użyteczność praktyczną i ogólną jakość; wyniki wskazały na korzystne zrównoważenie dokładności, zużycia zasobów i codziennej przydatności.
Co to oznacza dla zdrowia publicznego
W istocie artykuł pokazuje, że pojedyncze, dobrze dostrojone ustawienie HPLC może niezawodnie zmierzyć cztery kluczowe leki przeciwwirusowe w produktach farmaceutycznych jednocześnie. Dla laboratoriów kontroli jakości oznacza to mniej oddzielnych analiz, mniejsze zużycie rozpuszczalników i szybsze kontrole partii leków. W szerszym kontekście przygotowań na pandemie takie uproszczone metody ułatwiają monitorowanie zapasów leków repurposed i ochronę przed produktami niskiej jakości lub podróbkami, wspierając bezpieczniejsze i bardziej efektywne opcje leczenia, gdy potrzebne są szybkie działania.
Cytowanie: Ghazy, F.H., El-Bagary, R.I., Fahim, S.H. et al. A Box–Behnken design–assisted RP-HPLC method development and optimization for simultaneous determination of four antiviral drugs in pharmaceutical dosage forms. Sci Rep 16, 14733 (2026). https://doi.org/10.1038/s41598-026-50549-4
Słowa kluczowe: leki przeciwwirusowe, HPLC, kontrola jakości leków, COVID-19, opracowanie metody