Clear Sky Science · pl
Przygotowanie nowych kowalencyjnych immobilizatorów pochodzących z gumy karaja poprzez obróbkę polietylenoiminą i glutaraldehydem
Przekształcanie gumy roślinnej w inteligentnego pomocnika enzymatycznego
Wiele osób nie trawi cukru mlecznego — laktozy, a producenci żywności poszukują łagodniejszych, bardziej ekologicznych metod usuwania jej z produktów mlecznych i strumieni takich jak serwatka. W tym badaniu pokazano, jak naturalna guma drzewna, już stosowana w żywności i lekach, może zostać przekształcona w trwałe „miejsce postojowe” dla enzymów rozkładających laktozę. Poprzez zmodyfikowanie tego materiału roślinnego tak, by enzymy silnie do niego przylegały, badacze stworzyli małe, nadające się do ponownego użycia narzędzia, które działają przez tygodnie, nawet w obecności temperatury, jonów metali i rozpuszczalników, które zwykle osłabiają białka.
Powszechny dodatek spożywczy o nowych możliwościach
Praca koncentruje się na gumie karaja, biodegradowalnym polisacharydzie pozyskiwanym z soku drzew z rodzaju Sterculia. Guma karaja jest tania, dobrze pochłania wodę i jest już używana jako środek zagęszczający w żywności, opatrunkach i systemach podawania leków. Jednak sama w sobie bywa zwykle miękka i trudna w obróbce. Aby przekształcić ją w stałe, lecz delikatne podłoże dla enzymów, badacze połączyli gumę karaja z niewielką ilością agaru, innego powszechnego żelującego środka pochodzenia morskiego. Po podgrzaniu i ostudzeniu mieszanka utworzyła zwarte dyski, które można było podnosić, myć i przetwarzać bez kruszenia.
Budowanie lepkiej, ale stabilnej platformy dla enzymów
Sam kontakt enzymów z dyskami gumowo-agarowymi nie wystarczyłby: mogłyby się wypłukać lub utracić aktywność. Zespół zastosował więc dwuetapową obróbkę chemiczną, aby przekształcić dyski w trwałe „kowalencyjne immobilizatory”. Najpierw nasączono dyski roztworem polietylenoiminy, dodatnio naładowanego, rozgałęzionego polimeru, który przylega do ujemnie naładowanych cukrów w gumie i agarze, tworząc gęste zewnętrzne powłoki bogate w grupy aminowe. Następnie pokryty materiał potraktowano glutaraldehydem, małą cząsteczką łącznikową reagującą z tymi grupami aminowymi i tworzącą liczne punkty zakotwiczenia. Gdy następnie dodano enzym, przyłączał się on do tych punktów poprzez wiele trwałych wiązań, co znacznie ograniczało jego wypłukiwanie i ruch, które mogłyby prowadzić do uszkodzeń.
Dopasowanie przepisu dla maksymalnej aktywności enzymu
Aby znaleźć optymalne warunki produkcji immobilizatora, badacze systematycznie zmieniali kwasowość (pH) i stężenie roztworu polietylenoiminy oraz ilość glutaraldehydu. Wykorzystując statystyczne podejście do projektowania eksperymentu, odkryli, że umiarkowanie zasadowy roztwór polietylenoiminy oraz relatywnie wysokie stężenia obydwu reagentów dawały najwyższą aktywność przyłączonego enzymu. Mikroskopia pokazała, że obróbka wygładziła i wzmocniła powierzchnię dysków, a spektroskopia w podczerwieni potwierdziła powstanie nowych wiązań chemicznych. W zoptymalizowanych warunkach materiał mógł wiązać znaczne ilości enzymu β-galaktozydazy, który rozkłada laktozę do prostszych cukrów — glukozy i galaktozy — przy efektywnościach immobilizacji sięgających około 70%.
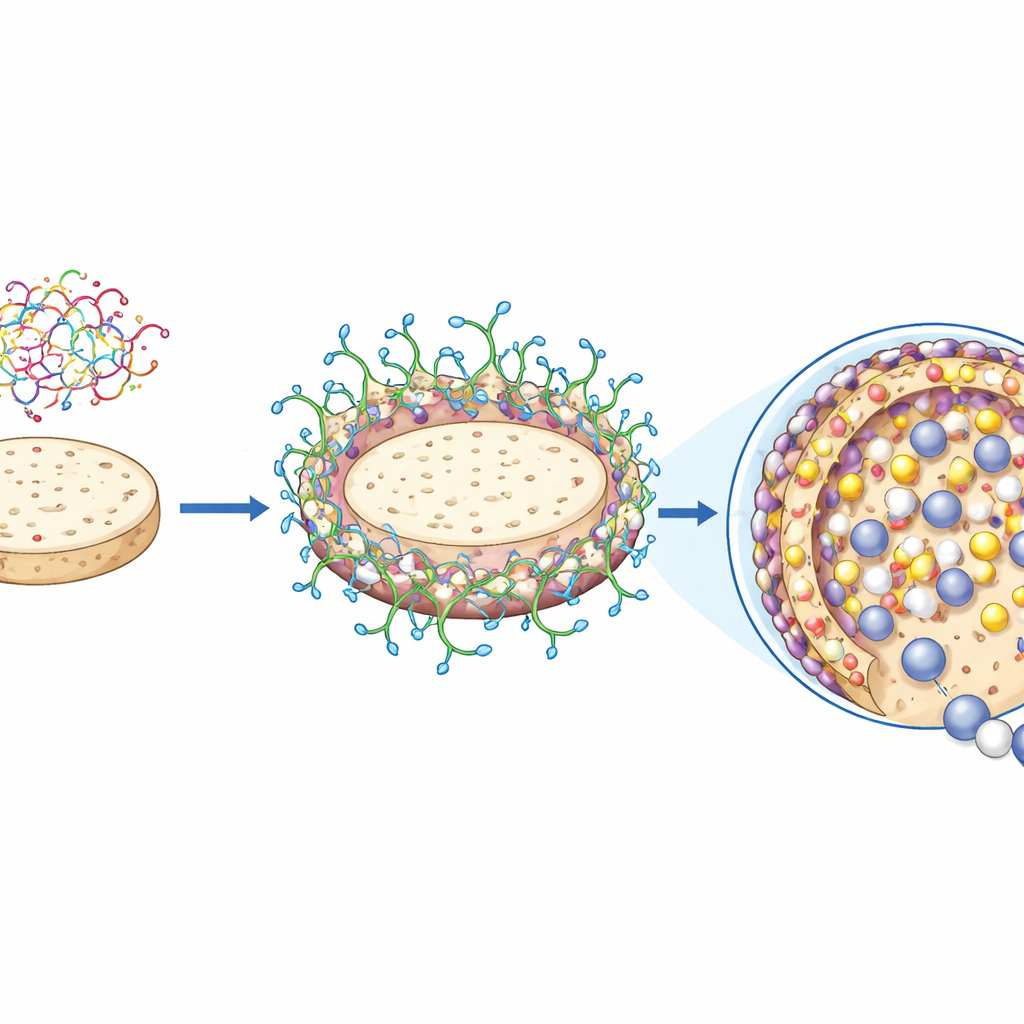
Enzymy odporne na ciepło, metale i rozpuszczalniki
Po przyłączeniu do zmodyfikowanych dysków gumowo-agarowych β-galaktozydaza zachowywała się bardziej jak wytrzymałe narzędzie przemysłowe niż delikatna cząsteczka biologiczna. Enzym immobilizowany tolerował wyższe temperatury niż forma wolna i wolniej tracił aktywność przy podwyższonych temperaturach, co objawiało się dłuższymi czasami półtrwania i większą odpornością na rozkład termiczny. Jego użyteczny zakres pH stał się szerszy i przesunął się nieco w stronę warunków bardziej kwaśnych. Co ważne, immobilizowany enzym wytrzymywał obecność jonów metali ciężkich, takich jak rtęć, glin i żelazo — zanieczyszczeń, które mogą występować w mleku i serwatce — bez istotnej utraty aktywności, podczas gdy enzym wolny był silnie hamowany. Radził sobie również znacznie lepiej w kontakcie z kilkoma rozpuszczalnikami organicznymi, częściowo dlatego, że gęsta powłoka polimerowa i uwodniony żel pomagały go chronić przed szkodliwym otoczeniem.
Od laboratoryjnych dysków do czystszych strumieni mlecznych
Dla każdego systemu immobilizacji enzymów kluczowe są długoterminowe ponowne użycie i przechowywanie. Zmodyfikowane dyski z gumy karaja i agaru zachowały ponad 90% początkowej aktywności po dziewięciu tygodniach w lodówce i wykazywały nadal około 95% aktywności po 23 powtórnych cyklach użycia, przewyższając kilka wcześniej opisywanych nośników. Zastosowane do rzeczywistej permeatu serwatkowego, ubocznego produktu przy produkcji sera, immobilizowana β-galaktozydaza rozłożyła prawie 80% laktozy w ciągu jednego dnia, wyraźnie przewyższając enzym wolny w tych samych warunkach i pozostając skuteczną przez sześć kolejnych dziennych zastosowań. Dla czytelnika niebędącego specjalistą kluczowy wniosek jest taki, że prostą, bezpieczną gumę roślinną można ulepszyć do postaci wytrzymałego, nadającego się do wielokrotnego użycia nośnika enzymatycznego, który przekształca odpadowe strumienie mleczne w produkty lepiej strawne i potencjalnie bardziej wartościowe — to obiecujący krok w kierunku bardziej zrównoważonego przetwórstwa żywności.
Cytowanie: Wahba, M.I. Preparation of novel karaya gum derived covalent immobilizers via polyethylene-imine and glutaraldehyde processing. Sci Rep 16, 12069 (2026). https://doi.org/10.1038/s41598-026-45030-1
Słowa kluczowe: guma karaja, immobilizacja enzymów, mleko bezlaktozowe, waloryzacja serwatki, hydrożele biopolimerowe