Clear Sky Science · de
Herstellung neuartiger, aus Karaya-Gummi gewonnener kovalenter Immobilisierer durch Verarbeitung mit Polyethylenimin und Glutaraldehyd
Aus Pflanzenharz wird ein intelligenter Enzymhelfer
Viele Menschen können den Milchzucker Laktose nicht verdauen, und Lebensmittelhersteller suchen nach schonenderen, ökologischeren Methoden, um ihn aus Milchströmen wie Molke zu entfernen. Diese Studie zeigt, wie ein natürlicher Baumgummi, der bereits in Lebensmitteln und Arzneimitteln verwendet wird, in einen stabilen „Parkplatz“ für Laktase-Enzyme verwandelt werden kann. Durch das chemische Umgestalten dieses pflanzlichen Materials, sodass Enzyme fest daran haften, schufen die Forschenden winzige, wiederverwendbare Werkzeuge, die wochenlang aktiv bleiben – selbst bei Hitze, Metallionen und Lösungsmitteln, die Proteine sonst schwächen würden.
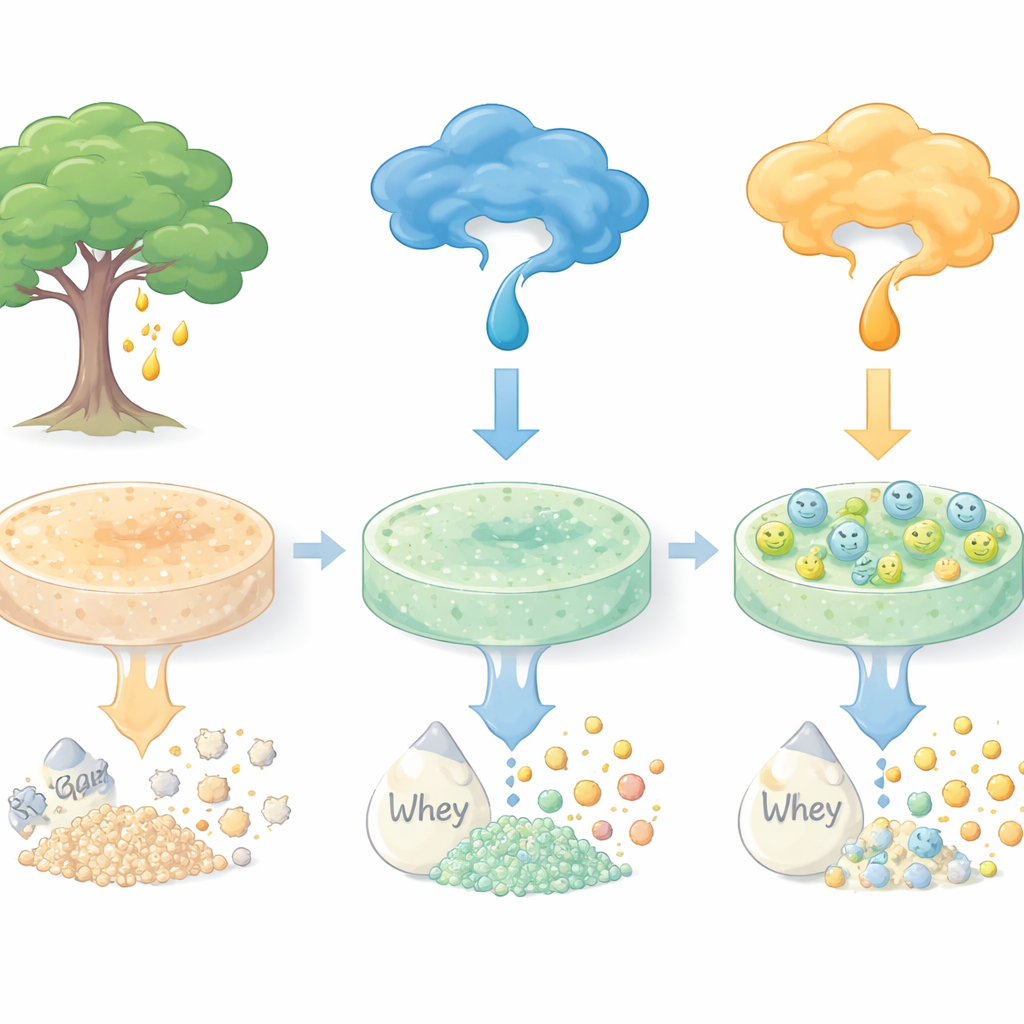
Ein verbreiteter Lebensmittelzusatzstoff mit neuen Möglichkeiten
Im Mittelpunkt der Arbeit steht Karaya-Gummi, ein biologisch abbaubares Polysaccharid, das aus dem Saft von Sterculia-Bäumen gewonnen wird. Karaya-Gummi ist preiswert, nimmt gut Wasser auf und wird bereits als Verdickungsmittel in Lebensmitteln, in Wundauflagen und in Wirkstoffabgabesystemen eingesetzt. Allerdings ist es in reiner Form meist weich und schwer zu handhaben. Um es zu einer festen, aber schonenden Trägeroberfläche für Enzyme zu machen, mischten die Forschenden Karaya-Gummi mit einer kleinen Menge Agar, einem bekannten Geliermittel aus Algen. Beim Erhitzen und anschließenden Abkühlen bildete diese Mischung feste Scheiben, die gehoben, gewaschen und weiterverarbeitet werden konnten, ohne zu zerbröseln.
Aufbau einer klebenden, aber stabilen Enzymplattform
Allein das Ablegen von Enzymen auf den Karaya–Agar-Scheiben wäre nicht ausreichend: Sie könnten weggespült werden oder Aktivität verlieren. Deshalb wandte das Team eine zweistufige chemische Behandlung an, um die Scheiben in robuste „kovalente Immobilisierer“ zu verwandeln. Zuerst tauchten sie die Scheiben in eine Lösung aus Polyethylenimin, einem positiv geladenen, verzweigten Polymer, das an die negativ geladenen Zucker des Gummis und Agars bindet und eine dichte Außenbeschichtung mit vielen Aminogruppen bildet. Anschließend behandelten sie dieses beschichtete Material mit Glutaraldehyd, einem kleinen Verbindungsstück, das mit den Aminogruppen reagiert und zahlreiche Verankerungspunkte schafft. Wenn das Enzym später zugegeben wird, bindet es an diese Punkte über mehrere permanente Bindungen, wodurch Auswaschen und Bewegungen, die zu Schäden führen können, stark reduziert werden.
Rezeptur abstimmen für maximale Enzymleistung
Um die besten Bedingungen für die Herstellung dieses Immobilisierers zu finden, variierten die Forschenden systematisch den Säuregrad (pH), die Konzentration der Polyethylenimin-Lösung und die Menge an Glutaraldehyd. Mithilfe eines statistischen Versuchsplans fanden sie heraus, dass eine mäßig alkalische Polyethylenimin-Lösung und relativ hohe Konzentrationen beider Wirkstoffe die höchste Aktivität des angelagerten Enzyms ergaben. Die Mikroskopie zeigte, dass die Behandlung die Oberfläche der Scheiben glättete und verstärkte, während die Infrarotspektroskopie bestätigte, dass neue chemische Verbindungen entstanden waren. Unter diesen optimierten Bedingungen konnte das Material erhebliche Mengen des Enzyms β-Galactosidase binden, das Laktose in die einfachen Zucker Glukose und Galaktose spaltet, mit Immobilisierungseffizienzen von nahezu 70 %.
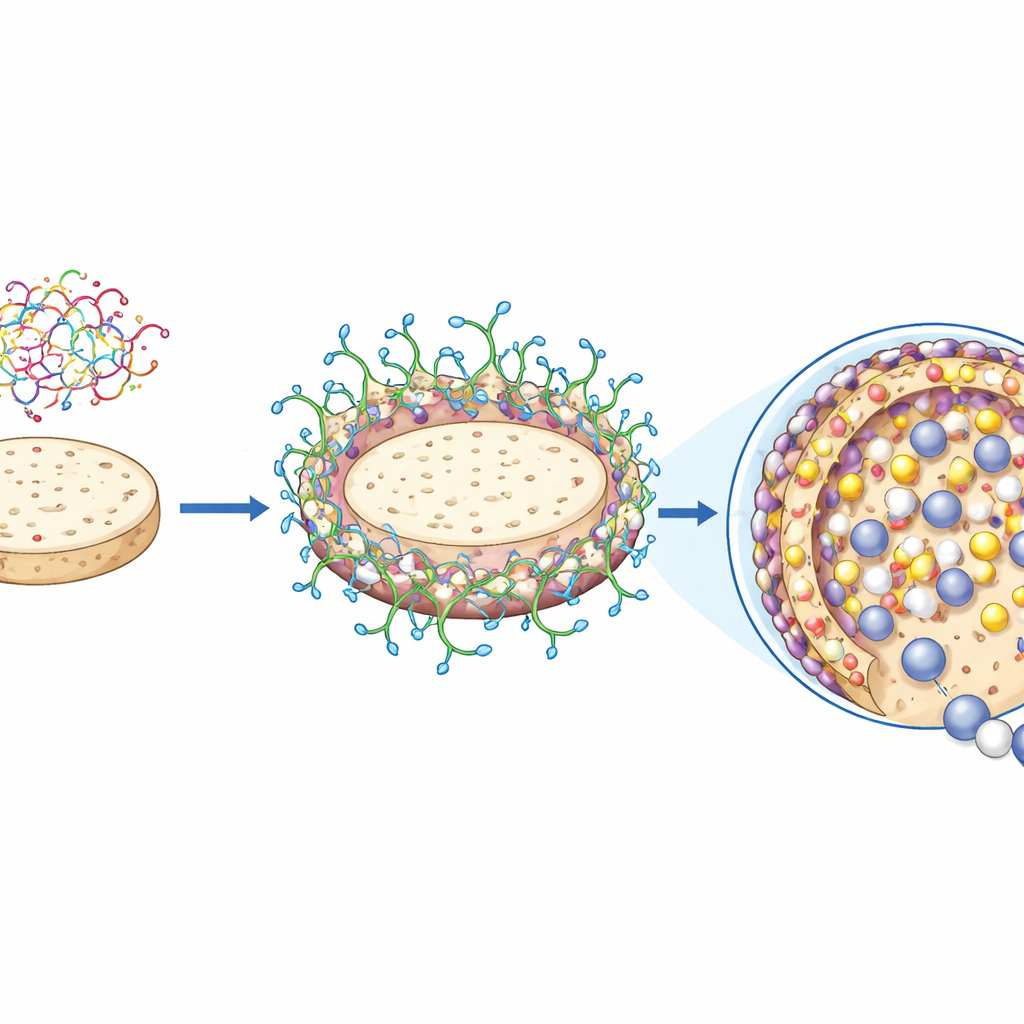
Enzyme, die Hitze, Metallen und Lösungsmitteln trotzen
Einmal an die modifizierten Karaya–Agar-Scheiben gebunden, verhielt sich die β-Galactosidase eher wie ein robustes Industriewerkzeug als wie ein empfindliches Biomolekül. Das immobilisierte Enzym tolerierte höhere Temperaturen als das freie Enzym und verlor bei erhöhter Hitze langsamer an Aktivität, wie längere Halbwertszeiten und größere Resistenz gegen thermischen Abbau zeigen. Sein nützlicher pH-Bereich wurde breiter und verschob sich leicht in Richtung saurerer Bedingungen. Wichtig ist, dass das immobilisierte Enzym schwere Metallionen wie Quecksilber, Aluminium und Eisen – Kontaminanten, die in Milch und Molke vorkommen können – ohne nennenswerten Aktivitätsverlust verkraftete, während das freie Enzym stark gehemmt wurde. Es vertrug auch den Kontakt mit mehreren organischen Lösungsmitteln deutlich besser, zum Teil weil die dicke Polymerbeschichtung und das hydratisierte Gel es vor harschen Umgebungen schützten.
Von Laborscheiben zu saubereren Milchströmen
Für jedes System mit immobilisierten Enzymen sind Langzeitwiederverwendung und Lagerung entscheidend. Die modifizierten Karaya–Agar-Scheiben behielten über 90 % ihrer Anfangsaktivität nach neun Wochen im Kühlschrank und zeigten nach 23 aufeinanderfolgenden Nutzungszyklen immer noch etwa 95 % Aktivität, womit sie mehrere zuvor berichtete Trägermaterialien übertrafen. Auf realer Molkenpermeat angewandt, baute die immobilisierte β-Galactosidase in einem einzigen Tag nahezu 80 % der Laktose ab, deutlich mehr als das freie Enzym unter denselben Bedingungen, und blieb über sechs aufeinanderfolgende Tagesläufe wirksam. Für Nichtfachleute lautet die Kernbotschaft: Ein einfacher, sicherer Pflanzenkaugummi lässt sich zu einem robusten, wiederverwendbaren Enzymträger aufwerten, der Abfallmilchströme in besser verdauliche und potenziell wertvollere Produkte verwandelt und einen vielversprechenden Schritt zu nachhaltigeren Lebensmittelverarbeitungen darstellt.
Zitation: Wahba, M.I. Preparation of novel karaya gum derived covalent immobilizers via polyethylene-imine and glutaraldehyde processing. Sci Rep 16, 12069 (2026). https://doi.org/10.1038/s41598-026-45030-1
Schlüsselwörter: Karaya-Gummi, Enzymimmobilisierung, laktosefreie Milchprodukte, Molkenverwertung, Biopolymer-Hydrogele