Clear Sky Science · pl
Klonidyna chroni neurony hipokampa i kory szczura przed uszkodzeniem wywołanym niedoborem tlenu i glukozy oraz reutlenowaniem poprzez kanały HCN
Dlaczego ma to znaczenie dla udaru i zdrowia mózgu
Kiedy udar odcina dopływ krwi i glukozy do mózgu, komórki nerwowe mogą ginąć w ciągu kilku minut, pozostawiając trwałe problemy z ruchem, pamięcią lub nastrojem. Lekarze mają tylko krótki czas na przywrócenie przepływu krwi, a dostępne leki nie zabezpieczają w pełni najbardziej wrażliwych komórek mózgu. W tym badaniu sprawdzono, czy istniejący lek obniżający ciśnienie krwi i stosowany przy sedacji — klonidyna — może chronić komórki mózgu przed uszkodzeniem po zdarzeniu przypominającym udar w warunkach laboratoryjnych, i ujawniono, jak działa wewnątrz tych komórek.
Komórki mózgu pod stresem
Naukowcy wykorzystali komórki mózgowe szczura pobrane z dwóch kluczowych obszarów związanych z pamięcią i funkcjami poznawczymi: kory i hipokampu. Poddali je wyzwaniu przypominającemu udar, zwanemu niedoborem tlenu i glukozy (oxygen-glucose deprivation), które naśladuje sytuację, gdy przepływ krwi ustaje, a następnie reutlenowaniu (reoxygenation), które odpowiada ratunkowemu przywróceniu tlenu. To połączenie może dodatkowo uszkodzić komórki, podobnie jak przywrócenie przepływu krwi u pacjentów może wywołać dodatkowe uszkodzenia. Zespół mierzył, ile komórek przetrwało oraz ile enzymu związanego z uszkodzeniem wydostało się na zewnątrz, co dawało wgląd w stan zdrowia komórek przy różnych sposobach leczenia.
Lek na nadciśnienie jako osłona komórkowa
Klonidyna, najlepiej znana ze zmniejszania ciśnienia krwi i łagodzenia objawów odstawienia, aktywuje określone miejsca dokujące na komórkach nerwowych, zwane receptorami alfa2-adrenergicznymi i imidazolinowymi. W tym badaniu wstępne leczenie komórek klonidyną zwiększyło przeżywalność neuronów po urazie przypominającym udar i zmniejszyło przeciek enzymu związanego z uszkodzeniem. Inny związek, który bezpośrednio blokuje zestaw kanałów jonowych zwanych kanałami HCN, także chronił komórki, a połączenie obu substancji działało jeszcze lepiej. Kiedy badacze dodali leki blokujące główne receptory klonidyny, jej działanie ochronne osłabło, szczególnie po zablokowaniu receptora alfa2, co pokazuje, że to właśnie ten receptor jest głównym punktem wejścia dla efektu ochronnego.
Uspokajanie nadaktywnego „zamka” jonowego
Kanały HCN znajdują się w błonach komórek nerwowych i działają jak maleńkie bramki wpuszczające i wypuszczające naładowane cząstki, pomagając ustalić łatwość, z jaką komórka generuje sygnały. Po urazie przypominającym udar komórki mózgowe zwiększyły produkcję dwóch powszechnych typów kanałów HCN, HCN1 i HCN2. Ten wzrost wiąże się ze szkodliwą nadaktywnością i zwiększonym stresem wewnątrzkomórkowym. Klonidyna, lek blokujący HCN oraz oddzielny inhibitor kluczowego enzymu przekaźnikowego obniżyły poziomy HCN1 i HCN2 zarówno na poziomie genów, jak i białek. Razem te terapie zmniejszały liczbę i aktywność tych „bramek”, pomagając utrzymać stabilne właściwości elektryczne komórek i wewnętrzną chemię, zapobiegając wymknięciu się sytuacji spod kontroli.
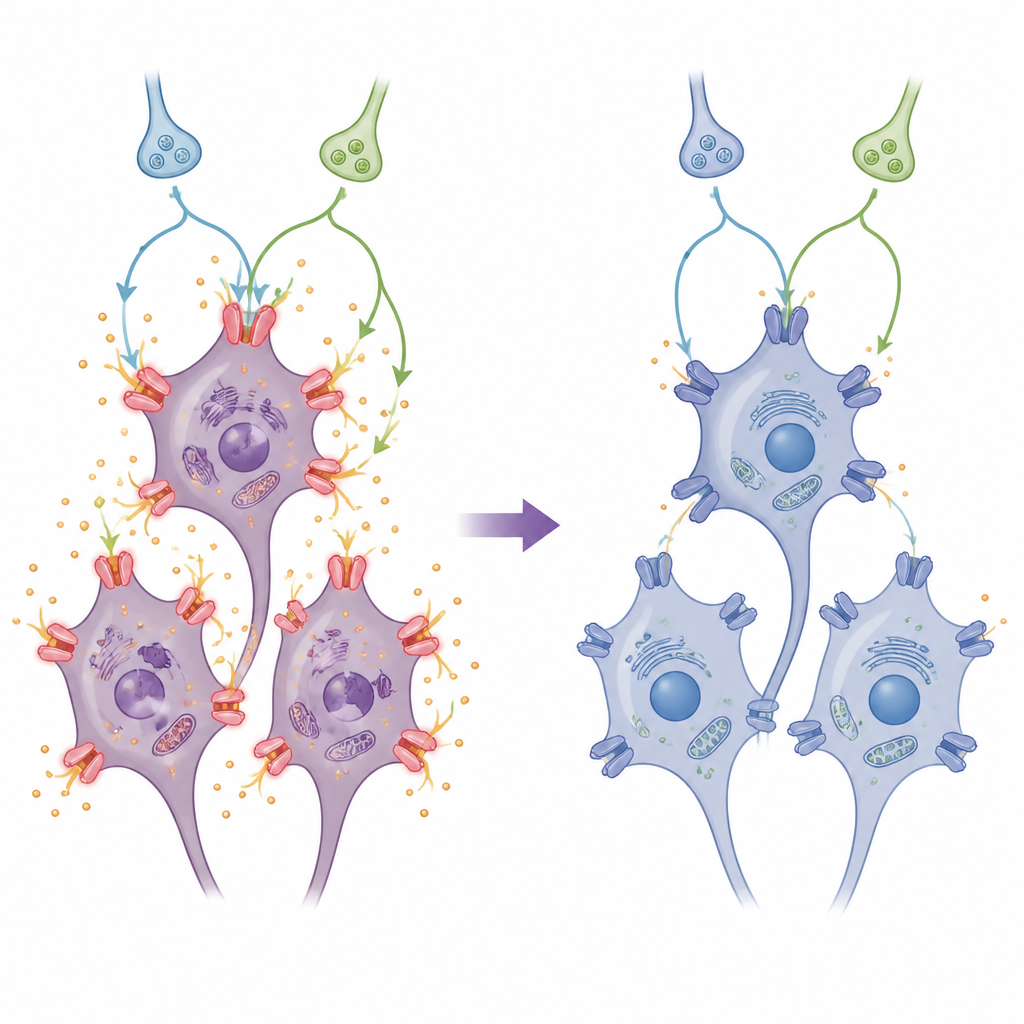
Wewnątrz komórkowych obwodów alarmowych i przetrwania
Zespół śledził także dwa ważne szlaki sygnałowe wewnątrz neuronów. Jeden szlak, często związany ze stresem, przebiega przez cząsteczki znane jako AC, cAMP i PKA. Drugi, powiązany z przetrwaniem komórki, przechodzi przez PI3K i Akt. Uraz przypominający udar podnosił poziomy kanałów HCN jednocześnie przesuwając te szlaki w niekorzystnym kierunku. Klonidyna odwracała te zmiany: tłumiła szlak AC–cAMP–PKA, który w przeciwnym razie zwiększa aktywność kanałów HCN, oraz przywracała aktywację szlaku PI3K/Akt, sprzyjającego przetrwaniu komórki. Kiedy badacze zablokowali PKA, zdolność klonidyny do wyciszania kanałów HCN się poprawiła; gdy zablokowali PI3K/Akt, działanie ochronne klonidyny osłabło, a poziomy kanałów HCN znów wzrosły. Ten wzorzec sugeruje, że klonidyna działa zarówno przez stłumienie szkodliwego obwodu alarmowego, jak i wzmocnienie obwodu ochronnego.
Co to może znaczyć dla przyszłej opieki nad udarem
Prace laboratoryjne nie pozwalają jeszcze stwierdzić, czy klonidyna uratuje tkankę mózgową u rzeczywistych pacjentów, a w badaniu zastosowano podanie leku przed urazem, a nie po nim, jak miałoby to miejsce klinicznie. Mimo to wyniki wskazują prostą narrację: klonidyna pomaga utrzymać przy życiu zestresowane komórki mózgu przez uciszenie nadaktywnych kanałów jonowych i przywrócenie równowagi kluczowych szlaków przetrwania wewnątrzkomórkowego. Powiązanie znanego leku z tymi konkretnymi przełącznikami molekularnymi wskazuje kanały HCN i powiązane z nimi szlaki sygnałowe jako obiecujące cele dla nowych terapii, które w przyszłości mogą ograniczać uszkodzenia mózgu po udarze.
Cytowanie: Wang, K., Yan, WJ., Li, G. et al. Clonidine protects rat hippocampal and cortical neurons from oxygen-glucose deprivation and reoxygenation-induced injury through HCN Channels. Sci Rep 16, 15128 (2026). https://doi.org/10.1038/s41598-026-44378-8
Słowa kluczowe: udar niedokrwienny, klonidyna, kanały HCN, ochrona neuronów, sygnalizacja komórkowa