Clear Sky Science · fr
La clonidine protège les neurones hippocampiques et corticaux de rat contre les lésions induites par la privation d’oxygène-glucose et la réoxygénation via les canaux HCN
Pourquoi cela compte pour l’AVC et la santé cérébrale
Lorsque l’AVC coupe l’apport de sang et de glucose au cerveau, les cellules nerveuses peuvent mourir en quelques minutes, entraînant des séquelles durables sur le mouvement, la mémoire ou l’humeur. Les médecins disposent d’un laps de temps limité pour rétablir la circulation, et les traitements actuels ne protègent pas complètement les cellules cérébrales vulnérables. Cette étude examine comment un médicament existant pour la pression artérielle et la sédation, la clonidine, pourrait contribuer à protéger les cellules cérébrales des dommages après un épisode de type AVC en laboratoire, et révèle comment il agit au cœur de ces cellules.
Des cellules cérébrales sous stress
Les chercheurs ont utilisé des cellules cérébrales de rat prélevées dans deux régions clés de la mémoire et du raisonnement, le cortex et l’hippocampe. Ils ont exposé ces cellules à un défi analogue à un AVC appelé privation d’oxygène-glucose, qui reproduit ce qui se passe lorsque l’apport sanguin s’arrête, suivi d’une réoxygénation, qui reproduit le sauvetage médical. Cette combinaison peut blesser davantage les cellules, tout comme la restauration du flux sanguin chez les patients peut déclencher des dommages supplémentaires. L’équipe a mesuré le nombre de cellules survivantes et la fuite d’une enzyme liée aux lésions, ce qui leur a donné une fenêtre sur la santé cellulaire selon les traitements appliqués.
Un médicament antihypertenseur comme bouclier cellulaire
La clonidine, surtout connue pour abaisser la tension artérielle et atténuer les symptômes de sevrage, active certains sites d’accrochage sur les cellules nerveuses appelés récepteurs alpha2 adrénergiques et imidazoliniques. Dans cette étude, un prétraitement des cellules par la clonidine a aidé davantage de neurones à survivre à l’agression de type AVC et a réduit la fuite de l’enzyme de dommage. Un autre composé qui bloque directement un ensemble de canaux ioniques, les canaux HCN, a également protégé les cellules, et la combinaison des deux a été encore plus efficace. Lorsque les chercheurs ont ajouté des médicaments bloquant les principaux récepteurs de la clonidine, sa protection a diminué, en particulier lorsque le récepteur alpha2 était bloqué, montrant que ce récepteur est le principal point d’entrée de son action protectrice.
Calmer des « portes » ioniques hyperactives
Les canaux HCN se trouvent dans la membrane des neurones et agissent comme de petites portes laissant passer des particules chargées, contribuant à définir la facilité avec laquelle une cellule génère des signaux. Après l’agression de type AVC, les cellules cérébrales ont augmenté la production de deux types courants de canaux HCN, HCN1 et HCN2. Cette hausse est liée à une hyperactivité nuisible et à un stress intracellulaire accru. La clonidine, le médicament bloquant les HCN et un bloqueur distinct d’une enzyme messagère clé ont tous fait redescendre les niveaux de HCN1 et HCN2, tant au niveau de l’ARN que des protéines. Ensemble, ces traitements ont réduit le nombre et l’activité de ces portes, aidant à préserver le comportement électrique des cellules et leur chimie interne pour éviter qu’elles ne dégénèrent.
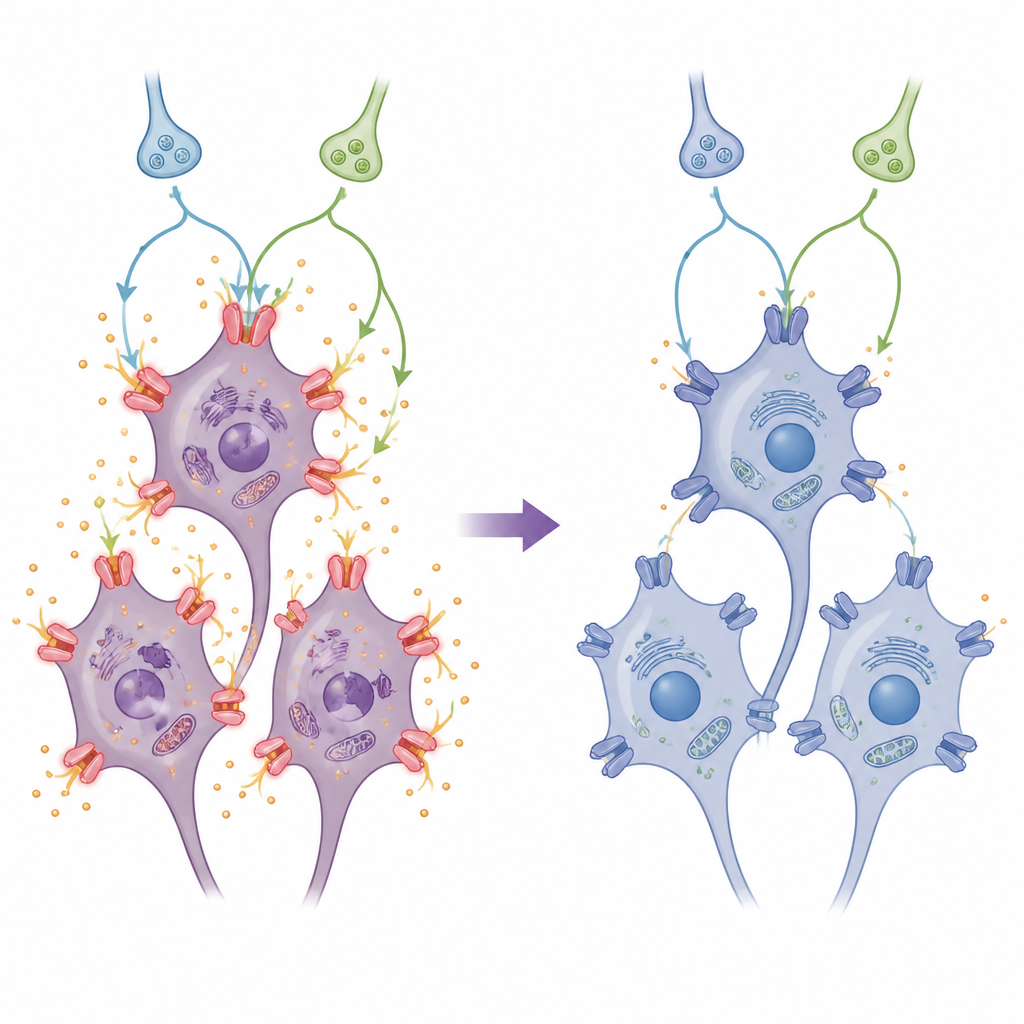
À l’intérieur des circuits d’alerte et de survie cellulaires
L’équipe a également suivi deux voies de signalisation importantes à l’intérieur des neurones. Une voie, souvent liée au stress, passe par des molécules connues sous les sigles AC, cAMP et PKA. L’autre, souvent associée à la survie cellulaire, transite par PI3K et Akt. L’agression de type AVC a augmenté les canaux HCN tout en décalant ces voies dans des directions nuisibles. La clonidine a inversé ces tendances : elle a atténué la voie AC–cAMP–PKA, qui stimule autrement l’activité des canaux HCN, et elle a restauré l’activation de la voie PI3K/Akt, favorable à la survie cellulaire. Lorsque les chercheurs ont bloqué PKA, la capacité de la clonidine à réduire les HCN s’est améliorée ; lorsqu’ils ont bloqué PI3K/Akt, la protection conférée par la clonidine a faibli et les niveaux de canaux HCN ont de nouveau augmenté. Ce schéma suggère que la clonidine agit à la fois en coupant un circuit d’alarme délétère et en renforçant un circuit protecteur.
Ce que cela pourrait signifier pour les futurs soins post-AVC
Ce travail en laboratoire ne permet pas encore de dire si la clonidine préservera le tissu cérébral chez des patients réels, et il a utilisé un prétraitement plutôt que l’administration du médicament après la lésion, comme cela se passerait en clinique. Néanmoins, les résultats dessinent une histoire claire en termes simples : la clonidine aide à maintenir en vie les cellules cérébrales stressées en calmant des portes ioniques hyperactives et en rééquilibrant des voies de survie clés à l’intérieur de la cellule. En reliant un médicament familier à ces commutateurs moléculaires spécifiques, l’étude met en avant les canaux HCN et leurs voies de signalisation associées comme des cibles prometteuses pour de nouveaux traitements susceptibles, un jour, de limiter les dommages cérébraux après un AVC.
Citation: Wang, K., Yan, WJ., Li, G. et al. Clonidine protects rat hippocampal and cortical neurons from oxygen-glucose deprivation and reoxygenation-induced injury through HCN Channels. Sci Rep 16, 15128 (2026). https://doi.org/10.1038/s41598-026-44378-8
Mots-clés: AVC ischémique, clonidine, canaux HCN, protection neuronale, signalisation cellulaire