Clear Sky Science · pl
Hamujący wpływ trzech nowo zsyntezowanych kationowych surfaktantów gemini na szybkość korozji stali węglowej w 1 M HCl
Dlaczego ochrona codziennych metali ma znaczenie
Od samochodów i mostów po rurociągi naftowe głęboko pod ziemią — stal węglowa jest jednym z filarów współczesnego życia. Jednak w agresywnych, kwaśnych warunkach metal ten może się powoli rozpuszczać, powodując wycieki, awarie i kosztowne naprawy. Opisane tutaj badanie bada nową rodzinę związków przypominających detergenty, które mogą pokrywać stal i znacznie spowalniać to ukryte niszczenie, oferując bardziej inteligentny sposób wydłużenia żywotności krytycznej infrastruktury.
Nowi dwugłowi pomocnicy dla stali
Naukowcy zaprojektowali i otrzymali trzy blisko spokrewnione surfaktanty „gemini” — cząsteczki przypominające dwie połączone główki mydlane z długimi oleistymi ogonami. Te dwugłowe cząsteczki niosą ładunki dodatnie i zostały dostosowane z różną długością łańcuchów ogonowych, aby sprawdzić, jak struktura wpływa na działanie. Przy użyciu ustalonych etapów syntetycznych najpierw zbudowano szkielet zawierający jednostki bogate w azot, a następnie dołączono węglowodorowe ogony zawierające odpowiednio osiem, dwanaście lub szesnaście atomów węgla. Techniki laboratoryjne, takie jak spektroskopia w podczerwieni i magnetyczny rezonans jądrowy, potwierdziły, że zamierzone struktury zostały zsyntezowane z wysoką czystością.
Jak te cząsteczki zachowują się w wodzie
Podobnie jak domowe detergenty, nowe surfaktanty przemieszczają się do granic faz i agregują w wodzie. Zespół zmierzył, jak silnie obniżają napięcie powierzchniowe i przy jakim stężeniu zaczynają tworzyć drobne agregaty zwane micelami. Odkryli, że wszystkie trzy związki samoistnie się grupują przy bardzo niskich stężeniach, lecz wersja z dwunastowęglowymi ogonami osiąga najlepszą równowagę: gęsto układa się na powierzchni wody, najbardziej obniża napięcie powierzchniowe i tworzy micele łatwiej niż jej krótsza odmiana. Co zaskakujące, wydłużenie ogonów do szesnastu atomów węgla utrudniło dalsze grupowanie, prawdopodobnie dlatego, że dodatkowa długość powoduje zwijanie się i wzajemne zagęszczenie cząsteczek. Pomiary te wykazały również, że zarówno adsorpcja na powierzchni, jak i tworzenie miceli zachodzą spontanicznie, napędzane korzystną zmianą energii swobodnej.
Próba tarczy na stali
Aby sprawdzić, czy to zachowanie molekularne przekłada się na rzeczywistą ochronę, naukowcy zanurzyli próbki stali węglowej w mocnym kwasie solnym, z dodatkiem i bez dodania nowych surfaktantów. Monitorowali, ile metalu się rozpuściło, ważąc próbki przed i po ekspozycji, oraz badali proces korozji za pomocą czułych pomiarów elektrycznych. We wszystkich przypadkach dodatek surfaktantów gemini zmniejszał tempo rozpuszczania stali, a wyższe stężenia zapewniały silniejszą ochronę. Wersja z dwunastowęglowymi ogonami ponownie wypadła najlepiej, redukując tempo korozji o ponad dziewięćdziesiąt procent w wielu warunkach. Badania elektryczne wykazały, że cząsteczki te spowalniają zarówno anodowe (rozpuszczanie metalu), jak i katodowe (tworzenie gazu) strony reakcji korozyjnej, działając jako inhibitory typu mieszanego, bez zasadniczej zmiany samej chemii reakcji.
Jak działa niewidzialna bariera
Uważna analiza danych ujawniła, że molekuły surfaktantów przylegają do powierzchni stali w uporządkowany, jednowarstwowy sposób, zgodny z prostą regułą pakowania znaną jako izoterma Langmuira. Obliczenia termodynamiczne i to, jak wydajność poprawia się wraz z temperaturą, sugerują, że proces ten jest w dużej mierze chemicznym wiązaniem, a nie luźnym przyczepieniem fizycznym. Dodatnio naładowane główki mogą oddziaływać z ujemnie naładowanymi gatunkami na powierzchni stali, podczas gdy jednostki bogate w azot donują elektrony do pustych orbitali atomów żelaza, wzmacniając wiązanie. Po zakotwiczeniu długie oleiste ogony odchylają się od metalu, tworząc gęstą, niechłonną wodę powłokę, która blokuje dostęp kwasowych reagentów do stali. Obrazy mikroskopowe potwierdzają ten obraz: goła stal wystawiona na działanie kwasu wygląda chropowato i nadżarta, natomiast stal traktowana nowymi surfaktantami wydaje się gładka, co wskazuje na ciągłą ochronną powłokę. 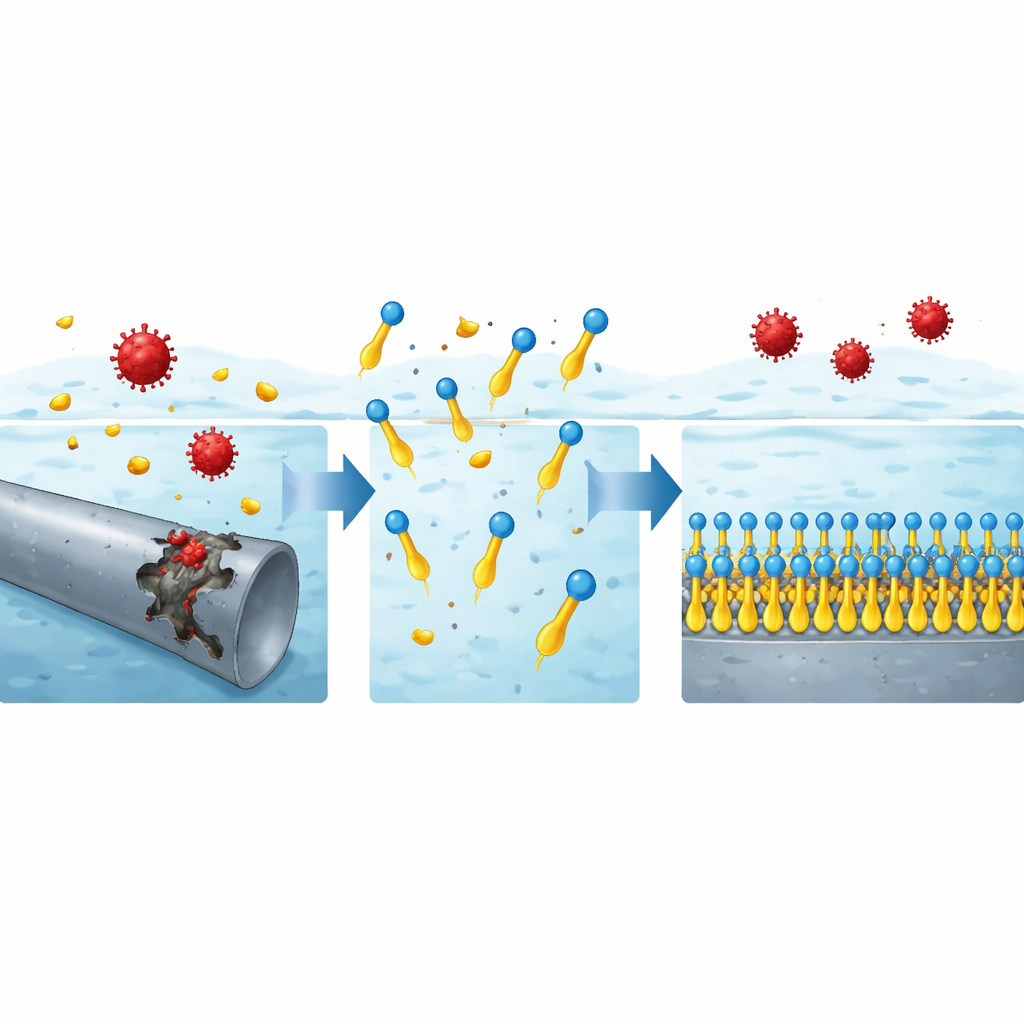
Co to oznacza dla systemów rzeczywistych
Mówiąc prosto, badanie pokazuje, że starannie zaprojektowane dwugłowe surfaktanty mogą działać jak przylegający płaszcz przeciwdeszczowy dla stali w środowisku kwaśnym, znacznie spowalniając tempo rozpuszczania metalu. Spośród trzech przebadanych wariantów cząsteczka o średniej długości ogonów oferuje najsilniejszą i najbardziej efektywną ochronę, dzięki zdolności do gęstego pakowania i mocnego wiązania z powierzchnią. Ponieważ takie inhibitory można dodać w niewielkich ilościach do istniejących kwaśnych roztworów czyszczących i procesowych, stanowią praktyczny sposób przedłużenia żywotności rurociągów, reaktorów i innego stalowego wyposażenia, jednocześnie potencjalnie redukując koszty konserwacji i wpływ na środowisko. 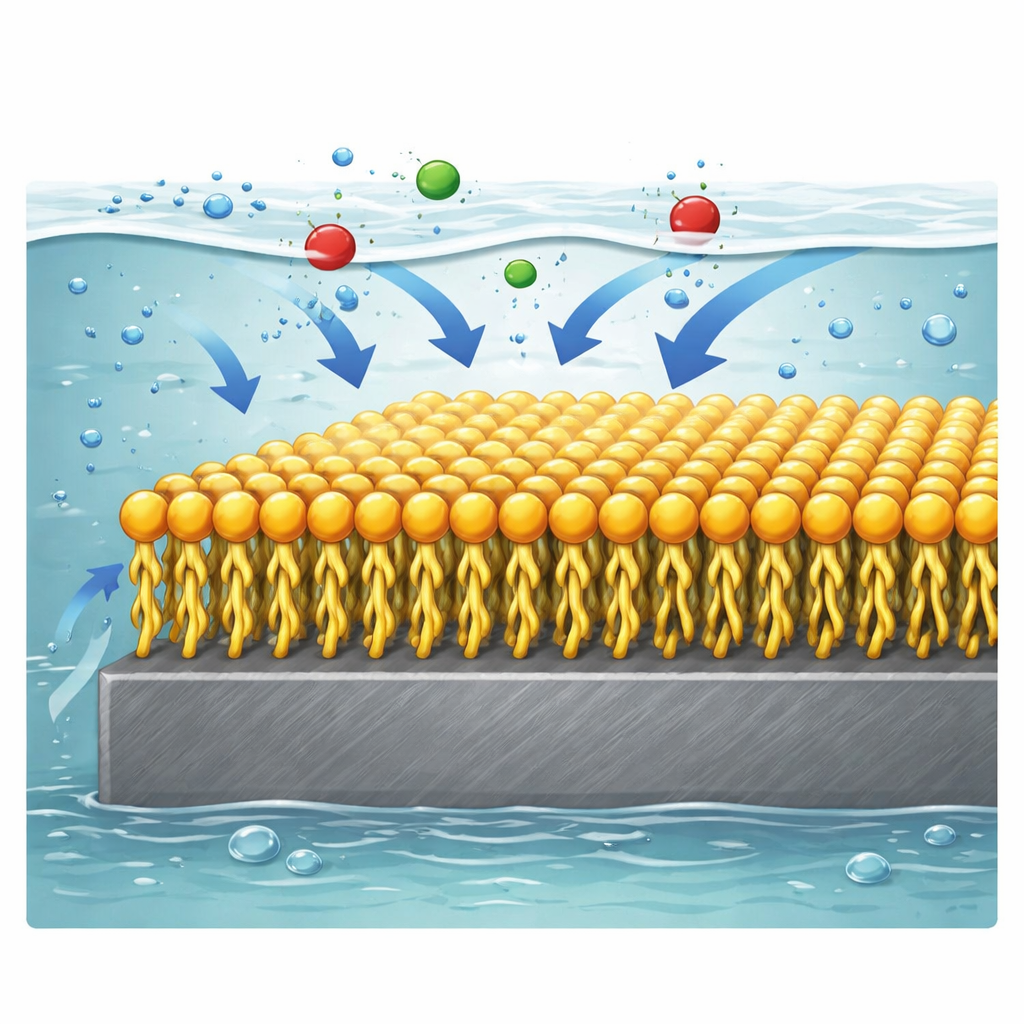
Cytowanie: Abdelhafiz, F.M., Sami, R.M., Ghiaty, E.A. et al. Inhibitory influence of three new synthesized cationic gemini surfactants on the corrosion rate of carbon steel in 1 M HCl. Sci Rep 16, 12055 (2026). https://doi.org/10.1038/s41598-026-44281-2
Słowa kluczowe: korozja stali węglowej, inhibitory korozji, surfaktanty gemini, środowiska kwaśne, ochrona powierzchni