Clear Sky Science · nl
Remmende invloed van drie nieuw gesynthetiseerde kationische gemini-oppervlakteactieve stoffen op de corrosiesnelheid van koolstofstaal in 1 M HCl
Waarom het beschermen van alledaagse metalen ertoe doet
Van auto’s en bruggen tot oliepijpleidingen diep onder de grond: koolstofstaal is een van de werkpaarden van het moderne leven. In agressieve zure omgevingen kan dit metaal echter ongemerkt wegtasten, wat leidt tot lekkages, storingen en dure reparaties. De hier beschreven studie onderzoekt een nieuwe familie van zeepachtige moleculen die staal kunnen bedekken en dit verborgen verval drastisch vertragen, en daarmee een slimmere manier bieden om de levensduur van kritieke infrastructuur te verlengen.
Nieuwe tweekoppige helpers voor staal
De onderzoekers ontwierpen en synthetiseerden drie nauw verwante “gemini” oppervlakteactieve stoffen — moleculen die eruitzien als twee verbonden zeepkoppen met lange olieachtige staarten. Deze tweekoppige moleculen dragen positieve ladingen en werden afgestemd met verschillende staartlengtes om te onderzoeken hoe structuur de prestaties beïnvloedt. Met gevestigde chemische stappen maakten ze eerst een ruggegraat met stikstofrijke eenheden en hechtten daar vervolgens koolwaterstofstaarten van acht, twaalf of zestien koolstofatomen aan. Laboratoriumtechnieken zoals infraroodspectroscopie en nucleaire magnetische resonantie bevestigden dat de beoogde structuren met hoge zuiverheid succesvol waren gesynthetiseerd.
Hoe deze moleculen zich in water gedragen
Net als huishoudelijke detergenten migreren de nieuwe oppervlakteactieve stoffen naar grensvlakken en klonteren ze samen in water. Het team mat hoe sterk ze de oppervlaktespanning verlagen en bij welke concentratie ze beginnen kleine aggregaten te vormen die micellen worden genoemd. Ze ontdekten dat alle drie verbindingen zelfassemblage vertonen bij zeer lage concentraties, maar de versie met twaalf-koolstofstaarten levert de beste balans: ze pakken zich dicht op het wateroppervlak, verlagen de oppervlaktespanning het meest en vormen gemakkelijker micellen dan hun korterstaartige verwant. Verrassend genoeg maakte het verlengen van de staarten naar zestien koolstoffen het klonteren minder gunstig, waarschijnlijk omdat de extra lengte de moleculen doet oprollen en elkaar belemmert. Deze metingen toonden ook aan dat zowel oppervlakteadsorptie als micelvorming spontaan plaatsvinden, gedreven door een gunstige verandering in vrije energie.
De bescherming op staal in de praktijk testen
Om te zien of dit moleculaire gedrag zich vertaalt naar echte bescherming, dompelden de wetenschappers koolstofstaalmonsters onder in sterke zoutzuuroplossing, met en zonder de nieuwe oppervlakteactieve stoffen. Ze registreerden hoeveel metaal oploste door de monsters voor en na blootstelling te wegen, en onderzochten het corrosieproces met gevoelige elektrische metingen. In alle gevallen verminderde het toevoegen van de gemini-oppervlakteactieve stoffen de snelheid waarmee staal oploste, en hogere concentraties boden sterkere bescherming. De versie met twaalf koolstofatomen presteerde opnieuw het best en verlaagde de corrosiesnelheden onder veel omstandigheden met meer dan negentig procent. Elektrische tests toonden aan dat deze moleculen zowel de metaaloplossende als de gasvormende onderdelen van de corrosiereactie vertragen, en fungeren als “gemengde” remmers zonder de onderliggende chemie fundamenteel te veranderen.
Hoe de onzichtbare barrière werkt
Zorgvuldige analyse van de gegevens toonde aan dat de oppervlakteactieve moleculen zich ordenen en zich in een enkele laag aan het staaloppervlak hechten volgens een eenvoudige packingsregel die bekendstaat als het Langmuir-isotherm. Thermodynamische berekeningen en de verbetering van de prestaties bij verhoging van de temperatuur suggereren dat dit hoofdzakelijk een chemisch bindingsproces is in plaats van een losse fysieke hechting. De positief geladen koppen kunnen interactie aangaan met negatief geladen soorten aan het staaloppervlak, terwijl de stikstofrijke eenheden elektronen doneren in lege orbitalen van ijzeratomen, waardoor de binding versterkt wordt. Eenmaal verankerd steken de lange olieachtige staarten weg van het metaal en vormen een dicht, waterafstotend film die zure deeltjes tegenhoudt. Microscopische beelden ondersteunen dit beeld: onbedekt staal dat aan zuur werd blootgesteld ziet er ruw en aangetast uit, terwijl met het nieuwe oppervlakteactieve middel behandeld staal er glad uitziet, wat wijst op een continue beschermende coating. 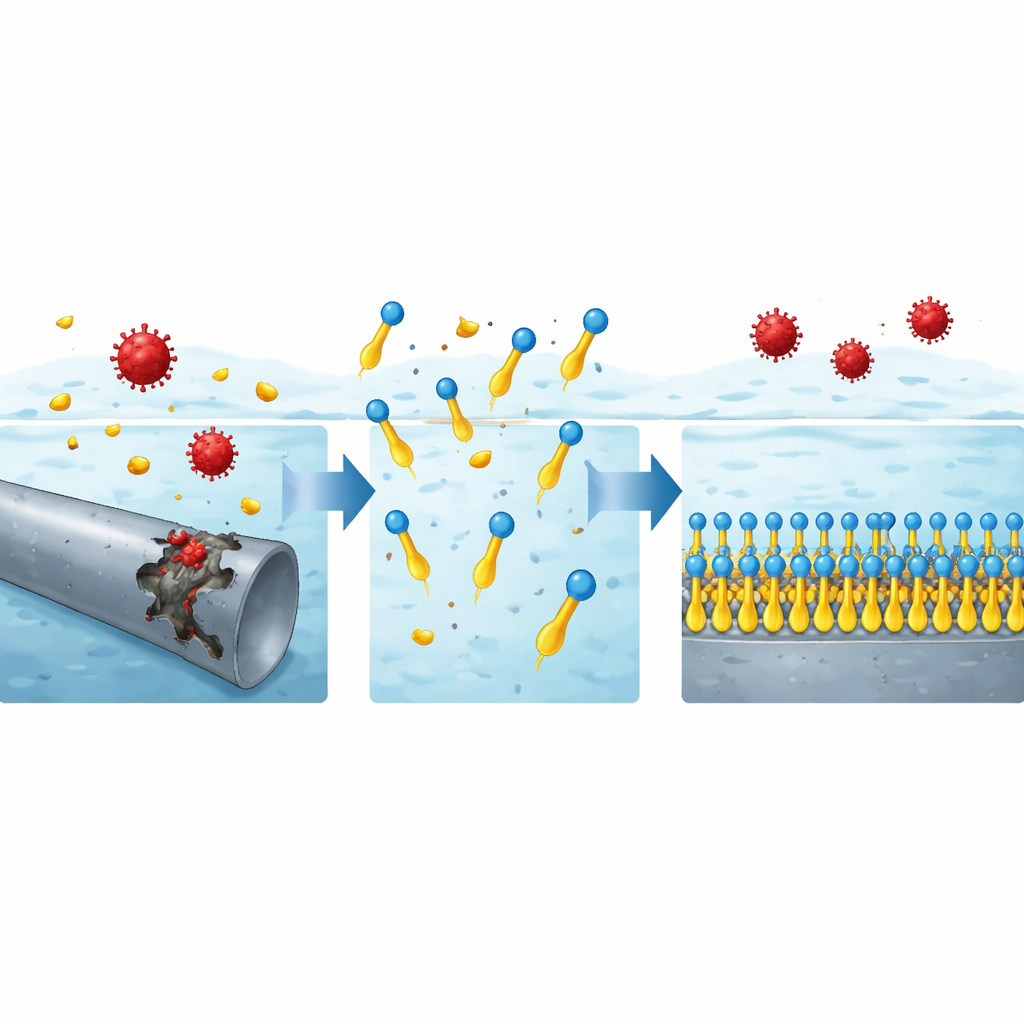
Wat dit betekent voor systemen in de praktijk
In eenvoudige bewoordingen laat de studie zien dat zorgvuldig ontworpen tweekoppige oppervlakteactieve stoffen als een aangehechte regenjas voor staal in zuur kunnen fungeren en de snelheid waarmee het metaal oplost sterk verminderen. Van de drie geteste varianten biedt het molecuul met middellange staarten de sterkste en meest efficiënte bescherming, dankzij het vermogen zich dicht te pakken en stevig aan het oppervlak te binden. Omdat dergelijke remmers in kleine hoeveelheden kunnen worden toegevoegd aan bestaande zure reinigings- en verwerkingsoplossingen, bieden ze een praktische manier om de levensduur van pijpleidingen, reactoren en andere stalen apparatuur te verlengen en tegelijkertijd onderhoudskosten en milieu-impact mogelijk te verminderen. 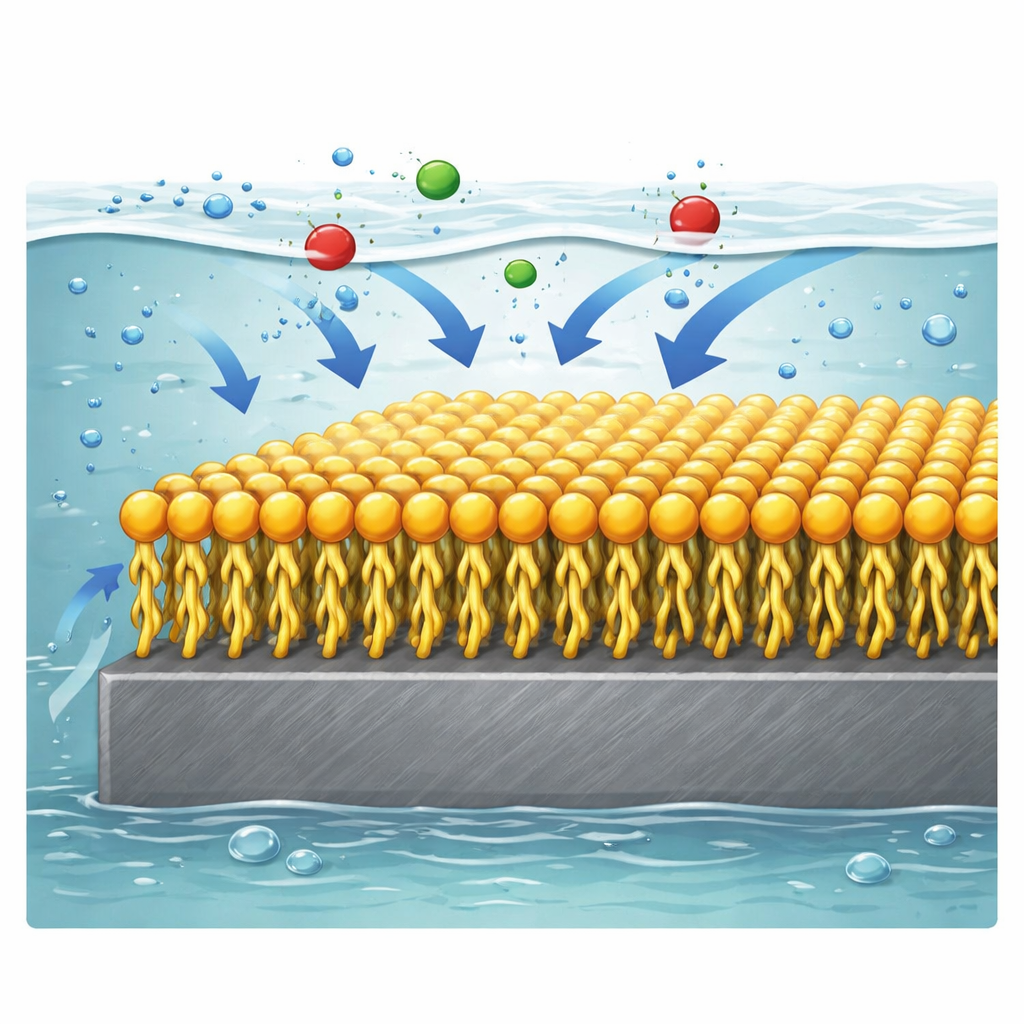
Bronvermelding: Abdelhafiz, F.M., Sami, R.M., Ghiaty, E.A. et al. Inhibitory influence of three new synthesized cationic gemini surfactants on the corrosion rate of carbon steel in 1 M HCl. Sci Rep 16, 12055 (2026). https://doi.org/10.1038/s41598-026-44281-2
Trefwoorden: corrosie van koolstofstaal, corrosieremmers, gemini-oppervlakteactieve stoffen, zure omgevingen, oppervlaktebescherming