Clear Sky Science · pl
Nanocząsteczki z naringeniną łagodzą neurotoksyczność wywołaną skopolaminą
Dlaczego cząsteczka z cytrusów i maleńkie cząstki mają znaczenie dla mózgu
W miarę starzenia się społeczeństw coraz więcej rodzin doświadcza ubytków pamięci i demencji, podczas gdy dzisiejsze leki zazwyczaj przynoszą jedynie tymczasową ulgę w objawach. W tym badaniu badacze rozważają pomysł: wykorzystać naringenin — naturalny związek występujący w owocach cytrusowych — i zapakować go w maleńkie cząsteczki, aby lepiej dotarł do mózgu i go chronił. Następnie sprawdzają, czy ta nanowersja naringeniny może złagodzić skutki działania leku, który czasowo zaburza pamięć u myszy, oraz czy połączenie jej ze standardowym lekiem na chorobę Alzheimera, donepezilem, może zwiększyć korzyści przy ograniczeniu działań niepożądanych.
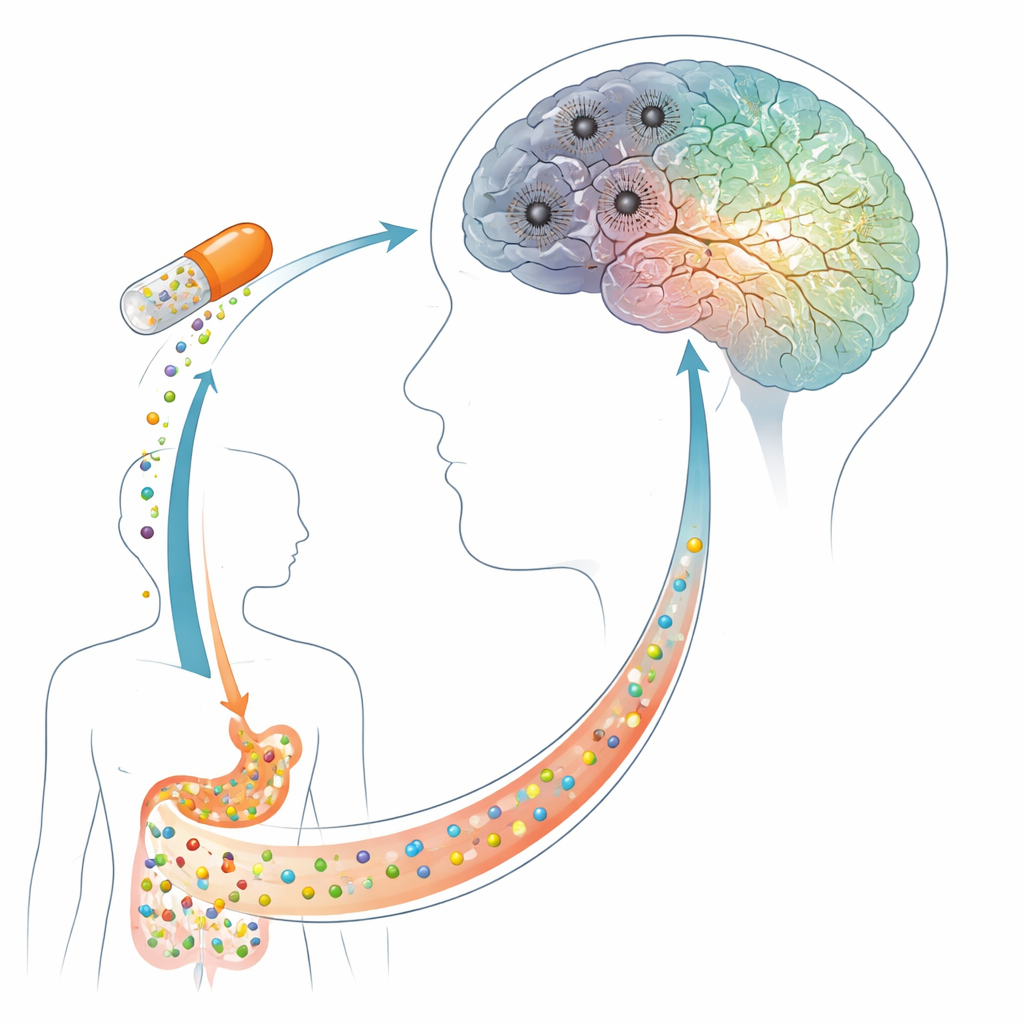
Przekształcanie cząsteczki z owoców w lek gotowy dla mózgu
Naringenina od dawna interesuje naukowców, ponieważ łagodzi stany zapalne, neutralizuje szkodliwe rodniki tlenowe i wpływa na kluczowe mechanizmy sygnalizacji w mózgu. Problem polega na tym, że przy zwykłym podaniu doustnym bardzo niewiele trafia do krwiobiegu, nie mówiąc o mózgu. Aby to obejść, zespół stworzył nanocząsteczki ładujące naringeninę — kuleczki o średnicy około 95 nanometrów, znacznie mniejsze niż czerwone krwinki — używając powszechnych środków powierzchniowo‑czynnych, by utrzymać je w stabilnej, jednorodnej formie. Szczegółowe obrazowanie i pomiary fizyczne wykazały, że cząsteczki były gładkie, jednolite i miały ujemny ładunek powierzchniowy, co pomaga im pozostawać rozproszonymi w płynach i przemieszczać się w organizmie. Testy in vitro sugerowały powolne uwalnianie naringeniny przez wiele godzin, co może utrzymywać stałą ochronę zamiast krótkich skoków stężenia.
Testowanie nowych cząsteczek w modelu zaburzeń pamięci
Aby sprawdzić, czy te cząsteczki naprawdę pomagają w żywym mózgu, badacze sięgnęli po znany model myszy z przejściowymi zaburzeniami pamięci. Zwierzętom podawano skopolaminę — lek, który krótkotrwale blokuje kluczowy układ komunikacyjny oparty na acetylocholinie oraz wywołuje stres oksydacyjny i stan zapalny — cechy przypominające niektóre wczesne zmiany obserwowane w chorobach neurodegeneracyjnych. Myszy otrzymywały następnie albo same nanocząsteczki z naringeniną, albo tylko donepezil, albo obie terapie razem, albo brak leczenia. Zespół ocenił uczenie w labiryncie wodnym, profile lipidowe krwi związane ze zdrowiem naczyń, chemiczne ślady uszkodzeń oksydacyjnych i zapalnych w tkance mózgowej, aktywność enzymów ochronnych, ekspresję wybranych genów mózgowych oraz mikroskopowe zmiany w hipokampie — obszarze kluczowym dla pamięci.
Co wydarzyło się w mózgu
Skopolamina sama w sobie upośledzała naukę w labiryncie, uszkadzała komórki mózgowe, zwiększała poziom szkodliwych utleniaczy i molekuł zapalnych oraz zaburzała profil lipidowy mózgu. Nanocząsteczki z naringeniną wyraźnie złagodziły te problemy. Leczone myszy szybciej uczyły się labiryntu, wykazywały wyższy poziom własnych mechanizmów przeciwutleniających mózgu i niższy poziom szkodliwych produktów ubocznych. Sygnały zapalne i markery uszkodzenia tkanek spadły, a lipidy mózgowe przeszły w zdrowszy układ, który może wspierać funkcję naczyń i błon komórkowych. Na poziomie mikroskopowym przekroje mózgu zwierząt leczonych pokazywały bardziej uporządkowane warstwy komórkowe i znacznie mniej oznak degeneracji. Gdy nanocząsteczki stosowano razem z umiarkowaną dawką donepezilu, poprawy były jeszcze wyraźniejsze, co sugeruje, że obie strategie się uzupełniają — jedna wzmacnia sygnalizację chemiczną, druga chroni komórki przed stresem i zapaleniem.
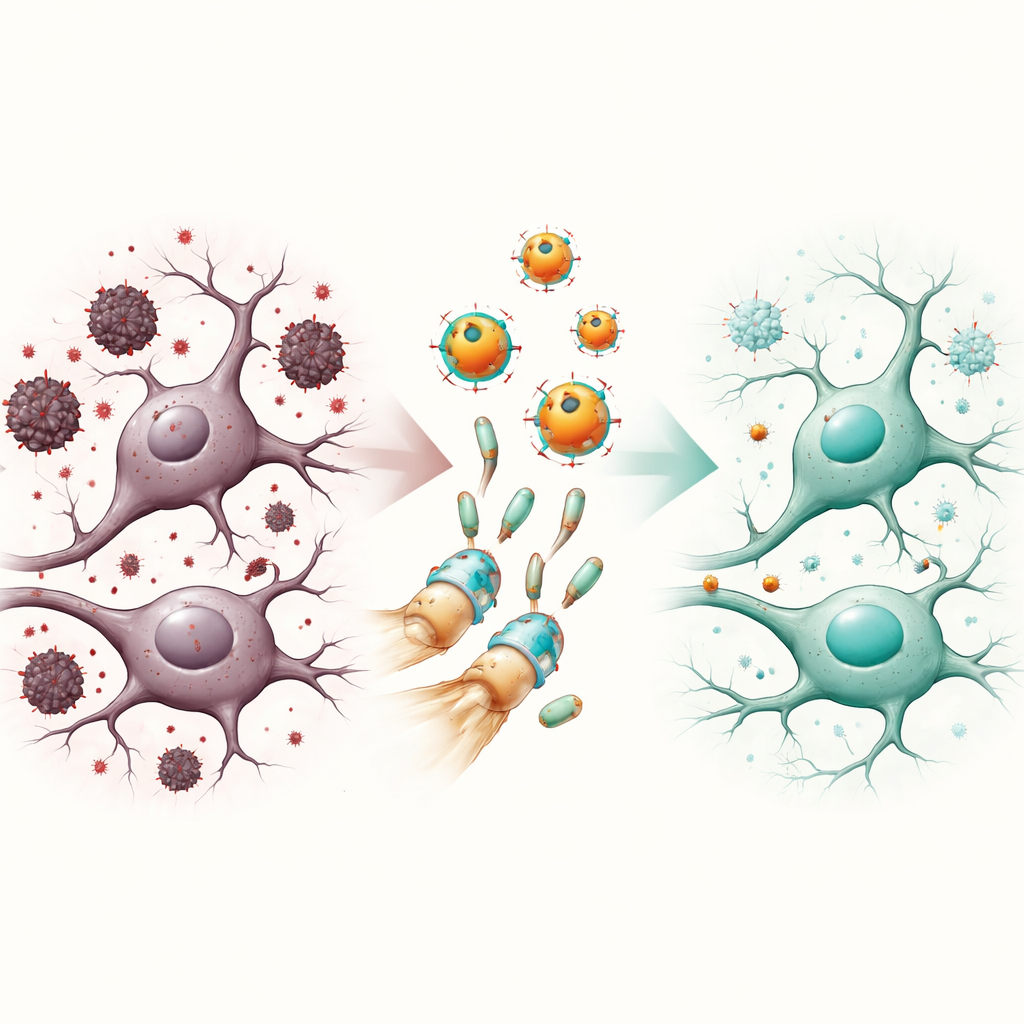
Wskazówki dotyczące mechanizmu ochrony
Poza tymi szerokimi wzorcami zespół przeanalizował kilka molekularnych „węzłów”. Stwierdzono, że skopolamina obniżała poziom podjednostki receptora związanego z uspokajającą aktywnością mózgu i podnosiła poziom kinazy często powiązanej ze szkodliwymi zmianami białek i zapaleniem. Nanocząsteczki z naringeniną odwracały te przesunięcia, a badania komputerowe dokowania sugerowały, że naringenina może fizycznie mieścić się i wpływać na oba cele. Leczenie także przywróciło aktywność szlaku sygnałowego związanego z przetrwaniem komórek i plastycznością. Razem te ustalenia malują obraz nanocząsteczek jako wielozadaniowych ochroniarzy, które przywracają równowagę obwodom mózgowym nie tylko poprzez neutralizację uszkodzeń chemicznych, ale też poprzez delikatne sterowanie kluczowymi przełącznikami kontrolującymi odpowiedź neuronów na stres.
Co to znaczy — i czego nie znaczy
Dla czytelnika ogólnego podsumowanie jest takie: zapakowanie związku pochodzącego z cytrusów w maleńkie nośniki uczyniło go bezpieczniejszym, bardziej stabilnym i znacznie efektywniejszym w ochronie mózgów myszy przed krótkotrwałym chemicznym uszkodzeniem. Nano‑naringenina łagodziła zaburzenia pamięci, uspokajała burze oksydacyjne i zapalne, poprawiała profil lipidów we krwi i zachowywała strukturę mózgu, zwłaszcza gdy łączono ją z niższą dawką standardowego leku na demencję. Jednak autorzy wyraźnie podkreślają, że model ten odzwierciedla ostre, odwracalne zaburzenie, a nie powolne, nieubłagane gromadzenie się patologicznych białek obserwowane w chorobie Alzheimera. Oznacza to, że wyniki wskazują na ochronę istotną dla objawów, a nie dowód prawdziwie modyfikującej przebieg choroby terapii. Aby stwierdzić, czy takie nanocząsteczki mogą rzeczywiście spowalniać lub zapobiegać chorobom neurodegeneracyjnym u ludzi, muszą zostać przetestowane w długoterminowych modelach zwierzęcych z postępującą patologią oraz w badaniach bezpośrednio potwierdzających, jak i gdzie naringenina działa w mózgu.
Cytowanie: Alqarni, A., Abd-Elghany, A.A., Bedewi, M.A. et al. Naringenin-loaded nanoparticles ameliorate scopolamine-induced neurotoxicity. Sci Rep 16, 13468 (2026). https://doi.org/10.1038/s41598-026-44225-w
Słowa kluczowe: nanocząsteczki naringeniny, neuroprotekcja, stres oksydacyjny, modele choroby Alzheimera, kombinacja z donepezilem