Clear Sky Science · ar
جسيمات نانوية محملة بالنارينجين تخفف السُمّية العصبية الناجمة عن سكوبولامين
لماذا يهم جزيء من الحمضيات وجسيمات صغيرة للدماغ
مع شيخوخة السكان، تتأثر عائلات أكثر بفقدان الذاكرة والخرف، لكن أدوية اليوم تعطي في الغالب تخفيفًا مؤقتًا للأعراض. تستعرض هذه الدراسة فكرة مبتكرة: أخذ النارينجين، مركب طبيعي موجود في فواكه الحمضيات، وتغليفه داخل جسيمات نانوية لكي يصل إلى الدماغ ويحميه بشكل أفضل. اختبر الفريق بعد ذلك ما إذا كان هذا الشكل النانوي من النارينجين يمكن أن يخفف تأثير دواء يعرقل الذاكرة مؤقتًا لدى الفئران، وما إذا كان اقترانه بدونيبيزيل، الدواء القياسي لمرض الألزهايمر، قد يعزز الفوائد ويحد من الآثار الجانبية.
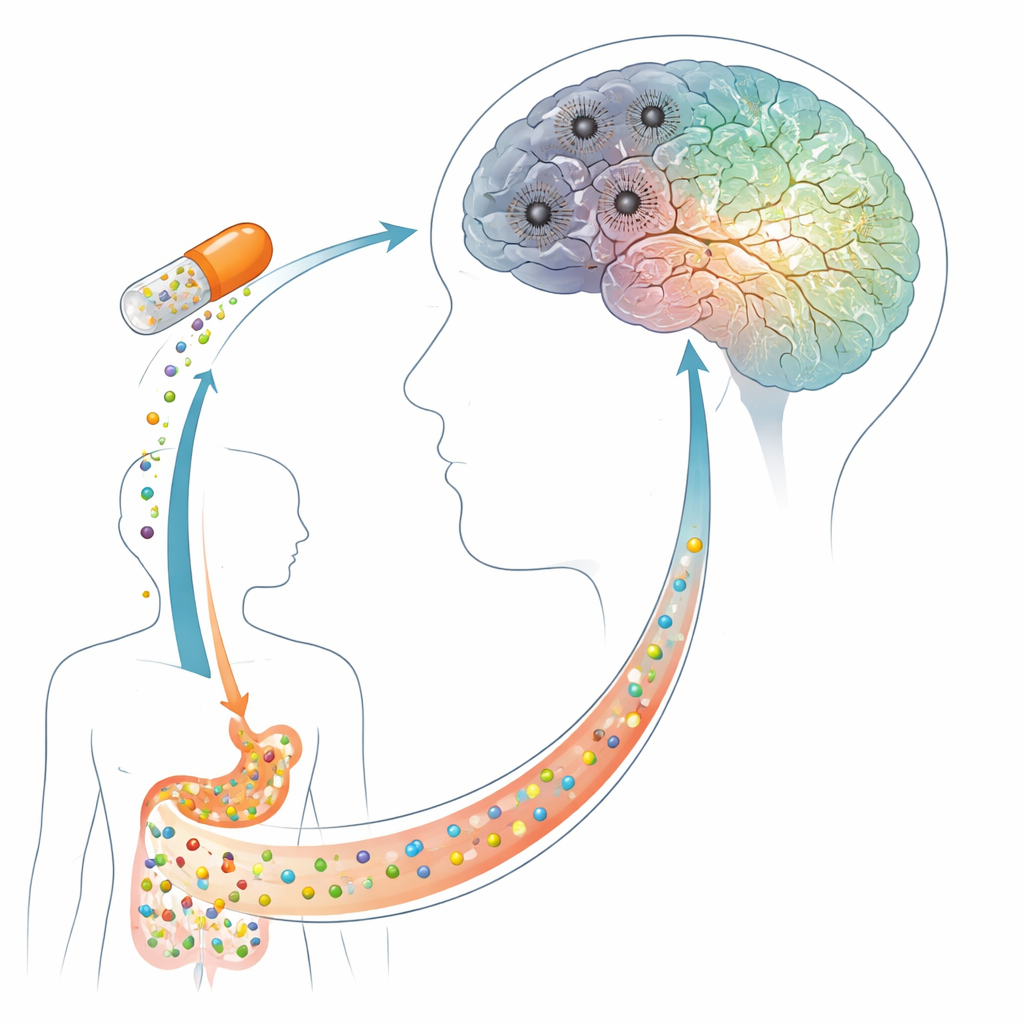
تحويل جزيء فاكهة إلى دواء جاهز للدماغ
أثار النارينجين اهتمام العلماء لوقت طويل لأنه يهدئ الالتهاب، ويحيّد الجزيئات المؤكسدة الضارة، ويؤثر على مسارات إشارية مهمة في الدماغ. المشكلة أن كمية ضئيلة منه تصل إلى مجرى الدم عند تناوله بالشكل العادي، ناهيك عن اختراقه للدماغ. لحل ذلك، صنع الفريق جسيمات نانوية محملة بالنارينجين—كرات يبلغ قطرها حوالي 95 نانومتر، أصغر بكثير من خلية دم حمراء—باستخدام عوامل مساعدية شائعة للحفاظ على استقرارها وتشتتها بالتساوي. أظهر التصوير والقياسات الفيزيائية أن هذه الجسيمات ناعمة وموحدة وتحمل شحنة سطحية سالبة تساعدها على البقاء منفصلة في السوائل والتحرك عبر الجسم. أشارت اختبارات المختبر إلى أنها تطلق النارينجين ببطء على مدى ساعات عدة، مما قد يساعد في الحفاظ على حماية مستمرة بدلًا من دفعات حادة.
اختبار تحمل هذه الجسيمات في نموذج الذاكرة
لمعرفة ما إذا كانت هذه الجسيمات تساعد دماغًا حيًا فعلاً، لجأ الباحثون إلى نموذج فأري معروف لاضطرابات الذاكرة المؤقتة. أعطوا الحيوانات سكوبولامين، وهو دواء يحجب مؤقتًا نظام تواصل رئيسي يعتمد على الناقل العصبي أسيتيل كولين كما يثير الإجهاد التأكسدي والالتهاب—سمات تعكس بعض التغيرات المبكرة التي تُرى في الأمراض التنكسية العصبية. تَلَقَّت الفئران بعد ذلك إما الجسيمات النانوية المحمّلة بالنارينجين وحدها، أو الدونيبيزيل وحده، أو الجمع بينهما، أو لا علاج. قاس الفريق التعلم في متاهة مائية، والدهون الدموية المرتبطة بصحة الأوعية، والمؤشرات الكيميائية للضرر التأكسدي والالتهاب في نسيج المخ، ونشاط الإنزيمات الواقية، وتعبير بعض الجينات المرتبطة بالدماغ، والتغيرات المجهرية في الحُصين، المنطقة الحرجة للذاكرة.
ما الذي حدث داخل الدماغ
أضعف السكوبولامين وحده تعلم المتاهة، وألحق أضرارًا بالخلايا العصبية، وزاد الجذور المؤكسدة والجزيئات الالتهابية الضارة، وأربك ملف الدهون الدماغي. خففت الجسيمات النانوية المحمّلة بالنارينجين هذه المشاكل بوضوح. تعلمت الفئران المعالجة المتاهة أسرع، وأظهرت مستويات أعلى من دفاعات المضادات الأكسدة الذاتية للدماغ، وانخفضت مستويات النواتج الضارة. تراجعت الإشارات الالتهابية وعلامات إصابة الأنسجة، بينما تحركت دهون الدماغ نحو نمط صحي أكثر قد يدعم وظيفة الأوعية وغشاء الخلايا. على مستوى المجهر، أظهرت مقاطع الدماغ من الحيوانات المعالجة طبقات خلوية أكثر انتظامًا وأقل بكثير من علامات التنكس. عندما جمع الباحثون بين الجسيمات النانوية وجرعة معتدلة من الدونيبيزيل، كانت التحسينات أكثر وضوحًا، مما يشير إلى أن الطريقتين تكملان بعضهما البعض—واحدة تعزز الإشارة الكيميائية، والأخرى تحمي الخلايا من الإجهاد والالتهاب.
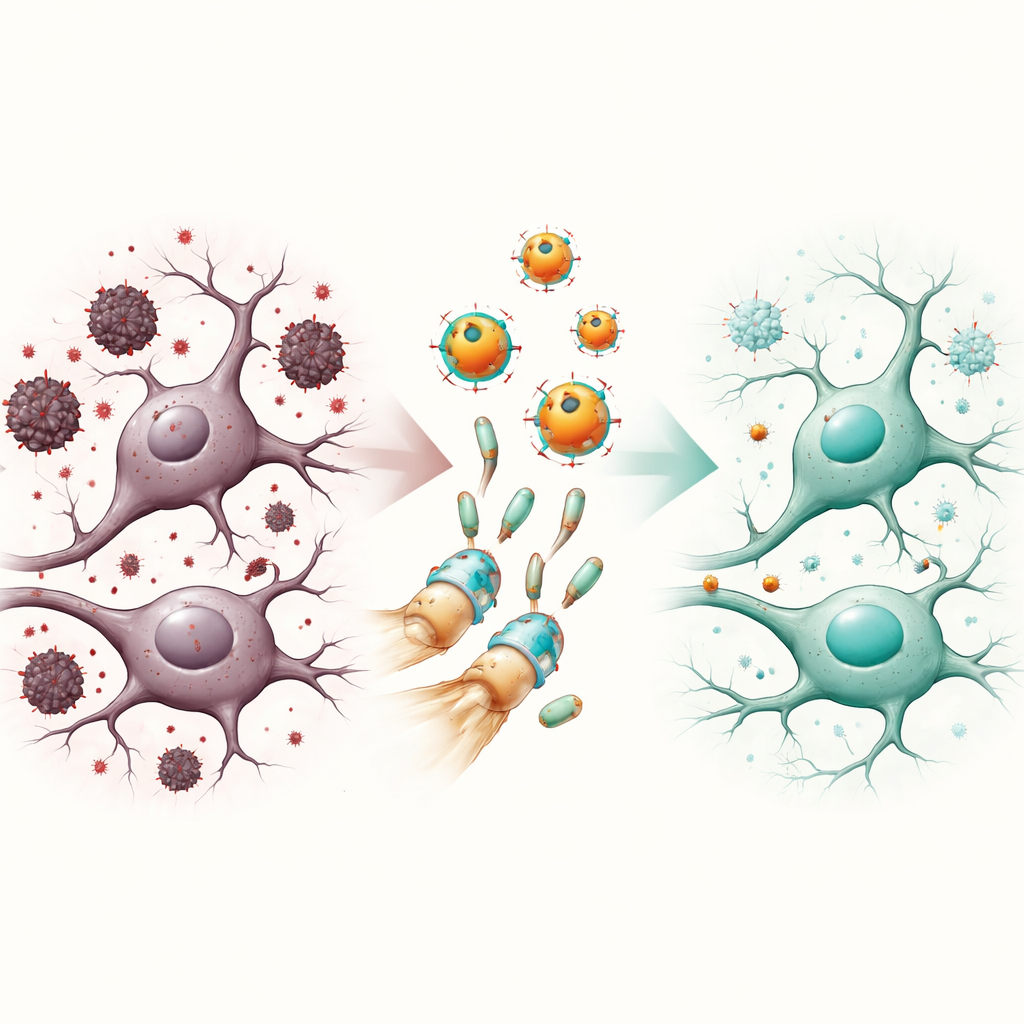
دلائل على آلية الحماية
خارج هذه الأنماط العامة، فحص الفريق عدة «مفاصل» جزيئية. وجدوا أن السكوبولامين خفض مستويات وحدة مستقبل مرتبطة بتهدئة نشاط الدماغ وزاد مستويات كيناز، وهو إنزيم غالبًا ما يرتبط بتغيرات بروتينية ضارة والالتهاب. عكست الجسيمات النانوية المحمّلة بالنارينجين هذه التحولات، وأشارت دراسات ربط حاسوبية إلى أن النارينجين يمكن أن يتناسب فعليًا مع كلا الهدفين ويؤثر عليهما. أعاد العلاج أيضًا نشاط مسار إشاري مرتبط ببقاء الخلايا والمرونة العصبية. مجتمعة، تصوّر هذه النتائج الجسيمات النانوية كحماة متعددة المهام يعيدون دوائر الدماغ نحو التوازن، ليس فقط عن طريق القضاء على الضرر الكيميائي، بل عن طريق تحريك مفاتيح رئيسية تتحكم في كيفية استجابة الخلايا العصبية للإجهاد.
ما الذي يعنيه هذا — وما لا يعنيه
بالنسبة للقارئ العام، الخلاصة هي أن تغليف مركب مشتق من الحمضيات داخل ناقلات نانوية جعله أكثر أمانًا واستقرارًا وأكثر فاعلية في حماية أدمغة الفئران من اعتداء كيميائي قصير الأمد. خفف النارينجين النانوي مشاكل الذاكرة، وهدأ العواصف التأكسدية والالتهابية، وحسّن أنماط الدهون الدموية، وحافظ على بنية الدماغ، خصوصًا عند اقترانه بجرعة منخفضة من دواء الخرف القياسي. مع ذلك، يؤكد المؤلفون بحذر أن هذا النموذج يحاكي اضطرابًا حادًا وقابلاً للعكس، وليس التراكم البطيء والمتواصل للبروتينات المرتبطة بالمرض كما يُرى في ألزهايمر. هذا يعني أن النتائج تبرز حماية ذات صلة بالأعراض بدلاً من دليل على تعديل مسار المرض نفسه. لمعرفة ما إذا كانت هذه الجسيمات النانوية يمكن أن تبطئ فعليًا أو تمنع أمراض الدماغ التنكسية لدى البشر، يجب اختبارها لاحقًا في نماذج حيوانية طويلة الأمد ذات مرض متقدم وفي دراسات تؤكد مباشرة كيف وأين يعمل النارينجين داخل الدماغ.
الاستشهاد: Alqarni, A., Abd-Elghany, A.A., Bedewi, M.A. et al. Naringenin-loaded nanoparticles ameliorate scopolamine-induced neurotoxicity. Sci Rep 16, 13468 (2026). https://doi.org/10.1038/s41598-026-44225-w
الكلمات المفتاحية: جسيمات نارينجين النانوية, الحماية العصبية, الإجهاد التأكسدي, نماذج ألزهايمر, توليفة مع الدونيبيزيل