Clear Sky Science · pl
CHD1L promuje progresję raka jądra poprzez epigenetyczną aktywację osi CXCR6/PI3K/AKT
Dlaczego te badania są ważne dla młodych mężczyzn
Rak jądra jest najczęstszym nowotworem litym u młodych mężczyzn; we wczesnych stadiach choroba często jest uleczalna, ale niektóre guzy się rozsiewają lub przestają reagować na standardową chemioterapię. To badanie zagląda w głąb mechanizmów komórek nowotworowych i towarzyszącego im układu odpornościowego, odkrywając kluczowy czynnik — białko CHD1L. Pokazując, jak CHD1L sprzyja wzrostowi, rozprzestrzenianiu się i uchylaniu się przed atakiem immunologicznym, praca ta wskazuje nowe potencjalne słabe ogniwo, które w przyszłości mogą wykorzystać leki, gdy standardowe terapie zawiodą.
Ukryty przełącznik w obrębie guzów jądra
Naukowcy zaczęli od pytania, czy CHD1L — znane z przekształcania organizacji chromatyny w innych nowotworach — odgrywa również rolę w raku jądra. Analizując próbki guzów od pacjentów oraz dane z The Cancer Genome Atlas, stwierdzili, że poziomy CHD1L były znacznie podwyższone w guzach jądra w porównaniu z normalną tkanką jądra. Wysoki poziom CHD1L był szczególnie częsty w guzach bardziej zaawansowanych i naciekających, co sugeruje, że to białko nie tylko jest obecne, lecz także powiązane z agresywną postacią choroby. Analizy statystyczne wykazały, że ekspresja CHD1L może pomóc w rozróżnieniu tkanki nowotworowej od prawidłowej z dobrą dokładnością.
Guz, który rośnie szybciej i przenosi się dalej
Aby sprawdzić, co CHD1L rzeczywiście robi, zespół manipulował jego poziomami w liniach komórkowych raka jądra hodowanych w laboratorium. Po zwiększeniu CHD1L komórki dzieliły się szybciej, tworzyły znacznie więcej kolonii, poruszały się szybciej po sztucznych „ranach” i naciekały przez bariery imitujące tkankę. Po obniżeniu poziomu CHD1L za pomocą ukierunkowanych narzędzi RNA obserwowano efekt odwrotny: hamowanie wzrostu komórek, wzrost apoptozy i zmniejszoną zdolność do migracji i inwazji. U myszy guzy pochodzące z komórek z podwyższonym CHD1L były większe, rosły szybciej i wykazywały wyższy poziom zarówno CHD1L, jak i markera proliferacji, co potwierdza, że to białko może napędzać wzrost guza in vivo.
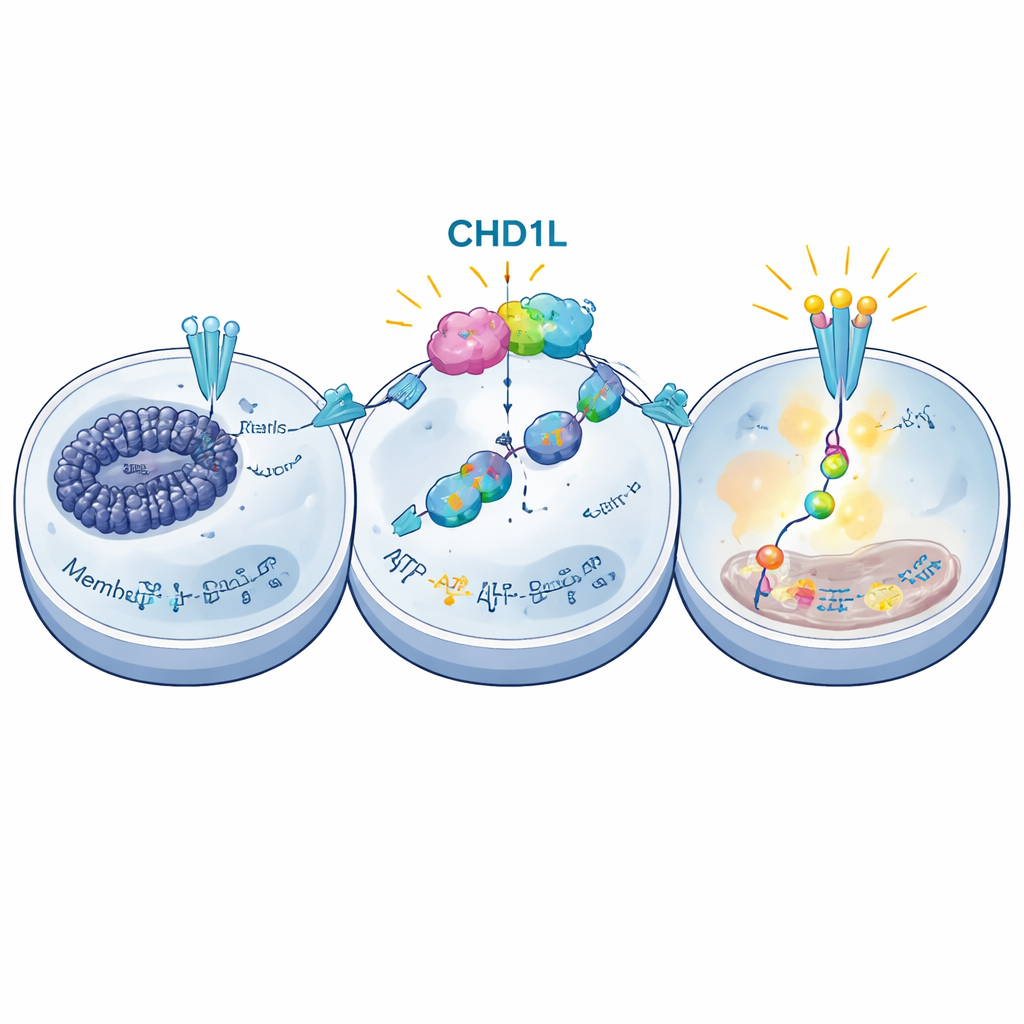
Jak CHD1L przeprogramowuje sygnały komórkowe
CHD1L nie działa jak prosty włącznik/wyłącznik; wpływa na przebudowę pakowania DNA, co z kolei kontroluje, które geny są aktywne. Naukowcy zastosowali metody ogniskujące się na całym genomie, aby zmierzyć zarówno regiony DNA otwarte i dostępne, jak i geny aktywne w komórkach z i bez CHD1L. Odkryli, że CHD1L pomaga utrzymywać określone odcinki DNA otwarte w pobliżu kluczowych genów zaangażowanych w komunikację chemiczną między komórkami. Jednym z wyróżniających się celów był CXCR6, receptor na powierzchni komórki, który może uruchamiać wewnątrzkomórkową ścieżkę wzrostu znaną jako PI3K/AKT. Po wyciszeniu CHD1L rejon DNA przy genie CXCR6 stał się bardziej skondensowany, poziomy CXCR6 spadły, a aktywność szlaku PI3K/AKT osłabła. Dalsze eksperymenty wykazały, że ta zmiana organizacji chromatyny wiązała się ze wzrostem represyjnego znaku chemicznego na histonach — H3K9me3 — który kumulował się w rejonie kontrolnym CXCR6 po utracie CHD1L.
Ucieczka przed atakiem odpornościowym w sąsiedztwie guza
Ponad samymi komórkami nowotworowymi zespół zbadał również, jak CHD1L koreluje z komórkami układu odpornościowego infiltrującymi guzy. Analiza dużych zbiorów danych pacjentów wykazała, że guzy o wyższych poziomach CHD1L miały tendencję do wzorców „wykluczenia” immunologicznego — komórki odpornościowe zdolne do zabijania, takie jak cytotoksyczne limfocyty T i komórki NK, były mniej aktywne lub trzymane na dystans, podczas gdy typy komórek związane z tłumieniem odpowiedzi, jak komórki regulatorowe i niektóre pomocnicze limfocyty T, były bardziej obecne. Te guzy miały wyższe ogólne wskaźniki związane z tkanką stromalną i infiltracją immunologiczną, ale jednocześnie objawy upośledzonej funkcji odpornościowej, co sugeruje, że nowotwory o wysokim CHD1L otaczają się mikrośrodowiskiem immunologicznym, które wygląda na aktywne, lecz jest nieskuteczne w atakowaniu guza.
Co to oznacza dla przyszłego leczenia
Podsumowując, wyniki pokazują, że CHD1L działa jako główny regulator, który pomaga komórkom raka jądra rosnąć, rozsiewać się i prawdopodobnie unikać zniszczenia przez układ odpornościowy poprzez epigenetyczne włączanie osi sygnałowej CXCR6/PI3K/AKT oraz modyfikowanie mikrośrodowiska guza. Dla pacjentów, szczególnie tych z zaawansowaną lub oporną na leczenie chorobą, wskazuje to na CHD1L jako obiecujący marker służący do identyfikacji nowotworów wysokiego ryzyka oraz potencjalny cel dla terapii nowej generacji, które będą przeprogramowywać aktywność genów komórki nowotworowej zamiast jedynie zabijać dzielące się komórki. Choć potrzebne są dalsze badania, w tym opracowanie leków i testy w bardziej realistycznych modelach, praca ta otwiera nową drogę do poradzenia sobie z trudnymi przypadkami raka jądra.
Cytowanie: Zhao, Y., Yan, H., Chen, X. et al. CHD1L promotes testicular cancer progression through epigenetic activation of the CXCR6/PI3K/AKT pathway. Sci Rep 16, 13955 (2026). https://doi.org/10.1038/s41598-026-43901-1
Słowa kluczowe: rak jądra, CHD1L, regulacja epigenetyczna, oś CXCR6 PI3K AKT, mikrośrodowisko guza