Clear Sky Science · ar
يعزز CHD1L تقدم سرطان الخصية من خلال التفعيل الوراثي/الابيجيني لمسار CXCR6/PI3K/AKT
لماذا يهم هذا البحث للشباب
يُعتبر سرطان الخصية أكثر أنواع الأورام الصلبة شيوعًا لدى الرجال صغار السن، وعلى الرغم من أن الحالات المبكرة غالبًا ما تكون قابلة للشفاء، فإن بعض الأورام تنتشر أو تتوقف عن الاستجابة للعلاج الكيميائي القياسي. يتعمق هذا البحث في الآليات الداخلية لخلايا سرطان الخصية وبيئة المناعة المحيطة بها، كاشفًا عن جزيء فاعل رئيسي يُدعى CHD1L. من خلال توضيح كيفية مساعدة CHD1L للأورام على النمو والانتشار وتجنب هجوم الجهاز المناعي، يشير العمل إلى نقطة ضعف جديدة قد تستهدفها أدوية مستقبلية عندما تفشل العلاجات الحالية.
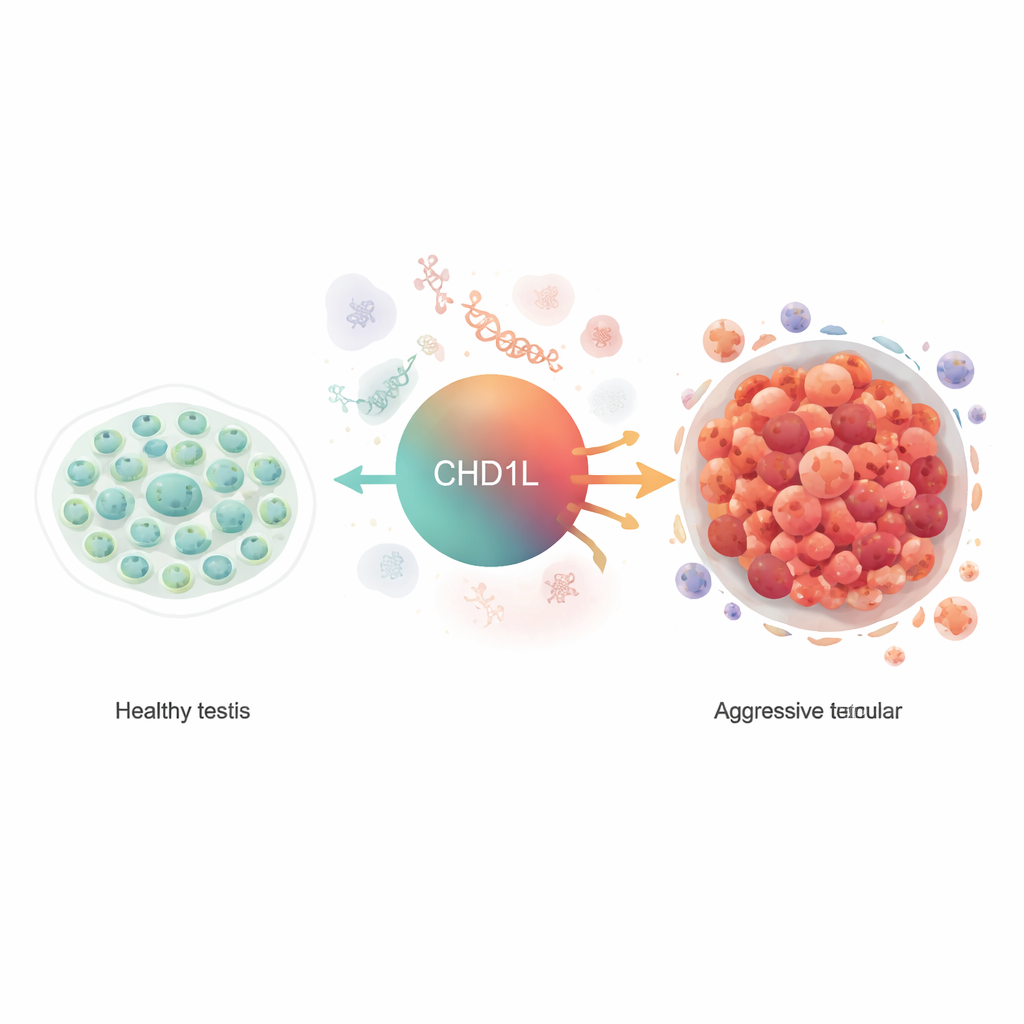
مفتاح مخفي داخل أورام الخصية
بدأ الباحثون بالسؤال عما إذا كان CHD1L، وهو بروتين معروف بإعادة تشكيل تغليف الحمض النووي في سرطانات أخرى، يلعب دورًا أيضًا في سرطان الخصية. باستخدام عينات أورام من مرضى وبيانات من مشروع أطلس الجينوم السرطاني (The Cancer Genome Atlas)، وجدوا أن مستويات CHD1L كانت أعلى بكثير في أورام الخصية مقارنة بأنسجة الخصية السليمة. كان ارتفاع CHD1L أكثر شيوعًا في الأورام المتقدمة والغازية، مما يشير إلى أن هذا البروتين ليس موجودًا فحسب، بل مرتبط أيضًا بمرض عدواني. أظهرت التحليلات الإحصائية أن تعبير CHD1L يمكن أن يساعد في تمييز نسيج السرطان عن النسيج الطبيعي بدقة جيدة.
ورم ينمو أسرع وينتشر أبعد
لاختبار وظيفة CHD1L الفعلية، عبّرت الفرق عن مستوياتها في خطوط خلايا سرطان الخصية المزروعة مخبرية. عندما زادوا CHD1L، انقسمت الخلايا بسرعة أكبر، وشكلت مستعمرات أكثر، وتحركت أسرع عبر «جروح» اصطناعية، وغزت عبر حواجز تحاكي الأنسجة. عندما خفّضوا CHD1L باستخدام أدوات RNA مستهدفة، حدث العكس: تباطأ نمو الخلايا، وزاد الموت الخلوي المبرمج، وقلت قدرة الخلايا على الهجرة والغزو. في الفئران، كانت الأورام المزروعة من خلايا زادت فيها CHD1L أكبر حجماً، ونمت أسرع، وأظهرت مستويات أعلى من CHD1L وعلامة التكاثر، مؤكدة أن هذا البروتين يمكن أن يقود نمو الورم في كائن حي.
كيف يعيد CHD1L توصيل إشارات الخلية
لا يعمل CHD1L كمفتاح بسيط يشغّل أو يطفئ؛ بل يعيد تشكيل كيفية تغليف الحمض النووي، وهو ما يتحكم بدوره في أي الجينات يتم تشغيلها. استخدم العلماء طرقًا جينومية واسعة النطاق لقياس المناطق المفتوحة والمتاحة من الحمض النووي، ولتحديد الجينات النشطة، في خلايا مع وجود CHD1L أو بدونه. وجدوا أن CHD1L يساعد في الحفاظ على مناطق معينة من الحمض النووي مفتوحة بالقرب من جينات رئيسية متورطة في الرسائل الكيميائية بين الخلايا. كان من بين الأهداف البارزة جين CXCR6، مستقبل على سطح الخلية يمكنه تنشيط مسار نمو داخلي معروف باسم PI3K/AKT. عند خفض CHD1L، أصبح الإقليم القريب من جين CXCR6 أكثر تشابكًا، وانخفضت مستويات CXCR6، وتراجع نشاط مسار PI3K/AKT. أظهرت تجارب إضافية أن هذا التغير في التغليف تضمن زيادة في علامة كيميائية كابحة على الهيستونات تُدعى H3K9me3، والتي تراكمت في منطقة تنظيم CXCR6 عند غياب CHD1L.
الهروب من هجوم المناعة في حي الورم
بعيدًا عن الخلايا السرطانية نفسها، درس الفريق أيضًا كيف يرتبط CHD1L بخلايا المناعة التي تغزو الأورام. من خلال تحليل مجموعات بيانات مرضى واسعة، لوحظ أن الأورام التي تحتوي على CHD1L مرتفع تميل إلى إظهار أنماط من «استبعاد» المناعة، حيث كانت الخلايا المناعية الفعالة مثل الخلايا التائية القاتلة والخلايا القاتلة الطبيعية أقل نشاطًا أو محجوبة، بينما كانت أنواع الخلايا المرتبطة بالقمع، مثل الخلايا التائية المنظمة وبعض خلايا المساعدة، أكثر بروزًا. كانت لهذه الأورام درجات مناعية ودرجات نسيجية داعمة أعلى بشكل عام لكنها لا تزال تظهر علامات ضعف في الوظيفة المناعية، مما يوحي بأن سرطانات ذات CHD1L عالية قد تحيط نفسها بمشهد مناعي يبدو نشيطًا لكنه غير فعّال في مهاجمة الورم.
ماذا يعني هذا للعلاج المستقبلي
تُظهر النتائج مجتمعة أن CHD1L يعمل كمتحكم رئيسي يساعد خلايا سرطان الخصية على النمو والانتشار وربما الهروب من التدمير المناعي عن طريق التبديل الإبيجيني في محور الإشارات CXCR6/PI3K/AKT وتغيير البيئة الدقيقة للورم. بالنسبة للمرضى، خصوصًا الذين يعانون مرضًا متقدمًا أو مقاومًا للعلاج، يشير ذلك إلى أن CHD1L يمكن أن يكون علامة واعدة لتحديد الأورام عالية المخاطر، وهدفًا محتملاً للعلاجات الجديدة التي تعمل على إعادة برمجة نشاط الجينات في الخلية السرطانية بدلًا من قتل الخلايا المنقسمة فقط. وبينما هناك حاجة لمزيد من الدراسات، بما في ذلك تطوير الأدوية والاختبارات في نماذج أكثر واقعية، يفتح هذا العمل مسارًا جديدًا للتعامل مع حالات سرطان الخصية الصعبة.
الاستشهاد: Zhao, Y., Yan, H., Chen, X. et al. CHD1L promotes testicular cancer progression through epigenetic activation of the CXCR6/PI3K/AKT pathway. Sci Rep 16, 13955 (2026). https://doi.org/10.1038/s41598-026-43901-1
الكلمات المفتاحية: سرطان الخصية, CHD1L, الضبط الإبيجيني, مسار CXCR6 PI3K AKT, البيئة الدقيقة للورم