Clear Sky Science · pl
Walidacja ferroptozy u danio pręgowanego jako wiarygodnego modelu do badań fenotypowych
Dlaczego małe rybki mają znaczenie dla zrozumienia śmierci komórkowej
Naukowcy odkryli stosunkowo nowy sposób umierania komórek, zwany ferroptozą, napędzany przez żelazo i wymykające się spod kontroli reakcje chemiczne uszkadzające lipidy w błonach komórkowych. Proces ten powiązano z rakiem, chorobami mózgu, zaburzeniami serca i chorobami naczyń krwionośnych, lecz większość badań opierała się dotąd na myszach, które są powolne i kosztowne w badaniach. Niniejsza praca bada, czy danio pręgowane — małe, szybko rosnące rybki akwariowe, których geny są dość podobne do ludzkich — mogą dać szybszy i jaśniejszy wgląd w ferroptozę oraz jej wpływ na rozwijające się tkanki, takie jak naczynia krwionośne i kości.
Nowy rodzaj śmierci komórki pod mikroskopem
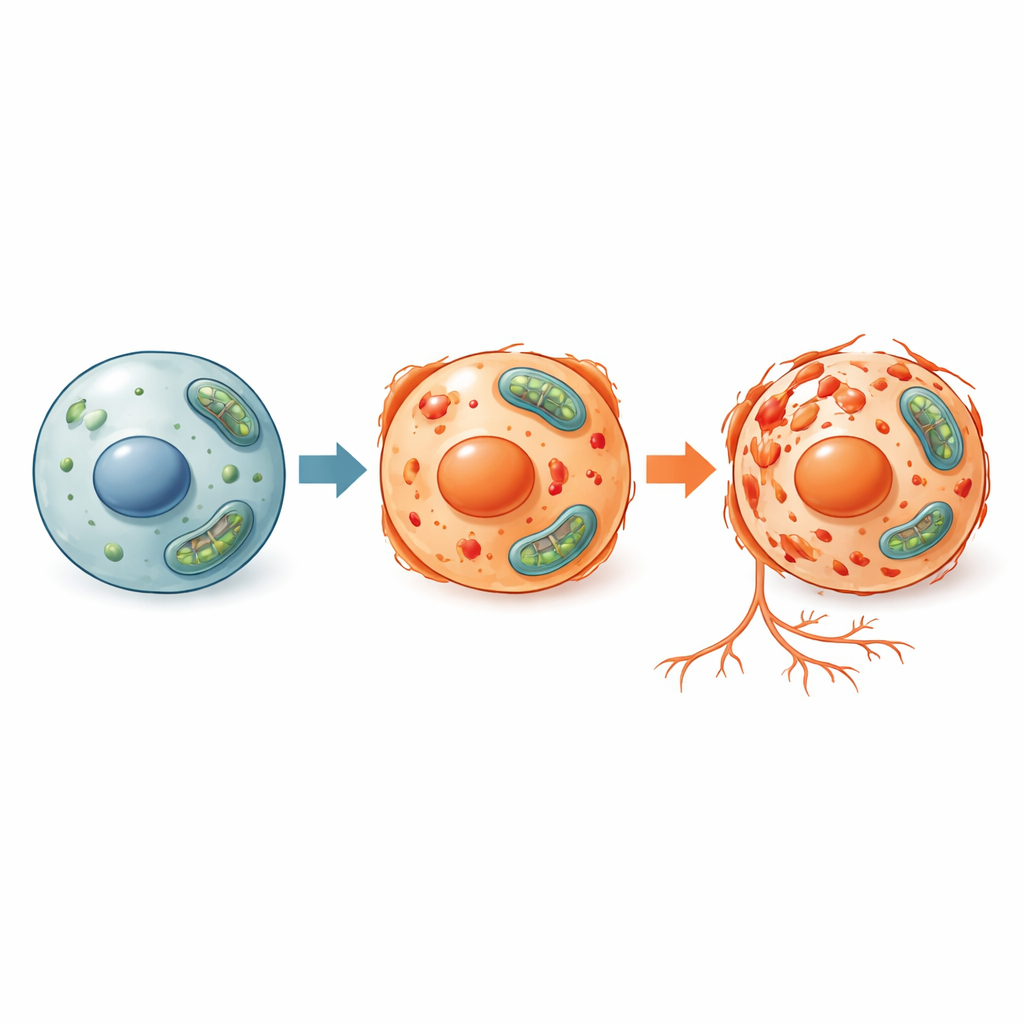
Ferroptoza różni się od lepiej znanych form śmierci komórkowej, takich jak apoptoza (porządkowane, zaprogramowane samounicestwienie) i nekroza (bardziej chaotyczny upadek). W ferroptozie żelazo i reaktywne formy tlenu współdziałają, atakując lipidy budujące błony komórkowe, co ostatecznie prowadzi do niewydolności komórki. Ponieważ ta ścieżka jest ściśle powiązana z gospodarką żelazem i obroną antyoksydacyjną, może odgrywać kluczową rolę w stanach związanych z gromadzeniem się żelaza lub nadmiernym stresem oksydacyjnym tkanek, w tym w niektórych nowotworach, udarach i chorobach degeneracyjnych. Do badania tego procesu i testowania potencjalnych terapii potrzebne są modele zwierzęce zarówno biologicznie istotne, jak i eksperymentalnie elastyczne.
Dlaczego danio pręgowane są silnym substytutem dla człowieka
Danio pręgowane oferują kilka zalet jako żywe laboratorium. Są kręgowcami, których około 85 procent genów ma odpowiedniki u ludzi, a ich szlaki sygnalizacyjne odpowiedzialne za wzrost i choroby są zaskakująco podobne. Zarodki rozwijają się poza organizmem matki i są przeźroczyste, co umożliwia bezpośrednie obserwowanie w czasie rzeczywistym powstawania narządów, naczyń krwionośnych i kości. Danio są tanie w hodowli na dużą skalę, co czyni je idealnymi do testowania wielu zmian genetycznych lub kandydatów na leki jednocześnie. Kluczowe pytanie tego badania brzmiało, czy cechy ferroptozy obserwowane w komórkach ssaczych — zależne od żelaza uszkodzenia oksydacyjne, zmiany w cząsteczkach ochronnych oraz zmiany w określonych genach i białkach — pojawiają się także u danio pręgowanego i czy da się je wyraźnie odróżnić od innych typów śmierci komórkowej.
Wzbudzanie ferroptozy u żywych danio pręgowanego
Badacze narażali młode danio na trzy różne czynniki wywołujące ferroptozę: dwa chemiczne induktory (Erastin i FIN56) oraz formę żelaza zwaną chlorkiem żelaza amonowego (ammonium ferric citrate). Mierzyli kilka oznak stresu wewnątrz ryb, w tym nagromadzenie reaktywnych form tlenu, równowagę pomiędzy kluczowym antyoksydantem (glutationem) a jego utlenioną formą oraz obecność uszkodzonych lipidów. Zbadali także, które geny były włączone lub wyłączone oraz zmierzyli poziomy centralnego białka ochronnego zwanego GPX4, które normalnie chroni błony komórkowe przed atakiem oksydacyjnym. We wszystkich trzech warunkach leczenia komórki danio wykazały oczekiwany podpis ferroptozy: zwiększone uszkodzenia oksydacyjne, zaburzoną równowagę antyoksydacyjną, obniżone białko GPX4 oraz aktywację genów powiązanych z ferroptozą. Jednocześnie markery apoptozy i autofagii zmieniały się w niewielkim stopniu, co wskazuje, że obserwowana śmierć komórek była specyficznie ferroptotyczna.
Jak ferroptoza zakłóca rozwój naczyń krwionośnych
Aby zobaczyć, jak ten proces wpływa na cały układ narządów, zespół użył transgenicznej linii danio, której naczynia krwionośne świecą pod mikroskopem. Gdy ryby te były traktowane indykatorem ferroptozy Erastinem, zwykle jasne, dobrze rozgałęzione naczynia wzdłuż grzbietu wydawały się cieńsze i przygaszone, co sugerowało zahamowanie wzrostu naczyń. Gdy naukowcy dodali leki blokujące ferroptozę lub wiążące nadmiar żelaza, wiele z tych defektów uległo złagodzeniu, co sugeruje, że ferroptoza napędzana żelazem w komórkach wyściełających naczynia bezpośrednio upośledza rozwój naczyń. Ponieważ wzrost naczyń krwionośnych jest ściśle powiązany z tworzeniem kości — relacja znana jako sprzężenie osteogenezy i angiogenezy — wyniki te stawiają danio pręgowane jako obiecujący model nie tylko chorób naczyniowych, lecz także zaburzeń kości związanych z przeciążeniem żelazem i uszkodzeniem oksydacyjnym.
Co to oznacza dla przyszłych badań nad chorobami
Pokazując, że ferroptoza u danio pręgowanego wiernie odzwierciedla obserwacje z układów ssaczych oraz że można ją indukować, mierzyć, a nawet odwracać za pomocą specyficznych leków, to badanie potwierdza danio jako praktyczny i wiarygodny model do badania śmierci komórkowej zależnej od żelaza. Dla czytelnika popularnonaukowego istotne przesłanie jest takie, że małe, przezroczyste rybki mogą pomóc naukowcom szybko przetestować, jak ferroptoza przyczynia się do chorób takich jak rak, udar, choroby naczyń i osteoporoza, oraz przesiewać terapie, które mogłyby chronić tkanki. Krótko mówiąc, danio pręgowane oferują szybki, wizualny i genetycznie podatny sposób badania destrukcyjnej formy śmierci komórkowej, która coraz częściej uznawana jest za wspólny czynnik wielu ludzkich schorzeń.
Cytowanie: Cao, Z., Liu, G., Zhang, R. et al. Validation of ferroptosis in zebrafish as a reliable model for phenotypic studies. Sci Rep 16, 14357 (2026). https://doi.org/10.1038/s41598-026-43493-w
Słowa kluczowe: ferroptoza, danio pręgowane, stres oksydacyjny, angiogeneza, przeciążenie żelazem