Clear Sky Science · es
Validación de la ferroptosis en pez cebra como modelo fiable para estudios fenotípicos
Por qué importan los peces diminutos para entender la muerte celular
Los científicos han descrito una vía relativamente nueva de muerte celular, llamada ferroptosis, impulsada por el hierro y por reacciones químicas fuera de control que dañan los lípidos de las membranas celulares. Este proceso se ha relacionado con el cáncer, enfermedades neurológicas, problemas cardíacos y trastornos vasculares, pero la mayor parte de la investigación hasta ahora se ha basado en ratones, cuyo estudio es lento y costoso. Este artículo explora si el pez cebra —pececillos de acuario de rápido crecimiento cuyos genes se parecen mucho a los nuestros— puede ofrecer una ventana más rápida y clara a la ferroptosis y sus efectos sobre tejidos en crecimiento como los vasos sanguíneos y el hueso.
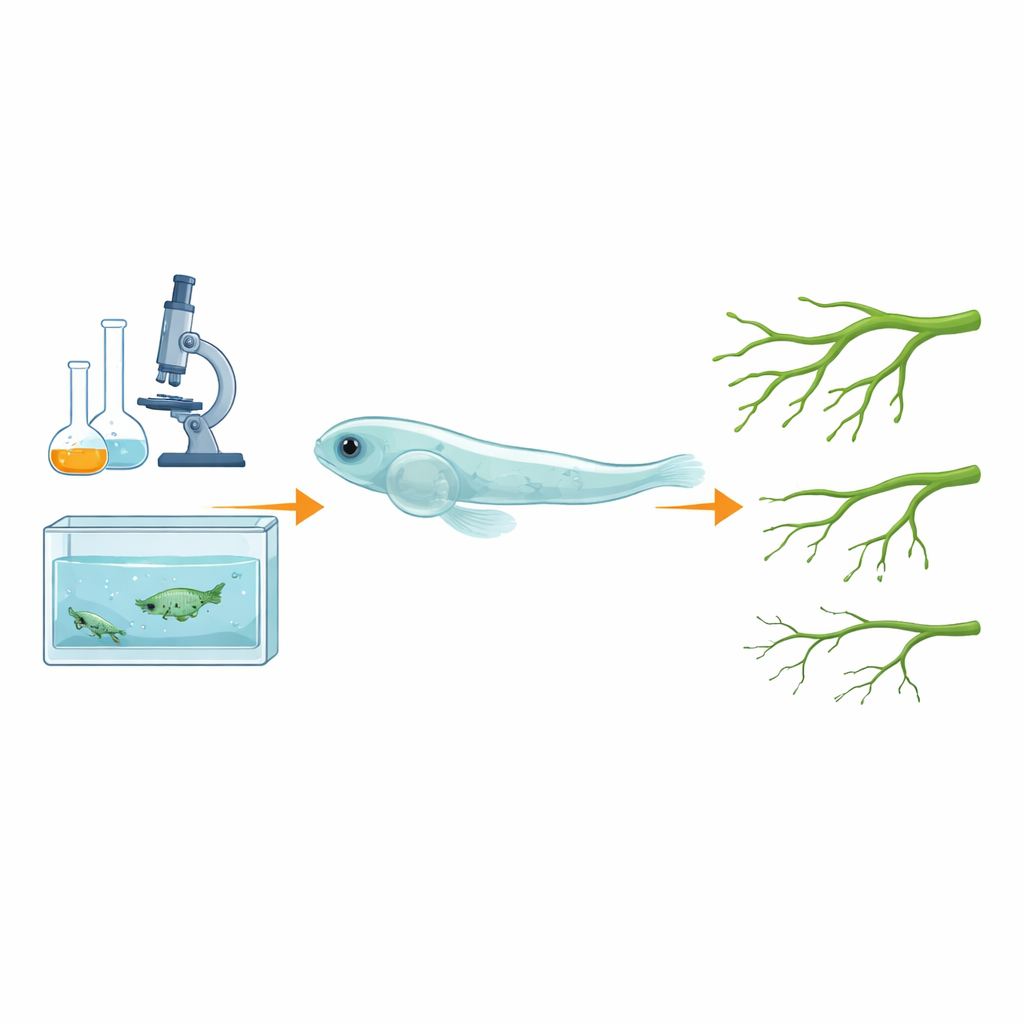
Un nuevo tipo de muerte celular bajo el microscopio
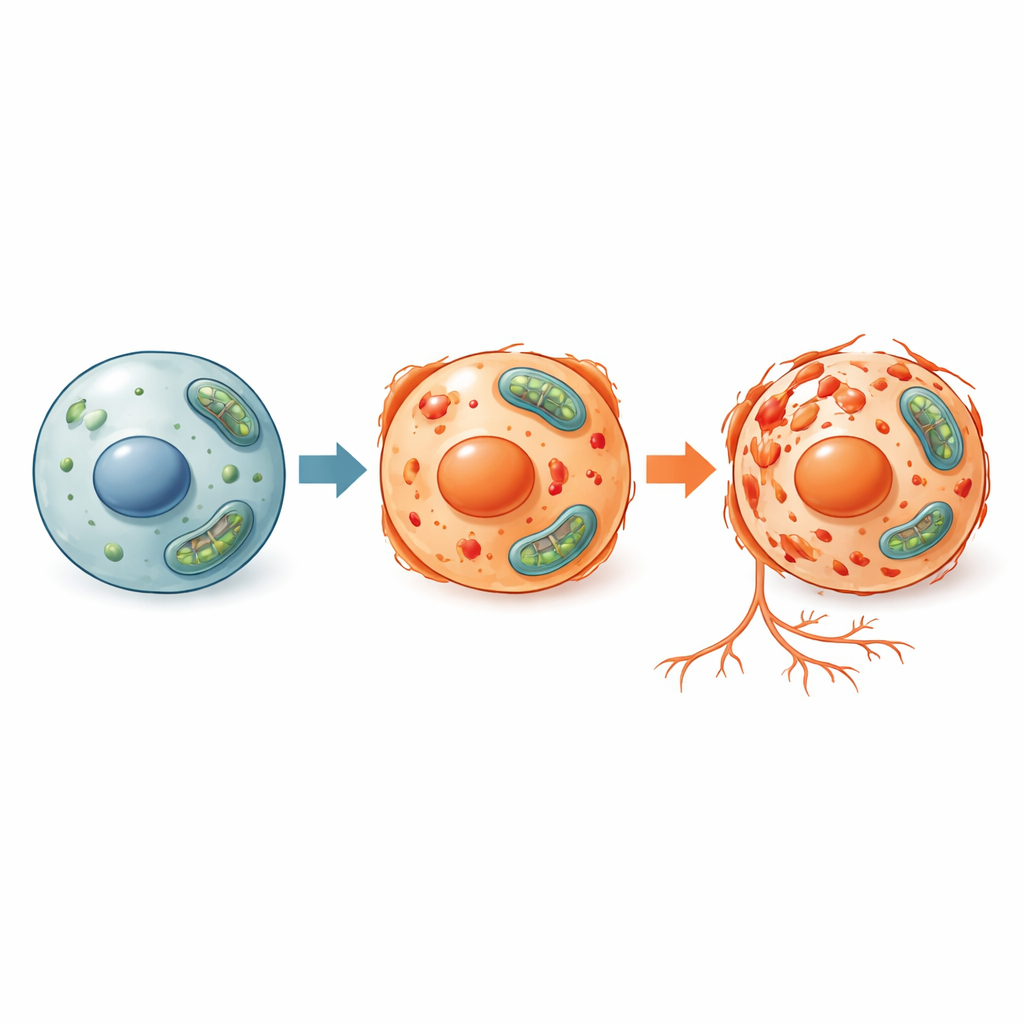
La ferroptosis difiere de formas más conocidas de muerte celular, como la apoptosis (una autodestrucción ordenada y programada) y la necrosis (un colapso más caótico). En la ferroptosis, el hierro y las moléculas reactivas de oxígeno actúan conjuntamente para atacar los lípidos que componen las membranas celulares, provocando finalmente la falla de la célula. Dado que esta vía está estrechamente ligada al manejo del hierro y a las defensas antioxidantes, puede desempeñar un papel clave en condiciones donde se acumula hierro o los tejidos están sometidos a estrés oxidativo, incluyendo algunos tumores, accidentes cerebrovasculares y enfermedades degenerativas. Para estudiar este proceso y probar posibles tratamientos, los investigadores necesitan modelos animales que sean a la vez biológicamente relevantes y experimentalmente flexibles.
Por qué el pez cebra es un sustituto potente para el humano
El pez cebra ofrece varias ventajas como laboratorio vivo. Es un vertebrado con aproximadamente el 85 por ciento de sus genes parecidos a los humanos, y sus rutas de señalización para el crecimiento y la enfermedad son notablemente similares. Sus embriones se desarrollan fuera de la madre y son transparentes, por lo que los científicos pueden observar directamente la formación de órganos, vasos sanguíneos y hueso en tiempo real. Los peces cebra son baratos de criar en gran número, lo que los hace idóneos para probar simultáneamente muchos cambios genéticos o candidatos farmacológicos. La pregunta clave que planteó este estudio fue si las características de la ferroptosis vistas en células de mamífero —daño oxidativo dependiente del hierro, cambios en moléculas protectoras y alteraciones en ciertos genes y proteínas— también aparecen en el pez cebra, y si esto puede distinguirse claramente de otros tipos de muerte celular.
Inducir la ferroptosis en peces cebra vivos
Los investigadores expusieron a ejemplares jóvenes de pez cebra a tres desencadenantes distintos conocidos por provocar ferroptosis: dos inyectores químicos (Erastina y FIN56) y una forma de hierro, el citrato férrico amónico. Midieron varias señales de estrés dentro de los peces, incluido el aumento de especies reactivas de oxígeno, el equilibrio entre un antioxidante clave (glutatión) y su forma oxidada, y la presencia de lípidos dañados. También examinaron qué genes se activaban o silenciaban y midieron los niveles de una proteína protectora central llamada GPX4, que normalmente protege las membranas celulares del ataque oxidativo. En las tres condiciones de tratamiento, las células del pez cebra mostraron la firma esperada de la ferroptosis: más daño oxidativo, un equilibrio antioxidante alterado, reducción de la proteína GPX4 y activación de genes asociados a la ferroptosis. Al mismo tiempo, los marcadores de apoptosis y autophagia cambiaron poco, lo que indica que la muerte celular observada era específicamente ferroptótica.
Cómo la ferroptosis altera los vasos sanguíneos en crecimiento
Para ver cómo este proceso afecta a un sistema orgánico completo, el equipo utilizó una línea transgénica de pez cebra cuyos vasos sanguíneos brillan bajo el microscopio. Cuando estos peces fueron tratados con el inductor de ferroptosis Erastina, los vasos normalmente brillantes y ramificados a lo largo del dorso aparecieron más finos y menos intensos, lo que sugiere un retraso en el crecimiento vascular. Cuando los científicos añadieron fármacos que bloquean la ferroptosis o quelan el exceso de hierro, muchos de estos defectos se mitigaron, lo que implica que la ferroptosis impulsada por el hierro en las células que recubren los vasos estaba afectando directamente el desarrollo vascular. Dado que el crecimiento de los vasos sanguíneos está estrechamente conectado con la formación ósea —una relación conocida como acoplamiento osteogénesis‑angiogénesis— estos hallazgos posicionan al pez cebra como un modelo prometedor no solo para enfermedades vasculares, sino también para trastornos óseos vinculados a la sobrecarga de hierro y al daño oxidativo.
Qué significa esto para la investigación de enfermedades futuras
Al demostrar que la ferroptosis en pez cebra refleja de cerca lo observado en sistemas de mamífero, y que puede inducirse, medirse e incluso revertirse con fármacos específicos, este estudio valida al pez cebra como un modelo práctico y fiable para estudiar la muerte celular impulsada por el hierro. Para el lector general, la conclusión es que estos pequeños peces transparentes pueden ayudar a los científicos a probar con rapidez cómo la ferroptosis contribuye a condiciones como el cáncer, el ictus, las enfermedades vasculares y la osteoporosis, y a detectar tratamientos que puedan proteger los tejidos vulnerables. En resumen, el pez cebra ofrece una forma rápida, visual y genéticamente manejable de investigar una forma destructiva de muerte celular que cada vez se reconoce más como un hilo común en muchas enfermedades humanas.
Cita: Cao, Z., Liu, G., Zhang, R. et al. Validation of ferroptosis in zebrafish as a reliable model for phenotypic studies. Sci Rep 16, 14357 (2026). https://doi.org/10.1038/s41598-026-43493-w
Palabras clave: ferroptosis, pez cebra, estrés oxidativo, angiogénesis, sobrecarga de hierro