Clear Sky Science · pl
Zielona synteza pochodnych 4,4′-diaminotriarylomethanu z użyciem odzyskiwalnego magnetycznego katalizatora kwasowego w nanoskali
Kolorowe cząsteczki o ukrytej roli
Wiele codziennych produktów — od leków przeciwnowotworowych po barwniki tekstylne — opiera się na rodzinie kolorowych związków zwanych triarylomethanami. Ich wytwarzanie zwykle wiąże się z użyciem agresywnych chemikaliów, dużym zużyciem energii i trudnościami z utylizacją odpadów. W artykule opisano czystszy, wielokrotnego użytku „magnetyczny” katalizator, który umożliwia chemikom łagodniejsze konstruowanie ważnych bloków budulcowych triarylomethanów, stosując prosty alkoholowy rozpuszczalnik i umiarkowane ogrzewanie. Praca leży na styku medycyny, nauki o materiałach i zielonej chemii, pokazując, jak inteligentniejsze narzędzia mogą zmniejszać zanieczyszczenia bez utraty wydajności.
Dlaczego te jasne cząsteczki mają znaczenie
Triarylomethany to coś więcej niż ładne barwy. Ich chemiczne rusztowanie występuje w szeregu leków, w tym przeciwnowotworowych, przeciwgrzybiczych, antybiotycznych i przeciwdrgawkowych, a także w wielu barwnikach przemysłowych stosowanych do farbowania włókien, atramentów i elementów optycznych. Ponieważ ta sama podstawowa struktura może być dostrajana, by wchodzić w konkretne interakcje biologiczne lub pochłaniać światło w precyzyjny sposób, chemicy potrzebują niezawodnych dróg do uzyskania wielu wariantów. Tradycyjne metody potrafią dać dobre ilości produktu, ale często polegają na żrących kwasach, toksycznych rozpuszczalnikach lub intensywnym ogrzewaniu. To napięcie — między zapotrzebowaniem na zaawansowane cząsteczki a kosztem środowiskowym ich wytwarzania — napędza poszukiwania bardziej zielonych metod.
Budowa maleńkiego magnetycznego pomocnika
Naukowcy zaprojektowali nowy katalizator stały oparty na nanocząstkach tlenku żelaza, które są naturalnie magnetyczne. Powlekli ten żelazowy rdzeń małym naturalnym aminokwasem, L-proliną, a następnie wprowadzili silnie kwasowe grupy sulfonowe, tworząc materiał oznaczony jako Fe3O4@L-proline@SO3H. Pod mikroskopem elektronowym cząstki te wyglądają jak prawie kuliste ziarna z cienką organiczną powłoką otaczającą gęste jądro. Badania przy użyciu dyfrakcji rentgenowskiej, pomiarów powierzchni właściwej i badań magnetycznych wykazały, że rdzeń z tlenku żelaza zachowuje swoją strukturę krystaliczną i silną odpowiedź magnetyczną nawet po funkcjonalizacji. Jednocześnie zewnętrzna powłoka dostarcza wielu miejsc kwasowych i porów, w których zachodzić mogą reakcje, łącząc reaktywność kwasu ciekłego z wygodą obsługi proszku stałego.
Synteza „one‑pot” w bardziej zielonym rozpuszczalniku
Mając katalizator, zespół przetestował prosty przepis: zmieszać aldehyd aromatyczny, pochodną dimetyloaniliny, etanol i katalizator magnetyczny, a następnie ogrzewać do około 80 °C. W tych łagodnych warunkach substraty łączą się w jednym etapie, tworząc pochodne 4,4′-diaminotriarylomethanu w przyzwoitych do doskonałych wydajnościach, zwykle między 73% a 92%. Systematyczne testy obejmowały zmiany ilości katalizatora, rozpuszczalnika, temperatury i czasu reakcji. Etanol — stosunkowo łagodny, biodegradowalny rozpuszczalnik — okazał się najlepszym medium, a do standardowego testu potrzebna była jedynie niewielka ilość katalizatora (0,2 g). Eksperymenty kontrolne wykazały, że gołe cząstki tlenku żelaza były znacznie mniej skuteczne, co podkreśla znaczenie starannie zaprojektowanej powłoki zewnętrznej w przyspieszaniu tworzenia wiązań.
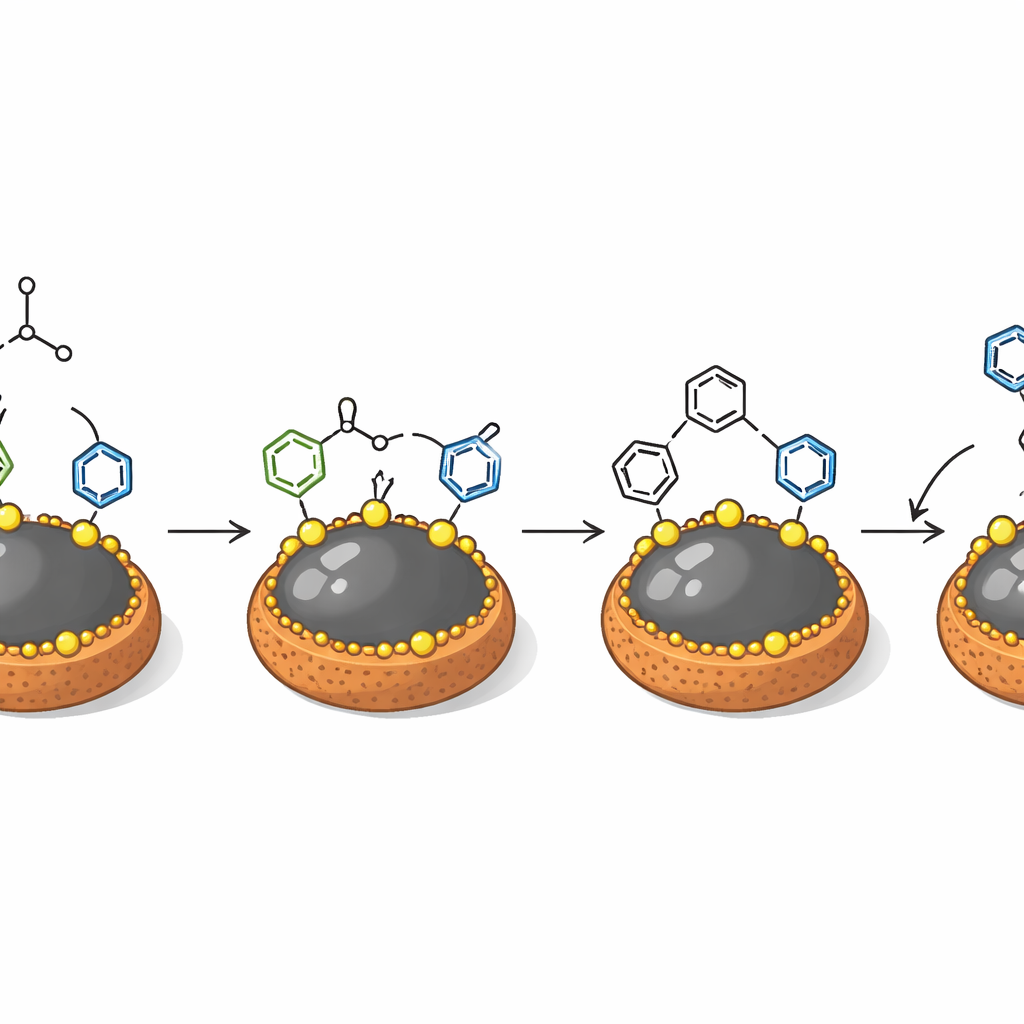
Jak katalizator wykonuje swoją pracę
Na poziomie molekularnym grupy kwasowe na powierzchni nanocząstek aktywują aldehyd, sprawiając, że jego atom węgla staje się bardziej skłonny do tworzenia wiązania. Molekuły dimetyloaniliny atakują następnie to aktywowane miejsce etapami, ostatecznie instalując dwie takie jednostki wokół centralnego atomu węgla i tworząc rdzeń triarylomethanowy. Ponieważ reakcja zachodzi na powierzchni katalizatora, materiał zachowuje się jak prawdziwy stały pomocnik: gdy mieszaninę odfiltrowano na gorąco, usuwając cząstki w połowie przebiegu, tworzenie produktu niemal ustawało. Cząstki można następnie wyciągnąć z reakcji za pomocą prostego magnesu, umyć i użyć ponownie. Przez co najmniej sześć cykli katalizator zachowuje większość swojej wydajności, a krótki zabieg kwasowego płukania może przywrócić powierzchnię utraconą na skutek zablokowania porów.
Odzyskiwalność i wpływ w świecie rzeczywistym
W porównaniu z wieloma wcześniejszymi metodami ten magnetyczny katalizator oferuje atrakcyjne połączenie wydajności i zrównoważenia. Unika silnie żrących kwasów ciekłych i problematycznych rozpuszczalników, stosuje umiarkowane temperatury i znacząco redukuje ilość odpadów dzięki możliwości recyklingu katalizatora wielokrotnie. Zespół także skwantyfikował, ile reakcji może przeprowadzić każde miejsce katalityczne i jak szybko, stwierdzając spójną aktywność dla szerokiego zakresu produktów. W bezpośrednich porównaniach z innymi systemami katalitycznymi z literatury nowy materiał prezentuje się dobrze pod względem wydajności, dodając jednocześnie kluczowe korzyści łatwego oddzielania magnetycznego i ponownego użycia.
Czystsze drogi do koloru i leków
Mówiąc prościej, ta praca pokazuje, że można nadal wytwarzać jasne cząsteczki potrzebne w medycynie i barwnictwie, przy jednoczesnym mniejszym obciążeniu dla środowiska. Dzięki przeniesieniu aktywnej chemii na magnetyczne nanocząstki autorzy stworzyli stałego pomocnika, którego można mieszać w prostej etanolowej mieszaninie, napędzać tworzenie wartościowych bloków budulcowych triarylomethanów, a potem wyciągnąć magnesem i użyć ponownie. Tego typu inteligentny, nadający się do recyklingu katalizator wskazuje drogę do wytwarzania chemikaliów, które zachowują swoje użyteczne kolory i właściwości terapeutyczne, przy znacznie mniejszym śladzie środowiskowym.
Cytowanie: Karamifar, S., Behbahani, F.K. & Keshmirizadeh, E. Green synthesis of 4,4′-diaminotriarylmethane derivatives using a recyclable magnetic acidic nano catalyst. Sci Rep 16, 12800 (2026). https://doi.org/10.1038/s41598-026-42570-4
Słowa kluczowe: zielona chemia, magnetyczny katalizator na nanocząstkach, barwniki triarylomethanowe, odzyskiwalna kataliza, przyjazna dla środowiska synteza