Clear Sky Science · de
Grüne Synthese von 4,4′-Diaminotriarylmethan-Derivaten unter Verwendung eines wiederverwendbaren magnetischen sauren Nanokatalysators
Farbige Moleküle mit versteckter Rolle
Viele Alltagsprodukte – von Krebsmedikamenten bis zu Textilfarbstoffen – beruhen auf einer Familie farbiger Moleküle, den Triarylmethanen. Die Herstellung dieser Verbindungen erfordert meist aggressive Chemikalien, hohen Energieeinsatz und aufwändige Abfallbehandlung. Dieser Aufsatz beschreibt einen saubereren, wiederverwendbaren „magnetischen“ Katalysator, der Chemikerinnen und Chemikern hilft, wichtige Triarylmethan-Bausteine schonender zu synthetisieren, unter Verwendung eines einfachen Alkohols als Lösungsmittel und mäßiger Wärmezufuhr. Die Arbeit liegt an der Schnittstelle von Medizin, Materialwissenschaft und grüner Chemie und zeigt, wie intelligentere Werkzeuge die Umweltbelastung verringern können, ohne die Leistung zu beeinträchtigen.
Warum diese leuchtenden Moleküle wichtig sind
Triarylmethane sind mehr als nur schöne Farben. Ihr chemisches Rückgrat findet sich in einer Reihe von Medikamenten, darunter Antikrebsmittel, Antimykotika, Antibiotika und Antikonvulsiva, sowie in vielen industriellen Farbstoffen zur Einfärbung von Fasern, Tinten und optischen Komponenten. Da das gleiche Grundgerüst so verändert werden kann, dass es mit biologischen Zielen interagiert oder Licht in bestimmten Bereichen absorbiert, benötigen Chemiker zuverlässige Syntheserouten für viele Varianten. Traditionelle Methoden liefern oft gute Ausbeuten, beruhen aber häufig auf ätzenden Säuren, toxischen Lösungsmitteln oder intensiver Erwärmung. Diese Spannung – zwischen dem Bedarf an fortschrittlichen Molekülen und den ökologischen Kosten ihrer Herstellung – treibt die Suche nach umweltfreundlicheren Verfahren an.
Bau eines winzigen magnetischen Helfers
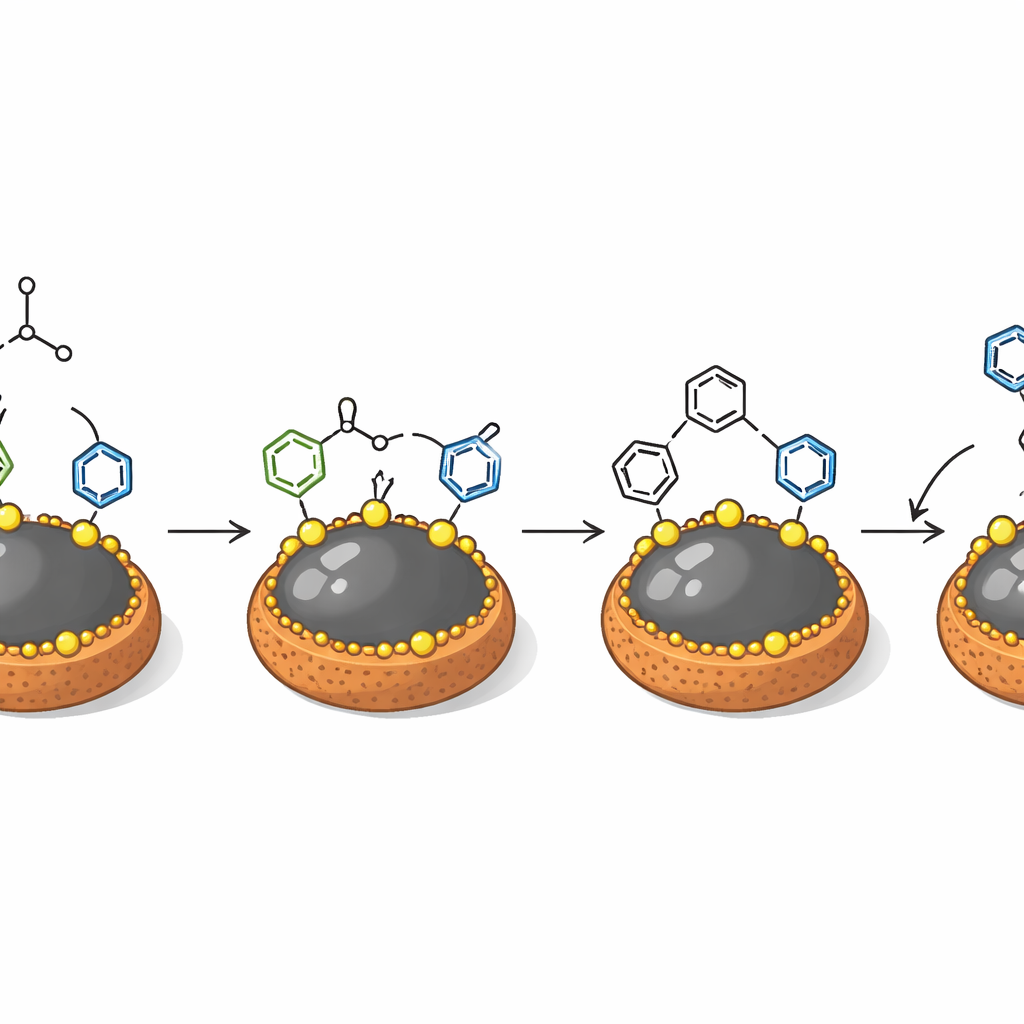
Die Forschenden entwickelten einen neuen Feststoffkatalysator, der auf Eisenoxid-Nanopartikeln basiert, die von Natur aus magnetisch sind. Sie beschichteten diesen Eisenkern mit einer kleinen natürlichen Aminosäure, L‑Prolin, und fügten anschließend stark saure Sulfongruppen hinzu, wodurch ein Material entstand, das als Fe3O4@L-proline@SO3H bezeichnet wird. Unter einem Elektronenmikroskop erscheinen diese Partikel als annähernd kugelförmige Körnchen mit einer dünnen organischen Schale um einen dichten Kern. Untersuchungen mittels Röntgenbeugung, Messungen der Oberfläche und magnetischer Studien zeigten, dass der Eisenoxidkern seine Kristallstruktur und starke magnetische Reaktion auch nach der Funktionalisierung behält. Gleichzeitig bietet die äußere Schicht viele saure Stellen und Poren, in denen Reaktionen stattfinden können, und verbindet so die Reaktivität einer flüssigen Säure mit der einfachen Handhabung eines festen Pulvers.
One-Pot-Chemie in einem grüneren Lösungsmittel
Mit dem Katalysator in der Hand untersuchte das Team ein einfaches Rezept: ein aromatisches Aldehyd, ein Dimethylanilin-Derivat, Ethanol und den magnetischen Katalysator mischen und dann auf etwa 80 °C erhitzen. Unter diesen milden Bedingungen reagieren die Ausgangsstoffe in einem einzigen Schritt zu 4,4′-Diaminotriarylmethan-Derivaten in ordentlichen bis ausgezeichneten Ausbeuten, typischerweise zwischen 73 % und 92 %. Systematische Tests variierten die Menge des Katalysators, das Lösungsmittel, die Temperatur und die Reaktionszeit. Ethanol – ein vergleichsweise unbedenkliches, biologisch abbaubares Lösungsmittel – erwies sich als das beste Medium, und nur eine moderate Menge Katalysator (0,2 g im Standardversuch) war erforderlich. Kontrollexperimente zeigten, dass unbeschichtete Eisenoxidpartikel deutlich weniger wirksam waren, was die Bedeutung der sorgfältig gestalteten äußeren Schicht für die Beschleunigung der Bindungsbildung unterstreicht.
Wie der Katalysator seine Arbeit verrichtet
Auf molekularer Ebene aktivieren die sauren Gruppen an der Nanopartikeloberfläche das Aldehyd, indem sie das zentrale Kohlenstoffatom reaktiver machen. Dimethylanilin-Moleküle greifen dann schrittweise diese aktivierte Stelle an und setzen schließlich zwei solche Einheiten um das zentrale Kohlenstoffatom herum ein, wodurch das Triarylmethan-Grundgerüst entsteht. Da die Reaktion an der Katalysatoroberfläche abläuft, verhält sich das Material wie ein echter Feststoffhelfer: Wird das Gemisch zur Hälfte der Reaktion heiß filtriert, um die Partikel zu entfernen, kommt die Produktbildung nahezu zum Stillstand. Die Partikel lassen sich anschließend mit einem einfachen Magneten aus dem Reaktionsgemisch abziehen, waschen und wiederverwenden. Über mindestens sechs Zyklen behält der Katalysator den Großteil seiner Leistung, und eine kurze Säurewäsche kann die durch Porenverstopfung verlorene Oberfläche wiederherstellen.
Wiederverwendbarkeit und Auswirkungen in der Praxis
Im Vergleich zu vielen früheren Verfahren bietet dieser magnetische Katalysator eine überzeugende Balance aus Effizienz und Nachhaltigkeit. Er vermeidet stark korrosive Flüssigsäuren und problematische Lösungsmittel, arbeitet bei moderaten Temperaturen und reduziert Abfall deutlich, da der Katalysator mehrfach recycelt werden kann. Das Team quantifizierte außerdem, wie viele Reaktionen jede katalytische Stelle durchführen kann und wie schnell, und fand eine konsistente Aktivität über ein breites Produktspektrum. Bei direkten Vergleichen mit anderen in der Literatur beschriebenen Katalysatorsystemen schneidet das neue Material in Bezug auf Ausbeute gut ab und bringt die entscheidenden Vorteile einfacher magnetischer Trennung und Wiederverwendung mit.
Sauberere Wege zu Farbe und Medizin
Alltäglich gesagt zeigt diese Arbeit, dass wir die leuchtenden Moleküle für Medikamente und Farbstoffe weiterhin herstellen können, dabei jedoch umweltfreundlicher vorgehen. Indem die aktive Chemie auf magnetische Nanopartikel verlagert wird, schufen die Autorinnen und Autoren einen festen Helfer, der in eine einfache Ethanollösung eingerührt werden kann, die Bildung wertvoller Triarylmethan-Bausteine antreibt und sich anschließend mit einem Magnet herausziehen und erneut verwenden lässt. Solch ein intelligenter, wiederverwendbarer Katalysator weist den Weg zu einer chemischen Produktion, die ihre nützlichen Farben und therapeutischen Eigenschaften bewahrt, aber mit deutlich kleinerer Umweltbilanz.
Zitation: Karamifar, S., Behbahani, F.K. & Keshmirizadeh, E. Green synthesis of 4,4′-diaminotriarylmethane derivatives using a recyclable magnetic acidic nano catalyst. Sci Rep 16, 12800 (2026). https://doi.org/10.1038/s41598-026-42570-4
Schlüsselwörter: grüne Chemie, magnetischer Nanopartikel-Katalysator, Triarylmethan-Farbstoffe, wiederverwendbare Katalyse, umweltfreundliche Synthese