Clear Sky Science · pl
Ryzyko genetyczne w chorobie Alzheimera
Dlaczego nasze geny mają znaczenie dla utraty pamięci
Choroba Alzheimera bywa postrzegana jako pech lub naturalna część procesu starzenia, jednak dekady badań pokazują, że geny odgrywają kluczową rolę w tym, kto zachoruje i kiedy. Ten artykuł przeglądowy zbiera najnowsze odkrycia dotyczące genetycznego ryzyka Alzheimera, wyjaśnia, dlaczego kobiety są dotknięte inaczej niż mężczyźni, oraz opisuje, jak współczesne narzędzia komputerowe mogą przekształcić tysiące drobnych różnic w DNA w wczesne wskaźniki ostrzegawcze. Dla rodzin zaniepokojonych otępieniem, praca ta wskazuje drogę ku przyszłości, w której ryzyko będzie można oszacować dokładniej, a terapie dopasować do indywidualnego pacjenta.
Wiele drobnych genetycznych pchnięć w kierunku choroby
Autorzy najpierw wyjaśniają, że choroba Alzheimera ma silny składnik dziedziczny — geny mogą odpowiadać nawet za cztery piąte ryzyka. Kilka rzadkich zmian genetycznych może niemal zagwarantować wczesne, agresywne postępowanie choroby, ale u większości ludzi zagrożenie wynika z łącznego działania wielu powszechnych wariantów DNA, z których każdy ma tylko niewielki wpływ. Ogromne międzynarodowe badania przesiewowe całego genomu odkryły już ponad 100 takich miejsc ryzyka. Niektóre z nich znajdują się w dobrze znanych genach, takich jak APOE, TREM2 i ABCA7, które biorą udział w usuwaniu lepkich fragmentów białek, kontrolowaniu stanu zapalnego w mózgu albo gospodarce tłuszczami i cholesterolem. Inne leżą w odcinkach DNA niekodujących białek, co utrudnia zrozumienie ich działania. Nowe badania komórek odpornościowych mózgu, zwanych mikroglejem, zaczynają pokazywać, że niektóre z tych „cichych” zmian modyfikują aktywność pobliskich genów i sposób, w jaki komórki reagują na wczesne uszkodzenia.
Nie jedna Alzheimerowska choroba, lecz wiele odmian
Coraz bardziej jasne staje się, że Alzheimera nie należy traktować jako jednej choroby, lecz rodziny powiązanych zaburzeń mózgu. Przegląd opisuje badania grupujące pacjentów w podtypy na podstawie białek w płynie mózgowo‑rdzeniowym. Jeden podtyp wykazuje objawy nadmiernego wzrostu komórek nerwowych, inny nadaktywnego układu odpornościowego, a kolejne wskazują na problemy z barierą krew–mózg lub systemami oczyszczania mózgu. Każdy schemat wiąże się z innym zestawem genów ryzyka, co sugeruje, że ludzie dochodzą do utraty pamięci różnymi drogami biologicznymi. Autorzy zwracają też uwagę na istotne różnice między grupami rasowymi i etnicznymi w tym, jak kluczowe warianty genowe, zwłaszcza APOE, kształtują ryzyko, oraz jak inne cechy odziedziczone, takie jak ciśnienie krwi i poziom cholesterolu, mogą przybliżać lub oddalać osoby od choroby.
Jak płeć wpływa na ryzyko genetyczne
Głównym wątkiem artykułu jest to, że kobiety i mężczyźni nie dzielą tej samej mapy genetycznej dotyczącej Alzheimera. Kobiety nie tylko chorują częściej, lecz także wydają się szybciej przechodzić przez szkodliwe procesy komórkowe, gdy zmiany w mózgu się pojawiają. Badania pojedynczych komórek mózgowych pokazują, że u kobiet komórki odpornościowe i komórki wspierające są silniej aktywowane, podczas gdy niektóre neurony u mężczyzn i kobiet mogą reagować nawet w przeciwne strony na tę samą patologię. Gdy badacze tworzą osobne wskaźniki genetycznego ryzyka dla każdej płci, okazuje się, że niektóre warianty DNA mają większe znaczenie u kobiet, a inne u mężczyzn, a wskaźniki dopasowane do płci lepiej przewidują wiek wystąpienia choroby i gromadzenie się białek związanych z chorobą. Metody uczenia maszynowego trenowane na dużych zbiorach genetycznych dodatkowo ujawniają geny specyficzne dla płci powiązane z naprawą DNA, podziałem komórek, reakcjami na stres i innymi procesami, które mogą pomagać wyjaśnić wyższe obciążenie chorobą u kobiet.
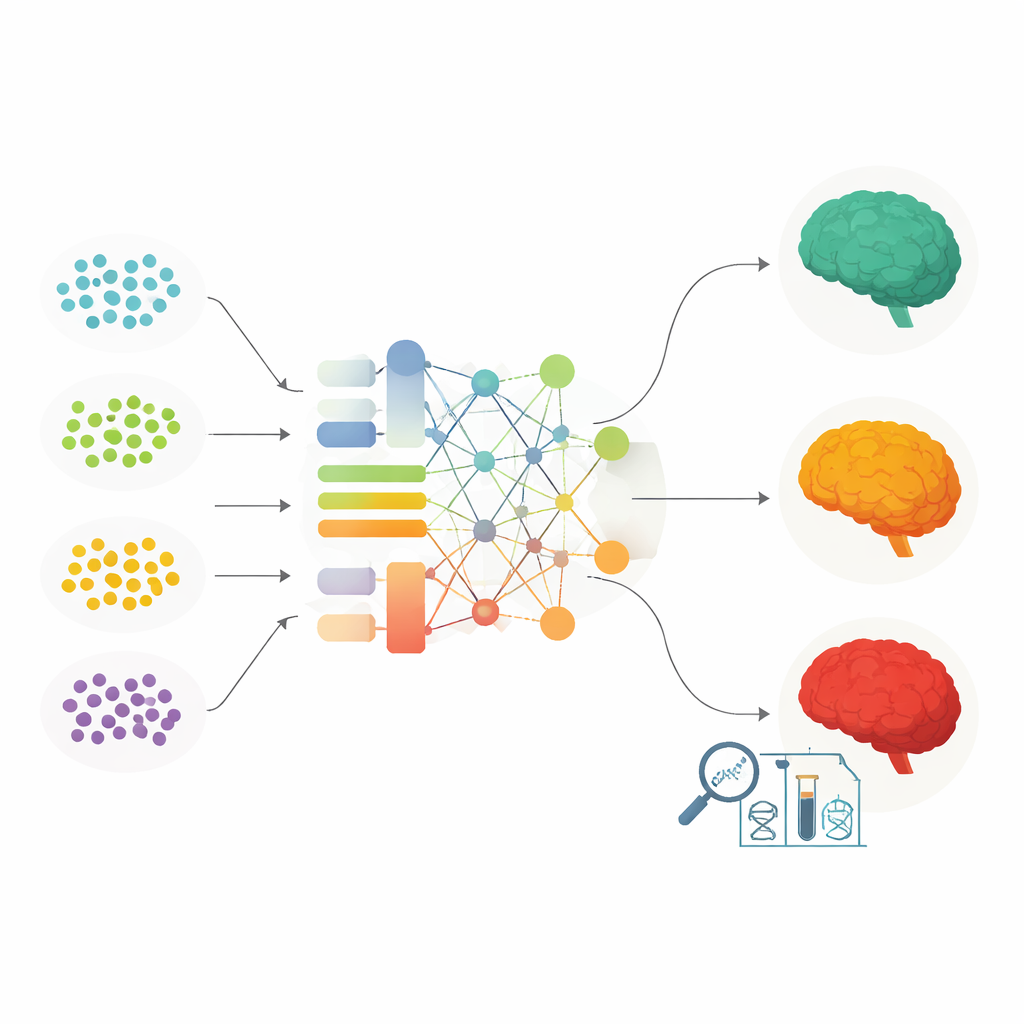
Od list genów do osobistych wskaźników ryzyka
Aby przekształcić wszystkie te informacje w coś potencjalnie użytecznego w praktyce klinicznej, naukowcy stosują poligeniczne wskaźniki ryzyka. Wskaźniki te sumują łączny wpływ wielu wariantów ryzyka w całym genomie, czasem nadając dodatkową wagę szczególnie istotnym regionom, takim jak APOE. Przegląd opisuje różne sposoby budowy tych wskaźników i pokazuje, że ostrożnie dostrojone wersje potrafią odróżnić osoby, które rozwiną chorobę Alzheimera lub przejdą z łagodnych zaburzeń pamięci do pełnego otępienia. Nowocześniejsze podejścia wykorzystują algorytmy uczenia maszynowego, które potrafią uchwycić złożone interakcje między wariantami, a nawet łączyć dane genetyczne ze skanami mózgu i markerami we krwi. Modele te na ogół przewyższają tradycyjne wskaźniki, także wśród osób o różnych wariantach APOE, i potrafią wskazać, które szlaki biologiczne są najważniejsze dla predykcji.
Co to znaczy dla przyszłych pacjentów
Podsumowując, artykuł stwierdza, że genetyka daje potężne narzędzie do określenia, kto jest narażony na chorobę Alzheimera, dlaczego to ryzyko różni się w zależności od płci i pochodzenia oraz które systemy biologiczne mogą być najlepszymi celami terapeutycznymi. Jednocześnie obecne wskaźniki ryzyka najlepiej działają u osób pochodzenia europejskiego i nie są jeszcze gotowe do rutynowego przesiewania. Autorzy argumentują, że potrzebne są większe i bardziej zróżnicowane badania genetyczne, głębsze eksperymenty wyjaśniające, jak niekodujące zmiany DNA wpływają na komórki, oraz bardziej przejrzyste modele uczenia maszynowego, zanim predykcja genetyczna będzie mogła bezpiecznie kierować zapobieganiem lub terapią. Jeśli te wyzwania zostaną sprostane, przyszli pacjenci mogą otrzymywać spersonalizowane oceny ryzyka łączące geny, płeć, pochodzenie i biomarkery, co otworzy drogę do wcześniejszej diagnozy i precyzyjniej dopasowanych interwencji.
Cytowanie: Pan, Y., Cho, H., Lou, Q. et al. Genetic risk in Alzheimer’s disease. npj Syst Biol Appl 12, 39 (2026). https://doi.org/10.1038/s41540-026-00665-8
Słowa kluczowe: Genetyka choroby Alzheimera, poligeniczny wskaźnik ryzyka, uczenie maszynowe, różnice płci, medycyna precyzyjna