Clear Sky Science · ar
المخاطر الوراثية في مرض ألزهايمر
لماذا تهمّ جيناتنا عند فقدان الذاكرة
غالبًا ما يُنظر إلى مرض ألزهايمر على أنه حظ سيئ أو جزء طبيعي من التقدم في العمر، لكن عقودًا من البحث تُظهر أن جيناتنا تلعب دورًا رئيسيًا في من يصاب بالمرض ومتى يحدث ذلك. تجمع هذه المراجعة أحدث الاكتشافات حول المخاطر الوراثية لألزهايمر، ولماذا تتأثر النساء بشكل مختلف عن الرجال، وكيف يمكن للأدوات الحاسوبية الحديثة تحويل آلاف الاختلافات الصغيرة في الحمض النووي إلى درجات إنذار مبكر. بالنسبة للعائلات القلقة بشأن الخرف، يشير هذا العمل إلى مستقبل يمكن فيه تقدير الخطر بدقة أكبر وتكييف العلاجات مع الفرد.
العديد من الدفعات الجينية الصغيرة نحو المرض
يشرح المؤلفون أولاً أن مرض ألزهايمر له مكوّن وراثي قوي، حيث تسهم الجينات بما يصل إلى أربعة أخماس الخطر. يمكن أن تضمن بعض التغيرات الجينية النادرة تقريبًا حدوث مرض مبكر وشديد، لكن خطر معظم الأشخاص ينشأ من التأثير المشترك للعديد من المتغيرات الشائعة في الحمض النووي، كل منها ذو أثر صغير فقط. كشفت دراسات دولية ضخمة تفحص الجينوم بأكمله الآن عن أكثر من 100 من هذه المواقع المرتبطة بالخطر. يقع بعضها في جينات معروفة مثل APOE وTREM2 وABCA7، التي تشارك في إزالة بقايا البروتين اللزجة، والتحكم في الالتهاب في الدماغ، أو معالجة الدهون والكوليسترول. وتقع أخرى في مقاطع من الحمض النووي لا تُشفّر بروتينات، مما يجعل من الصعب معرفة كيفية عملها. تُظهر أعمال جديدة على خلايا الجهاز المناعي الدماغي المسماة بالخلايا البلعمية الصغيرة (microglia) أن بعض هذه التغيرات "الصامتة" تعدّل نشاط الجينات القريبة وطريقة استجابة الخلايا للضرر المبكر.
ليس ألزهايمر واحدًا بل أصناف متعددة
بدلًا من كونه مرضًا واحدًا، يبدو ألزهايمر بشكل متزايد كعائلة من الاضطرابات الدماغية ذات الصلة. تصف المراجعة دراسات تُصنّف المرضى إلى أنواع فرعية بناءً على البروتينات الموجودة في سائل النخاع الشوكي. يظهر أحد الأنواع فرط نشاط في نمو الخلايا العصبية، وآخر علامة على جهاز مناعي مفرط النشاط، بينما تشير أنواع أخرى إلى مشاكل في الحاجز الدموي الدماغي أو في أنظمة تنظيف المخ من المخلفات. يتوافق كل نمط مع مجموعة مختلفة من جينات الخطر، مما يوحي بأن الأشخاص يصلون إلى فقدان الذاكرة عبر مسارات بيولوجية مميزة. كما يبرز المؤلفون فروقًا مهمة بين المجموعات العرقية والإثنية في كيفية تشكيل المتغيرات الجينية الرئيسية، وخصوصًا APOE، للخطر، وكيف أن صفات وراثية أخرى مثل ضغط الدم والكوليسترول يمكن أن تدفع الأشخاص أقرب إلى المرض أو أبعد عنه.
كيف يشكّل الجنس المخاطر الوراثية
موضوع رئيسي في المقال هو أن النساء والرجال لا يشتركون في نفس المشهد الوراثي لألزهايمر. فالنساء لا يُصبن بالمرض أكثر فحسب، بل يبدو أنهن أيضًا ينتقلن بشكل أسرع عبر المسارات الخلوية الضارة بمجرد أن تبدأ التغيرات الدماغية. تُظهر دراسات للخلايا الدماغية الفردية أن الخلايا المناعية والخلايا الداعمة في النساء أكثر نشاطًا، بينما قد تستجيب بعض الخلايا العصبية لدى الرجال والنساء باتجاهين متعاكسين لنفس المَرَضية. عندما يبني الباحثون درجات المخاطر الوراثية منفصلة لكل جنس، يجدون أن بعض المتغيرات في الحمض النووي لها أهمية أكبر عند النساء وآخرى عند الرجال، وأن الدرجات المطابقة للجنس تتنبأ بشكل أفضل بعمر البداية وتراكم البروتينات المرتبطة بالمرض. تكشف طرق التعلّم الآلي المدربة على مجموعات بيانات جينية كبيرة أيضًا عن جينات مرتبطة بالجنس تتعلق بإصلاح الحمض النووي، والانقسام الخلوي، واستجابات الإجهاد، وغيرها من العمليات التي قد تفسر العبء الأعلى للمرض لدى النساء.
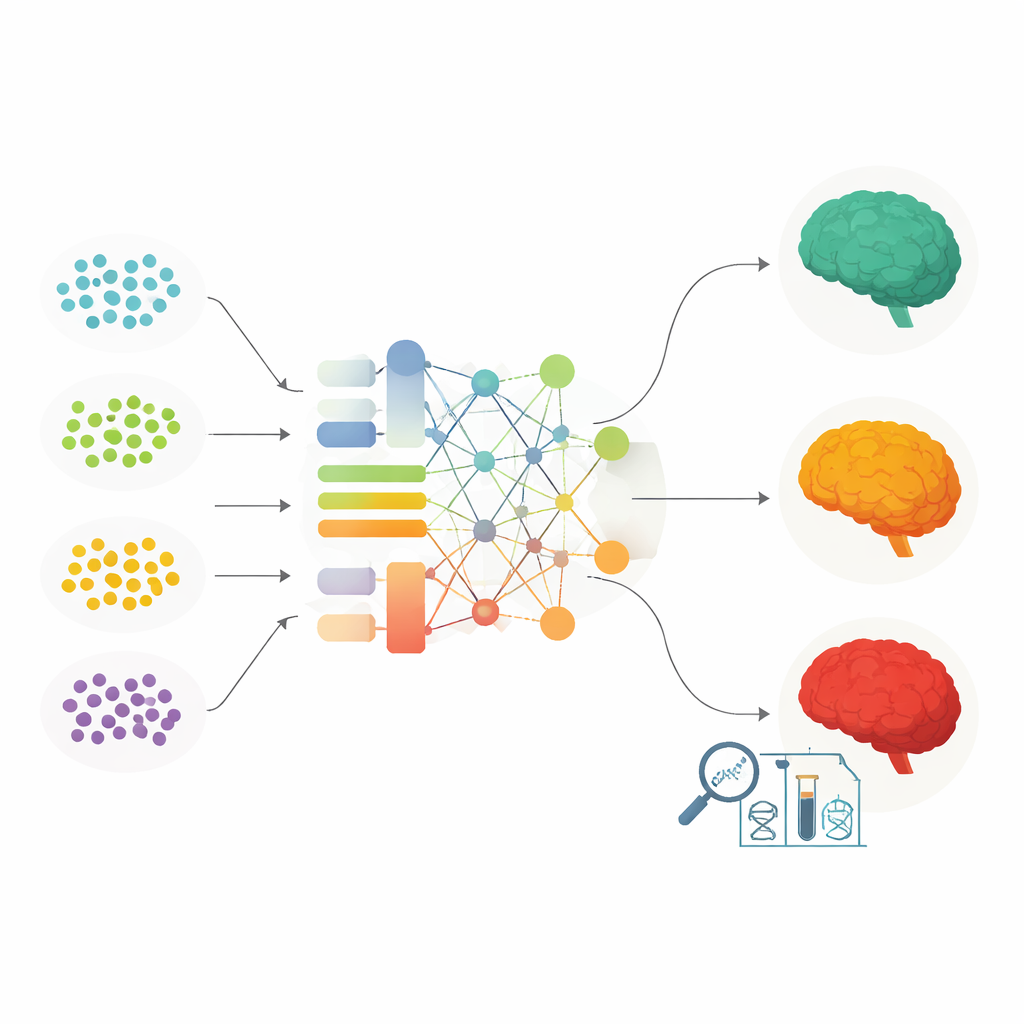
من قوائم الجينات إلى درجات المخاطر الشخصية
لجعل كل هذه المعلومات مفيدة محتملة في العيادة، يستخدم العلماء درجات المخاطر متعددة الجينات. تجمع هذه الدرجات الدفع المشترك للعديد من متغيرات الخطر عبر الجينوم، مع إعطاء وزن إضافي أحيانًا لمناطق مهمة مثل APOE. تستعرض المراجعة طرقًا مختلفة لبناء هذه الدرجات وتبيّن أن النسخ المولفة بعناية يمكن أن تميّز الأشخاص الذين سيتطوّر لديهم ألزهايمر أو ينتقلون من مشاكل ذاكرة خفيفة إلى خرف كامل. تستخدم الأساليب الأحدث خوارزميات التعلّم الآلي التي تستطيع التقاط التفاعلات المعقّدة بين المتغيرات، وحتى مزج البيانات الجينية مع صور الدماغ وعلامات الدم. تتفوق هذه النماذج عمومًا على الدرجات التقليدية، بما في ذلك لدى الأشخاص ذوي خلفيات APOE المختلفة، ويمكن أن تبرز أي المسارات البيولوجية هي الأكثر أهمية للتنبؤ.
ما الذي يعنيه هذا لمرضى المستقبل
خلاصة القول في المقال أن الوراثة توفر نافذة قوية لفهم من هم الأكثر عرضة لخطر ألزهايمر، ولماذا يختلف هذا الخطر بحسب الجنس والأصل، وأي الأنظمة البيولوجية قد تكون أفضل أهداف للعلاج. وفي الوقت نفسه، تعمل درجات المخاطر الحالية بشكل أفضل لدى الأشخاص ذوي الأصل الأوروبي وليست جاهزة بعد للفحص الروتيني. يرى المؤلفون أن دراسات وراثية أكبر وأكثر تنوعًا، وتجارب أعمق لفهم كيف تؤثر تغييرات الحمض النووي غير المرمّزة على الخلايا، ونماذج تعلّم آلي أكثر شفافية، كلها عوامل لازمة قبل أن يمكن للتنبؤ الوراثي أن يرشِد الوقاية أو العلاج بأمان. إذا تم تلبية هذه التحديات، فقد يتلقى مرضى المستقبل تقديرات مخاطر شخصية تجمع بين الجينات والجنس والأصل والبيوماركرز، ما يفتح الباب للتشخيص المبكر وتدخلات مصممة بدقة أكبر.
الاستشهاد: Pan, Y., Cho, H., Lou, Q. et al. Genetic risk in Alzheimer’s disease. npj Syst Biol Appl 12, 39 (2026). https://doi.org/10.1038/s41540-026-00665-8
الكلمات المفتاحية: وراثة ألزهايمر, مجموع المخاطر متعددة الجينات, التعلّم الآلي, الفروقات بين الجنسين, الطب الدقيق