Clear Sky Science · pl
Synteza sializowanych oligosacharydów mleka ludzkiego za pomocą zautomatyzowanego montażu glikanów
Dlaczego lepsze cukry mleczne są istotne
Mleko matki zawiera bogatą mieszaninę złożonych cukrów, które kształtują florę jelitową niemowlęcia, jego układ odpornościowy i odporność na infekcje. Wśród najważniejszych są sializowane oligosacharydy mleka ludzkiego — rozgałęzione łańcuchy cukrowe zakończone specjalnym cukrem zwanym kwasem sjalowym. Naukowcy chcieliby badać każdy z tych związków szczegółowo, a nawet przekształcać je w leki lub testy diagnostyczne, lecz wyizolowanie czystych próbek z mleka jest niezwykle trudne. W tym badaniu opisano sposób szybkiego i precyzyjnego konstruowania tych skomplikowanych cukrów mlecznych przy użyciu zautomatyzowanej maszyny do budowy cukrów.
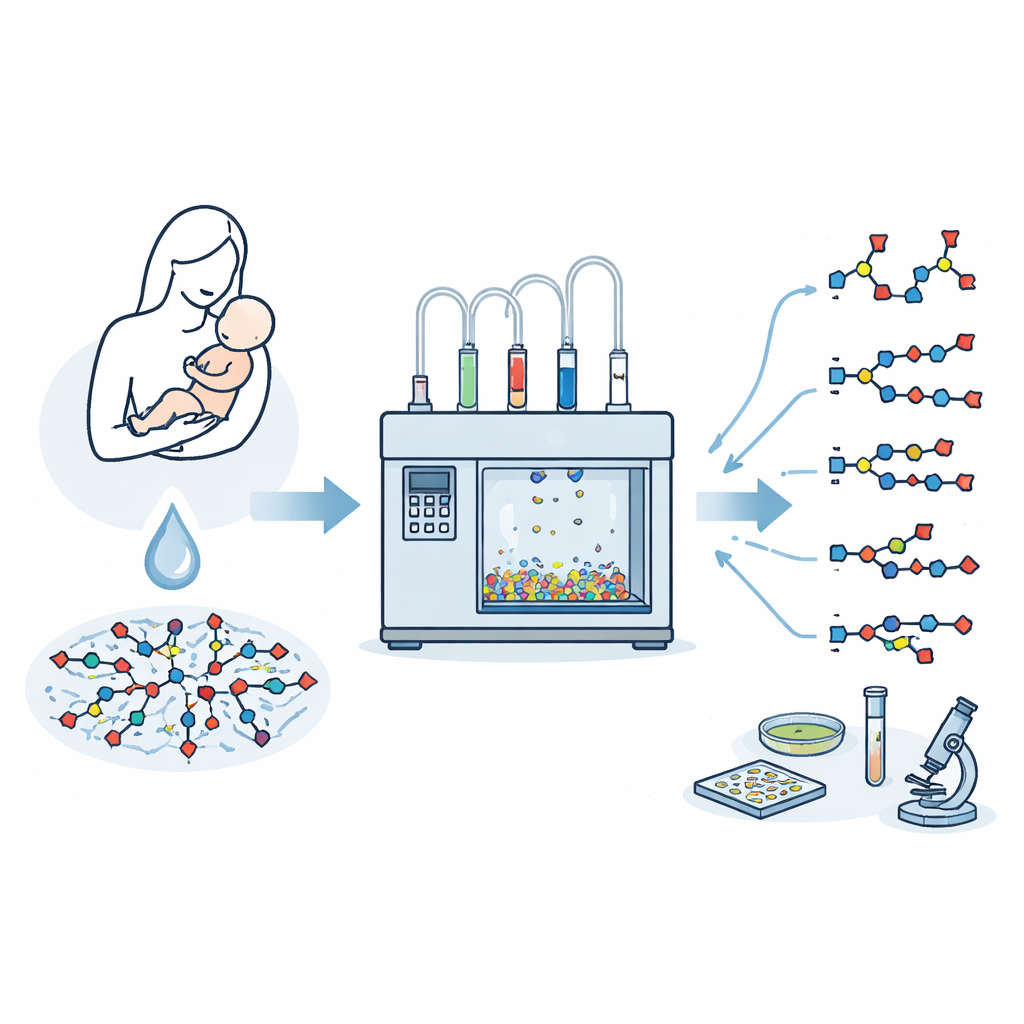
Specjalne cukry na końcach łańcuchów
Kwas sjalowy znajduje się na końcach wielu łańcuchów cukrowych na powierzchniach komórek, gdzie odgrywa kluczowe role w komunikacji między komórkami, obronie odpornościowej oraz tym, jak wirusy i bakterie przyczepiają się do naszych tkanek. W mleku matki około jedna na pięć znanych oligosacharydów zawiera kwas sjalowy. Te sializowane struktury wiązane są z korzyściami, takimi jak ochrona przed chorobami jelit u wcześniaków oraz pełnienie roli „przynęty”, która wiąże wirusy grypy. Jednak natura dostarcza ich tylko w śladowych ilościach, zmieszanych w złożonym roztworze, dlatego badacze potrzebują wydajnych metod syntezy, aby otrzymać miligramowe do gramowych ilości pojedynczych, dobrze zdefiniowanych struktur.
Przekształcenie składania cukrów w proces maszynowy
Zautomatyzowany montaż glikanów to technologia, która łączy proste cegiełki cukrowe na maleńkich żywicznych kulkach, krok po kroku, pod kontrolą komputera. Unika mozolnej oczyszczania po każdym etapie i potrafi skondensować syntezy, które kiedyś trwały miesiącami, do dni. Jednak przyłączanie kwasu sjalowego do rosnącego łańcucha na stałym nośniku było od dawna problemem. Kształt i ładunek kwasu sjalowego sprzyjają niepożądanej reakcji rozkładu zamiast tworzenia pożądanego wiązania, a kontrola nad stereochemią (trójwymiarowym „ukierunkowaniem”) nowego wiązania jest trudna. Wcześniejsze prace polegały albo na gotowych dwu-cukrowych blokach dostosowanych do konkretnego celu, albo działały tylko dla bardzo krótkich łańcuchów.
Nowa klasa „zamkniętych” bloków kwasu sjalowego
Autorzy przyjęli i zaadaptowali sprytny pomysł: makrobicykliczne donorzy kwasu sjalowego. W tych cegiełkach mały chemiczny łącznik łączy różne części kwasu sjalowego, tworząc sztywną, klatkową strukturę. To ograniczenie kieruje nadchodzący łańcuch cukrowy tak, by atakował z właściwej strony, zwiększając pożądany wynik stereochemiczny i jednocześnie tłumiąc ścieżkę rozkładu. Zespół systematycznie optymalizował, jak zachowują się ci donorzy na stałym nośniku — dostrajając mieszanki rozpuszczalników, ilość dodawanego donora, temperaturę i konstrukcję nadchodzących jednostek cukrowych. Odkryli, że umiarkowanie reaktywne donory radzą sobie lepiej na zatłoczonym żywicu niż wysoce reaktywne, oraz że odsłonięcie niektórych pozycji na cukrze-akceptorze podczas reakcji może zmniejszyć zatłoczenie i poprawić wydajności.
Budowanie biblioteki złożonych cukrów mlecznych
Wyposażeni w te warunki, badacze zmontowali dziewięć różnych sializowanych oligosacharydów mleka ludzkiego o różnej wielkości i rozgałęzieniu, w tym cząsteczki ozdobione nie tylko kwasem sjalowym, ale też innym ważnym cukrem — fukozą. Najważniejszym osiągnięciem jest udana zautomatyzowana synteza DSLNF II, silnie rozgałęzionego, fukozylowanego i dysialylowanego łańcucha siedmiocukrowego, który opierał się metodom enzymatycznym i wcześniej wymagał skomplikowanej, ręcznie prowadzonej syntezy całkowitej. Po drodze zespół wykrył, że subtelne zmiany daleko od miejsca reakcji — na przykład zamiana jednego typu tymczasowej grupy ochronnej na inny na odległym cukrze — mogą dramatycznie przyspieszyć lub spowolnić przyłączanie kwasu sjalowego.
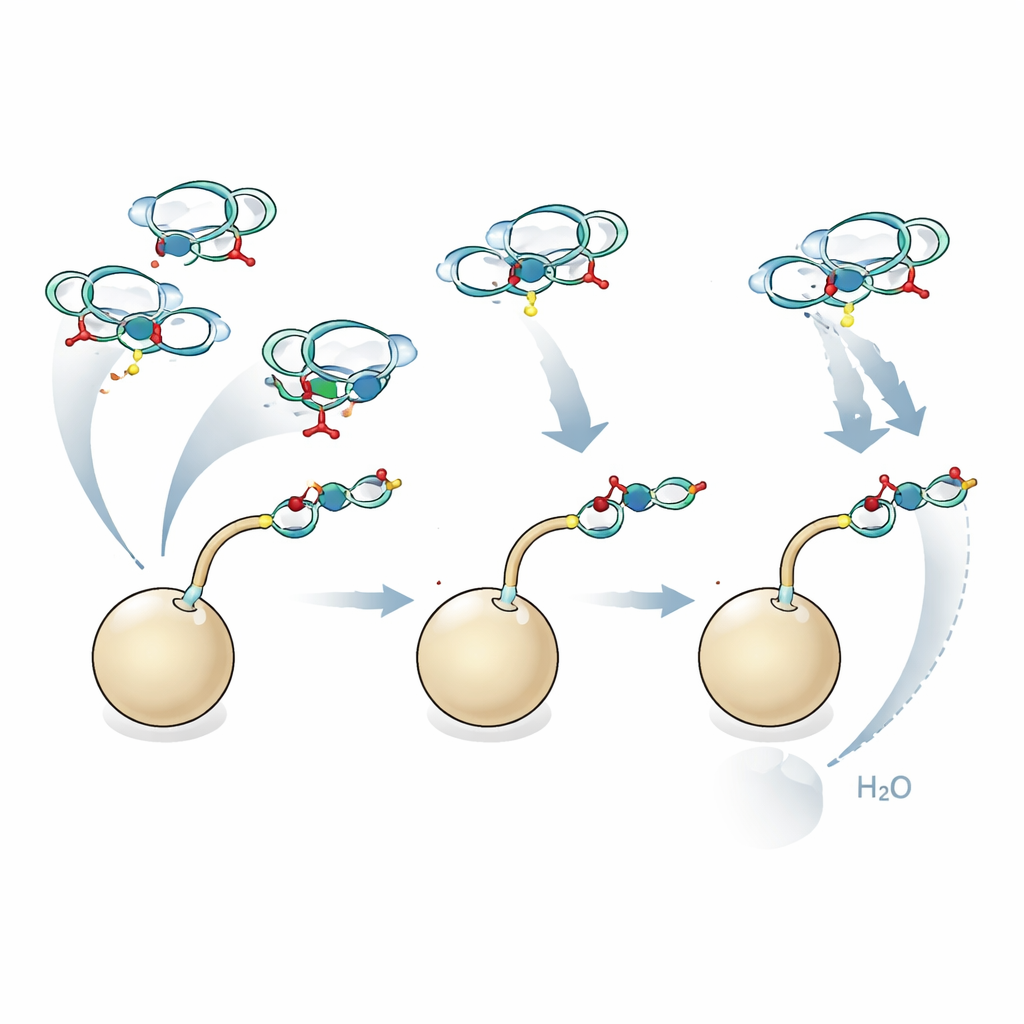
Od chronionych łańcuchów do gotowych narzędzi
Ponieważ zautomatyzowany montaż polega na grupach ochronnych, by kontrolować które pozycje reagują, produkty końcowe początkowo noszą wiele tymczasowych masek chemicznych. Usunięcie ich wszystkich bez uszkodzenia wrażliwych wiązań kwasu sjalowego i fukozy jest wyzwaniem. Autorzy opracowali delikatną, stopniową sekwencję deprotekcji zaczynającą od redukcji cynkowo-miedzianej, następnie kontrolowanej acetylacji, łagodnego traktowania zasadą, a w końcu hydrogenacji. Ten protokół konsekwentnie dawał czyste, w pełni odmaskowane glikany, z krótkim separatorem na jednym końcu, dzięki czemu można je łatwo przytwierdzić do szkiełek, cząstek lub białek do testów biologicznych.
Otwarcie drogi do systematycznych badań cukrów
Rozwiązując wąskie gardło polegające na niezawodnym dodawaniu kwasu sjalowego na stałym nośniku, praca ta przekształca zautomatyzowany montaż glikanów w znacznie potężniejszą platformę do badania biologii cukrów mleka ludzkiego i innych sializowanych glikanów. Badacze mogą teraz uzyskać panele blisko spokrewnionych struktur w ciągu dni, kontrolować wzory rozgałęzień czy obecność fukozy i bezpośrednio testować, jak te różnice wpływają na odporność, zakażenia czy choroby. W praktycznym wymiarze badanie przybliża nas do rutynowej, na żądanie produkcji złożonych cukrów mlecznych jako narzędzi badawczych, potencjalnych terapii lub składników następnej generacji żywienia niemowląt.
Cytowanie: Kuo, YT., Le Mai Hoang, K. & Seeberger, P.H. Synthesis of sialylated human milk oligosaccharides by automated glycan assembly. Nat Commun 17, 4214 (2026). https://doi.org/10.1038/s41467-026-73028-w
Słowa kluczowe: oligosacharydy mleka ludzkiego, kwas sjalowy, zautomatyzowany montaż glikanów, synteza węglowodanów, żywienie niemowląt