Clear Sky Science · de
Synthese sialylierter humaner Milch-Oligosaccharide durch automatisierte Glykanassemblierung
Warum bessere Milchzucker wichtig sind
Muttermilch enthält eine komplexe Mischung aus Zuckern, die die Darmflora, das Immunsystem und die Infektionsresistenz eines Säuglings prägen. Zu den wichtigsten zählen sialylierte humane Milch-Oligosaccharide — verzweigte Zuckerketten, die an den Enden ein spezielles Zuckerbaustein namens Sialinsäure tragen. Forschende möchten jedes dieser Moleküle genau untersuchen und sie möglicherweise als Wirkstoffe oder Diagnostika nutzen, doch die Gewinnung reiner Proben aus Milch ist extrem schwierig. Diese Studie beschreibt eine Methode, mit der sich diese komplizierten Milchzucker schnell und präzise in einer automatisierten Zucker‑Aufbauanlage herstellen lassen.
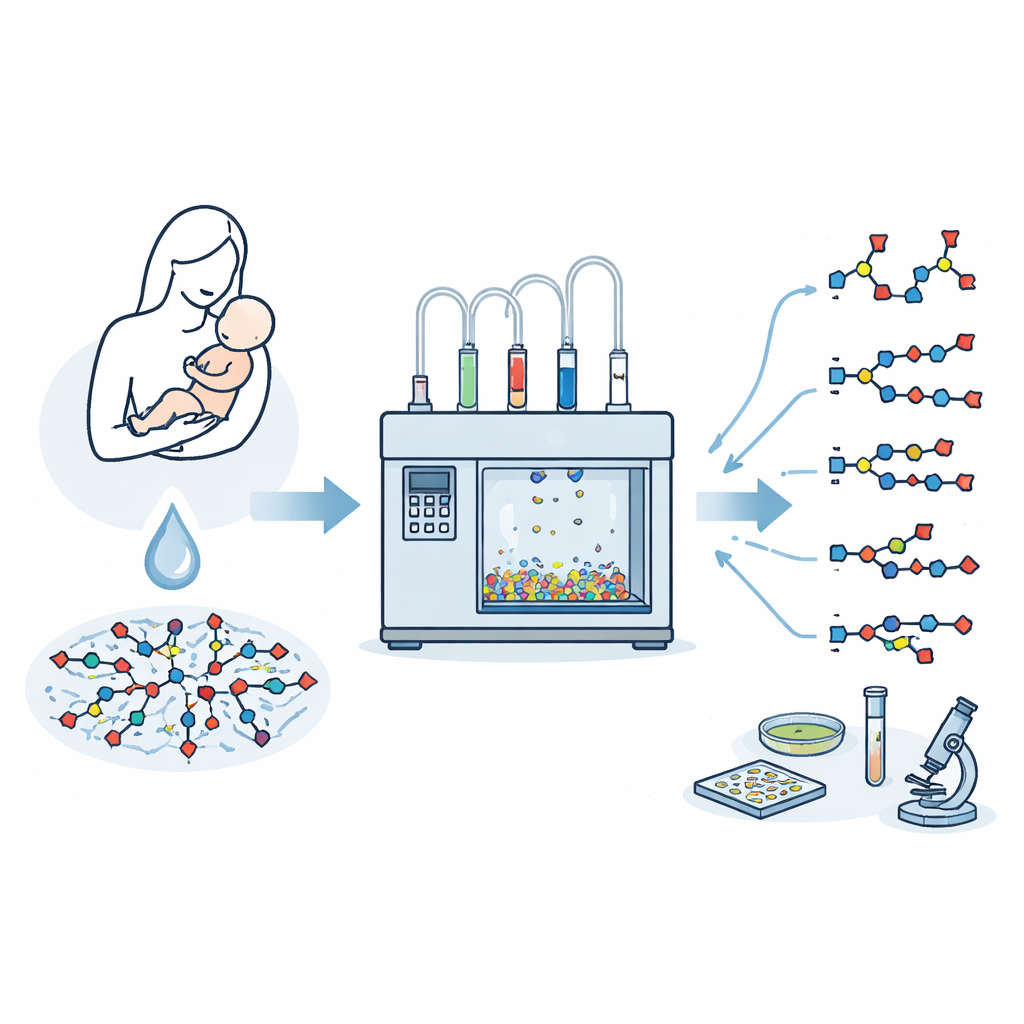
Spezielle Zucker an den Kettenenden
Sialinsäuren sitzen an den Spitzen vieler Zuckerketten auf Zelloberflächen und spielen Schlüsselrollen bei der Zellkommunikation, der Immunabwehr und beim Andocken von Viren und Bakterien an unser Gewebe. In der Muttermilch trägt etwa eines von fünf bekannten Oligosacchariden Sialinsäure. Diese sialylierten Strukturen werden mit Vorteilen wie Schutz vor Darmerkrankungen bei Frühgeborenen und der Funktion als Lockstoff, der Influenzaviren einfängt, in Verbindung gebracht. Die Natur stellt sie jedoch nur in winzigen Mengen und in einem komplexen Gemisch bereit, weshalb Forschende effiziente synthetische Wege benötigen, um Milligramm‑ bis Gramm‑Mengen einzelner, wohldefinierter Strukturen zu erhalten.
Den Zuckeraufbau in einen maschinellen Prozess verwandeln
Die automatisierte Glykanassemblierung ist eine Technik, bei der einfache Zuckerbausteine schrittweise auf winzigen Harzperlen verknüpft werden, gesteuert vom Computer. Sie erspart mühsame Aufreinigungen nach jedem Schritt und kann Synthesen, die früher Monate dauerten, auf Tage komprimieren. Allerdings war das Anfügen von Sialinsäure an eine wachsende Kette auf einer festen Phase ein langjähriges Problem. Form und Ladung der Sialinsäure begünstigen eine unerwünschte Abbaureaktion statt der gewünschten Bindungsbildung, und es ist schwierig, die räumliche Anordnung (die „Händigkeit“) der neuen Bindung zu kontrollieren. Frühere Arbeiten setzten entweder auf vorgefertigte Zwei‑Zucker‑Bausteine, die speziell für das jeweilige Ziel zugeschnitten waren, oder funktionierten nur für sehr kurze Ketten.
Eine neue Klasse „eingezäunter“ Sialinsäure‑Bausteine
Die Autorinnen und Autoren übernehmen und adaptieren ein einfallsreiches Konzept: makrobicyclische Sialinsäure‑Donoren. In diesen Bausteinen verbindet eine kleine chemische Hülse verschiedene Teile der Sialinsäure und bildet eine starre, käfigartige Struktur. Diese Einschränkung lenkt die angreifende Zuckerkette so, dass sie von der richtigen Seite angreift, was das gewünschte räumliche Ergebnis fördert und die Abbaureaktion unterdrückt. Das Team optimierte systematisch das Verhalten dieser Donoren auf fester Phase — sie variierten Lösungsmittelgemische, die Menge des zugegebenen Donors, Temperatur und das Design der eingreifenden Zuckereinheiten. Sie fanden heraus, dass moderat reaktive Donoren auf dem dicht gepackten Harz besser funktionieren als hochreaktive, und dass das Freilegen bestimmter Positionen am Akzeptor‑Zucker während der Reaktion Platz schafft und die Ausbeuten verbessert.
Aufbau einer Bibliothek komplexer Milchzucker
Mit diesen Bedingungen stellten die Forschenden neun verschiedene sialylierte humane Milch-Oligosaccharide unterschiedlicher Größe und Verzweigung her, darunter Moleküle, die nicht nur Sialinsäure, sondern auch einen weiteren wichtigen Zucker, Fucose, tragen. Ein Höhepunkt ist die erfolgreiche automatisierte Synthese von DSLNF II, einer stark verzweigten, fucosylierten und disialylierten Sieben‑Zucker‑Kette, die sich Enzymverfahren entzog und zuvor eine aufwändige, von Hand durchgeführte Totalsynthese erforderte. Dabei zeigte das Team, wie subtile Änderungen weit entfernt vom Reaktionszentrum — etwa der Austausch einer vorübergehenden Schutzgruppe gegen eine andere an einem entfernten Zucker — die Geschwindigkeit der Sialinsäure‑Anfügung dramatisch beschleunigen oder verlangsamen können.
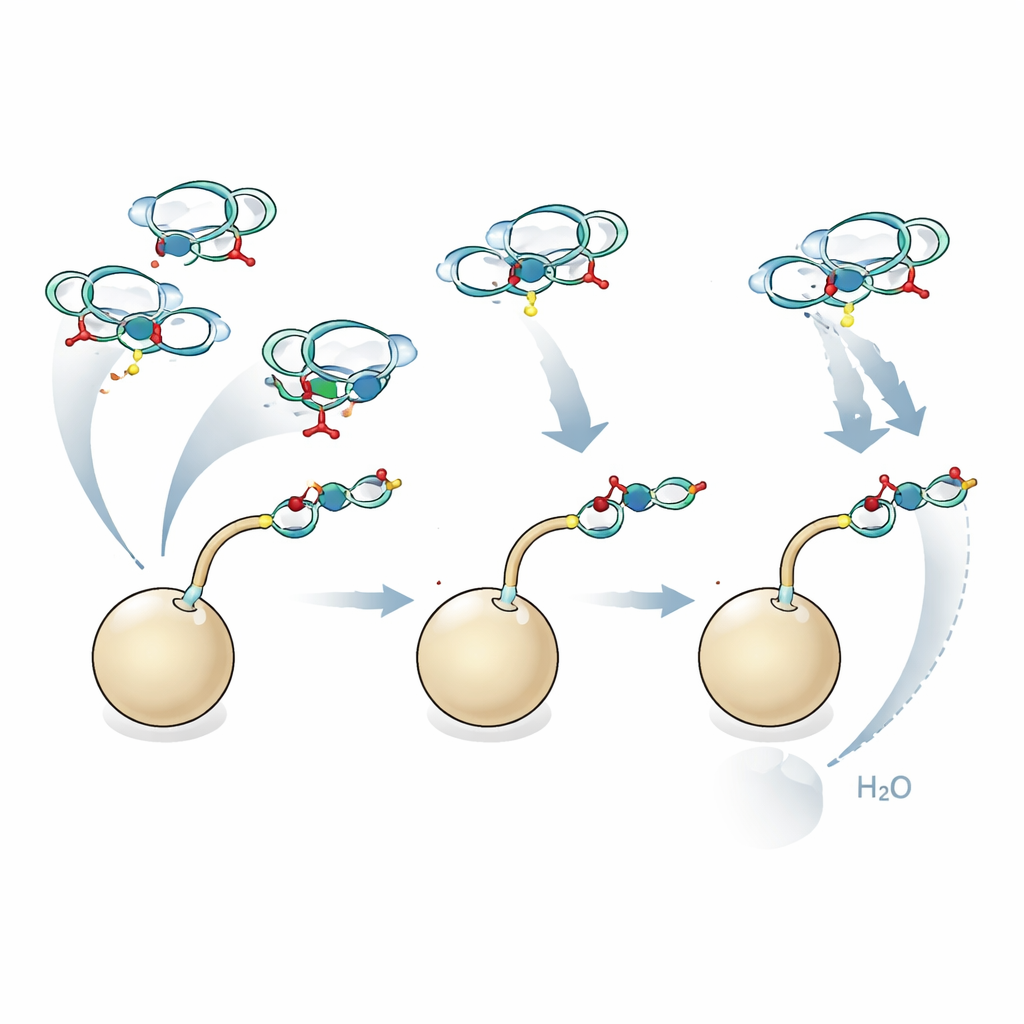
Von geschützten Ketten zu einsatzbereiten Werkzeugen
Da die automatisierte Assemblierung auf Schutzgruppen angewiesen ist, um zu steuern, welche Positionen reagieren, tragen die Endprodukte zunächst viele temporäre chemische Masken. Alle diese Gruppen zu entfernen, ohne empfindliche Sialinsäure‑ und Fucosbindungen zu beschädigen, ist eine Herausforderung. Die Autorinnen und Autoren entwickelten eine schonende, schrittweise Deprotektion, beginnend mit einer Zink‑Kupfer‑Reduktion, gefolgt von kontrollierter Acetylierung, milder Basenbehandlung und schließlich Hydrierung. Dieses Protokoll lieferte konsistent saubere, vollständig entfremdete Glykane, jeweils mit einem kurzen Spacer an einem Ende, so dass sie leicht an Gläser, Partikel oder Proteine für biologische Tests gekoppelt werden können.
Die Tür für systematische Zuckerstudien öffnen
Indem sie den Engpass der zuverlässigen Anfügung von Sialinsäure auf einer festen Phase gelöst haben, macht diese Arbeit die automatisierte Glykanassemblierung zu einer deutlich leistungsfähigeren Plattform, um die Biologie humaner Milchzucker und anderer sialylierter Glykane zu erforschen. Forschende können nun in Tagen auf Reihen eng verwandter Strukturen zugreifen, Verzweigungsmuster oder das Vorhandensein von Fucose gezielt variieren und direkt testen, wie diese Unterschiede Immunität, Infektion oder Krankheit beeinflussen. Praktisch bringt uns die Studie näher an eine routinemäßige, bedarfsorientierte Herstellung komplexer Milchzucker als Werkzeuge für die Forschung, potenzielle Therapeutika oder Bestandteile der nächsten Generation der Säuglingsernährung.
Zitation: Kuo, YT., Le Mai Hoang, K. & Seeberger, P.H. Synthesis of sialylated human milk oligosaccharides by automated glycan assembly. Nat Commun 17, 4214 (2026). https://doi.org/10.1038/s41467-026-73028-w
Schlüsselwörter: human milk oligosaccharides, sialic acid, automated glycan assembly, carbohydrate synthesis, infant nutrition