Clear Sky Science · pl
Podwójne zablokowanie punktów kontrolnych fagocytozy ożywia nadzór immunologiczny w modelach mysich glejaka
Skierowanie „ekipy sprzątającej” ciała przeciwko nowotworowi mózgu
Glejaki to jedna z najbardziej śmiertelnych postaci nowotworów mózgu, częściowo dlatego, że umiejętnie ukrywają się przed układem odpornościowym. Badanie to analizuje nowy sposób na odkrycie tych guzów, ucząc komórki „ekipy sprzątającej” organizmu rozpoznawania i pożerania komórek nowotworowych w sposób bardziej skuteczny. Prace sugerują, że zablokowanie dwóch określonych molekularnych tarcz na komórkach nowotworowych może wywołać silną reakcję łańcuchową, która mobilizuje różne ramiona układu odpornościowego przeciwko glejakowi, przynajmniej u myszy.
Jak guzy wysyłają do komórek odpornościowych sygnał „Nie jedz mnie”
Nasz układ odpornościowy obejmuje komórki takie jak makrofagi, które patrolują tkanki, pochłaniają uszkodzone lub nieprawidłowe komórki i prezentują ich fragmenty limfocytom T, by wywołać szerszy atak. Wiele nowotworów broni się jednak, eksponując na powierzchni cząsteczki działające jak sygnały „nie jedz mnie”. Jedna z takich cząsteczek, CD47, była głównym eksperymentalnym celem, ale leki blokujące samo CD47 dały nierówne korzyści. Autorzy tej pracy szukali innych podobnych tarcz w glejaku i odkryli, że inna cząsteczka, CD24, jest obficie eksponowana na komórkach glejowych, podczas gdy jej receptor Siglec-10 występuje na komórkach odpornościowych. Taki wzorzec sugeruje bezpośrednią linię komunikacji od guza do makrofaga, która każe układowi odpornościowemu stać z boku.
Atak na dwóch frontach przeciw tarczom guza
Korzytsając z mysich i ludzkich linii komórkowych glejaka, badacze testowali przeciwciała blokujące albo CD24, albo CD47, albo oba jednocześnie. Zaobserwowali, że blokada CD24 lub CD47 osobno nieznacznie zwiększała częstość, z jaką makrofagi pochłaniały komórki nowotworowe eksponujące CD24. Gdy jednak zablokowano oba sygnały jednocześnie, makrofagi pochłaniały znacznie więcej komórek nowotworowych, co potwierdza, że dwie ścieżki „nie jedz mnie” działają równolegle. W komórkach glejaka pozbawionych CD24, przywrócenie CD24 odtworzyło tę wrażliwość, co wzmacnia rolę CD24 jako kluczowego przełącznika warunkującego skuteczność podwójnego leczenia.
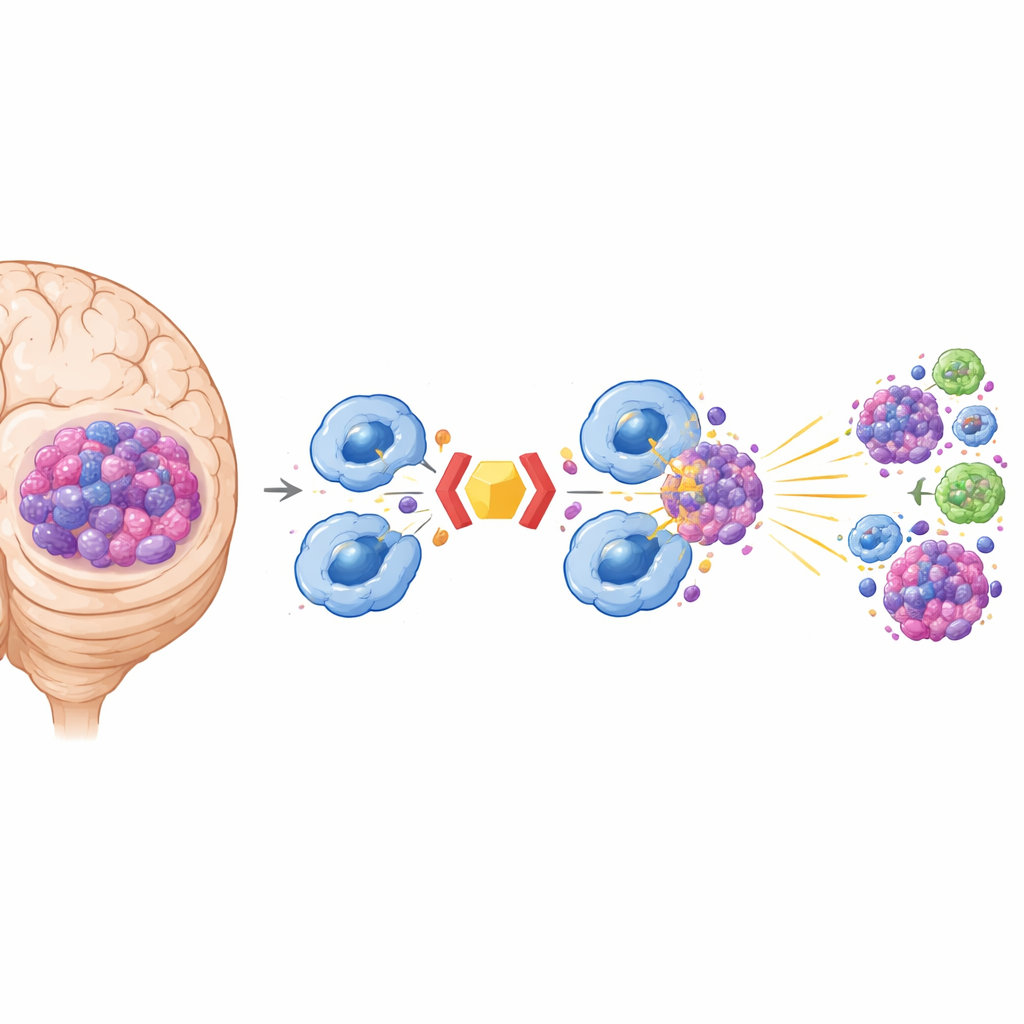
Od pożerania guzów do alarmowania całego układu odpornościowego
Makrofagi robią więcej niż tylko trawią guzy. Po skonsumowaniu komórek nowotworowych przetwarzają białka guza i eksponują je na swojej powierzchni, gdzie limfocyty T mogą je „zobaczyć” i ulec aktywacji. W modelach mysich podwójna blokada CD24 i CD47 prowadziła do silniejszej prezentacji testowego antygenu nowotworowego oraz żywiołowej proliferacji zarówno pomocniczych (CD4+), jak i cytotoksycznych (CD8+) limfocytów T. W wnętrzu makrofagów to zwiększone pożeranie uruchamiało szlak cGAS–STING, molekularny system alarmowy wykrywający DNA z pochłoniętych komórek nowotworowych i napędzający produkcję zapalnych cząsteczek zwanych interferonami typu I. Te sygnały pomagały przekształcić środowisko guza z „zimnego” i immunosupresyjnego w „gorące”, z większą liczbą aktywowanych makrofagów i nasilonym napływem limfocytów T do guzów mózgu.
Łączenie odporności wrodzonej z nowoczesną immunoterapią
W mysich modelach glejaka, szczególnie w tych zaprojektowanych tak, by odzwierciedlać oporność guzów ludzkich na leczenie, podwójna blokada wyraźnie poprawiła przeżywalność w porównaniu z blokowaniem tylko jednego punktu kontrolnego. Korzyść ta zależała od prawidłowego działania sygnalizacji cGAS–STING w makrofagach gospodarza oraz od obecności limfocytów CD8+, co pokazuje, że potrzebne były zarówno odporność wrodzona, jak i adaptacyjna. Autorzy zaobserwowali też, że w miarę jak guzy stawały się zapalne i napływały limfocyty T, wzmacniała się droga PD1–PDL1, znany mechanizm ucieczki, który może osłabić aktywność limfocytów T. Gdy badacze połączyli podwójną blokadę punktów kontrolnych fagocytozy z przeciwciałem blokującym PD1 — klasą leków już stosowaną w klinice — zaobserwowali dalsze korzyści: więcej komórek T walczących z guzem, mniej supresyjnych komórek mieloidalnych, mniejsze guzy i dłuższe przeżycie. Myszy, które pokonały guzy dzięki tej potrójnej terapii, także opierały się ponownemu wszczepieniu guza, co wskazuje na trwałą pamięć immunologiczną.

Co to może znaczyć dla przyszłego leczenia nowotworów mózgu
Dla niespecjalisty główne przesłanie jest takie, że praca ta przedstawia plan pomagający układowi odpornościowemu „zobaczyć” i skuteczniej zaatakować glejaka. Dzięki jednoczesnemu usunięciu dwóch oddzielnych sygnałów „nie jedz mnie” makrofagi mogą zarówno bezpośrednio niszczyć komórki nowotworowe, jak i rozgłaszać silny alarm, który pobudza limfocyty T. Dodanie blokady PD1 zapobiega następnie temu, by guz ponownie wygasił te limfocyty. Chociaż wyniki pochodzą z badań na myszach i będą wymagać starannego przełożenia na leki gotowe do użycia u ludzi, wskazują na strategie kombinacyjne łączące terapie ukierunkowane na makrofagi z istniejącymi inhibitorami punktów kontrolnych limfocytów T. Jeśli podobne efekty pojawią się u ludzi, takie podejścia mogłyby ostatecznie zapewnić pacjentom z glejakiem bardziej trwałą i silniejszą obronę immunologiczną przeciwko temu agresywnemu nowotworowi.
Cytowanie: Ha, J., Wang, Y., Ma, Y. et al. Dual phagocytosis-checkpoint blockade revitalizes immune surveillance in mouse models of glioblastoma. Nat Commun 17, 3709 (2026). https://doi.org/10.1038/s41467-026-70221-9
Słowa kluczowe: glejak, makrofagi, blokada punktów kontrolnych immunologicznych, cGAS-STING, immunoterapia przeciwnowotworowa