Clear Sky Science · ar
حجب نقطتي التفاغي يعيد تنشيط المراقبة المناعية في نماذج فأرية للغليوبلاستوما
توجيه طاقم التنظيف في الجسم ضد سرطان الدماغ
الغليوبلاستوما هي واحدة من أشد أنواع سرطان الدماغ فتكًا، ويرجع ذلك جزئيًا إلى براعتها في الاختباء من الجهاز المناعي. تستكشف هذه الدراسة طريقة جديدة لكشف هذه الأورام من خلال تعليم خلايا «طاقم التنظيف» في الجسم على التعرف على الخلايا السرطانية وابتلاعها بشكل أكثر فاعلية. تشير النتائج إلى أن حجب درعين جزيئيين محددين على خلايا الورم يمكن أن يوقظ سلسلة من التفاعلات القوية التي تحشد عدة أذرع من الجهاز المناعي ضد الغليوبلاستوما، على الأقل في الفئران.
كيف تخبر الأورام خلايا المناعة «لا تأكلوني»
تشمل دفاعاتنا المناعية خلايا مثل البلعميات الكبيرة، التي تقوم بدوريات في الأنسجة وتبتلع الخلايا التالفة أو الشاذة وتعرض شظاياها للخلايا التائية لتحفيز هجوم أوسع. ومع ذلك، تحمي العديد من السرطانات نفسها من خلال عرض جزيئات سطحية تعمل كإشارات «لا تأكلوني». كان أحد هذه الجزيئات، CD47، هدفًا تجريبيًا مهمًا، لكن العقاقير التي تحجب CD47 وحده أعطت فوائد متفاوتة. بحث مؤلفو الورقة عن دروع مماثلة في الغليوبلاستوما ووجدوا أن جزيئًا آخر، CD24، معروض بغزارة على خلايا الورم، بينما يستقر مستقبل شريكه Siglec-10 على خلايا المناعة. يشير هذا النمط إلى خط اتصال مباشر من الورم إلى البلعميات يخبر الجهاز المناعي بالتراجع.
هجوم ذو جبهتين على دروع الورم
باستخدام خطوط خلايا غليوبلاستوما فأرية وبشرية، اختبر الباحثون أجسامًا مضادة تحجب CD24 أو CD47 أو كلاهما معًا. لاحظوا أن حجب CD24 أو CD47 بشكل منفرد زاد بشكل معتدل من وتيرة ابتلاع البلعميات لخلايا الورم التي تعبر عن CD24. عندما حجبوا الإشارتين معًا، ومع ذلك، ابتلعت البلعميات عددًا أكبر بكثير من الخلايا السرطانية، مؤكدين أن طريقَي «لا تأكلني» يعملان بالتوازي. في خلايا الغليوما التي افتقرت إلى CD24، أعاد إدخال CD24 هذه الحساسية، مما عزز أن CD24 هو مفتاح يحدد ما إذا كان العلاج المزدوج فعالًا.
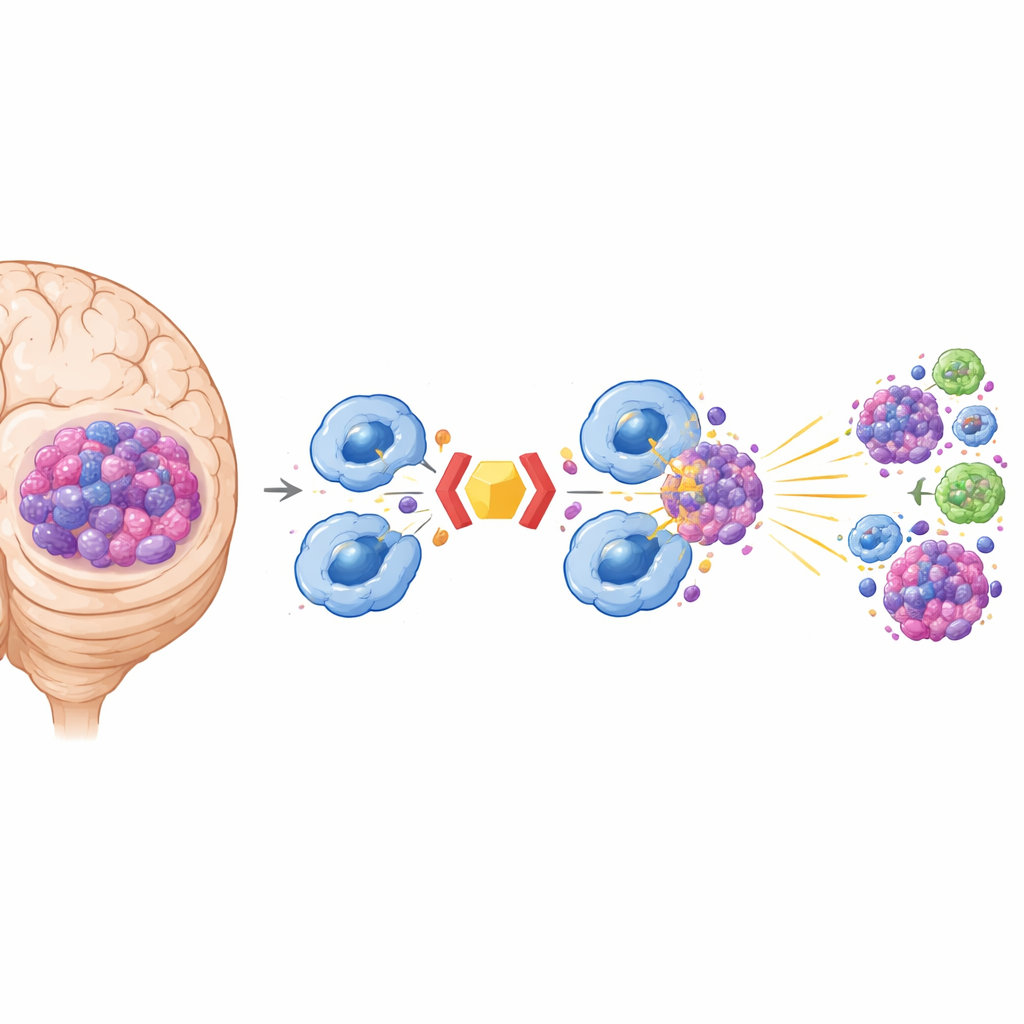
من أكل الأورام إلى إنذار الجهاز المناعي بأكمله
تفعل البلعميات أكثر من مجرد هضم الأورام. بعد أن تبتلع الخلايا السرطانية، تعالج بروتينات الورم وتعرضها على سطحها، حيث تستطيع الخلايا التائية «رؤيتها» وتصبح مفعلة. في نماذج الفئران، أدى الحجب المزدوج لـ CD24 وCD47 إلى عرض أقوى لمستضد تجريبي من الورم وتكاثر قوي لكل من الخلايا التائية المساعدة (CD4+) والقاتلة (CD8+). داخل البلعميات، أدى هذا الابتلاع المعزز إلى تنشيط مسار cGAS–STING، وهو نظام إنذار جزيئي يكشف DNA من الخلايا المبتلعة ويدفع إنتاج جزيئات التهابية تسمى إنترفيرونات نوع I. ساعدت هذه الإشارات في إعادة تشكيل بيئة الورم من «باردة» وقمعية مناعيًا إلى «ساخنة»، مع زيادة في البلعميات المفعلة وتوغل أكبر للخلايا التائية إلى أورام الدماغ.
ربط الدفاعات الفطرية بالعلاج المناعي الحديث
في نماذج الغليوبلاستوما الفأرية، خاصة تلك المصممة لمحاكاة الطبيعة المقاومة للعلاج في الأورام البشرية، حسّن الحجب المزدوج بوضوح البقاء على قيد الحياة مقارنة بحجب نقطة تفتيش واحدة فقط. اعتمدت هذه الفائدة على وجود إشارة cGAS–STING سليمة في بلعميات العائل وعلى وجود الخلايا التائية CD8+، مما يبيّن أن كلا المناعة الفطرية والمكتسبة كانتا مطلوبتين. لاحظ المؤلفون أيضًا أنه مع التهاب الأورام ودخول الخلايا التائية، صعدت خلايا الورم مسار PD1–PDL1، وهو طريق معروف للهروب يمكنه كبح نشاط الخلايا التائية. عندما جمع الباحثون حجب نقطتي التفاغي المزدوجة مع جسم مضاد حابس لـ PD1—فئة دوائية مستخدمة بالفعل سريريًا—شهدوا مكاسب إضافية: مزيد من الخلايا التائية المقاتلة للورم، عدد أقل من الخلايا النخاعية القمعية، أورام أصغر وبقاء أطول. الفئران التي تغلبت على أورامها تحت هذا العلاج الثلاثي قاومت حتى إعادة تحدي الورم، مما يشير إلى ذاكرة مناعية دائمة.

ماذا قد يعني هذا لعلاج سرطان الدماغ في المستقبل
بالنسبة لغير المتخصصين، الرسالة الرئيسية هي أن هذا العمل يقدم مخططًا لمساعدة الجهاز المناعي على «رؤية» ومهاجمة الغليوبلاستوما بشكل أكثر فاعلية. من خلال رفع إشارتَي «لا تأكلني» منفصلتين في آن واحد، تستطيع البلعميات تدمير خلايا الورم مباشرة وإرسال إنذار قوي يوقظ الخلايا التائية. ثم يمنع حجب PD1 الأورام من إعادة إسكات تلك الخلايا التائية. بينما تستند النتائج إلى تجارب في الفئران وستتطلب ترجمة دقيقة باستخدام عقاقير جاهزة للاستخدام البشري، فإنها تشير إلى استراتيجيات مركبة توحد العلاجات الموجهة نحو البلعميات مع مثبطات نقاط التفتيش الخلوية المعتمدة على الخلايا التائية. إذا ظهرت تأثيرات مماثلة لدى البشر، فقد تمنح هذه المقاربات في النهاية مرضى الغليوبلاستوما دفاعًا مناعيًا أقوى وأكثر دوامًا ضد هذا السرطان العدواني.
الاستشهاد: Ha, J., Wang, Y., Ma, Y. et al. Dual phagocytosis-checkpoint blockade revitalizes immune surveillance in mouse models of glioblastoma. Nat Commun 17, 3709 (2026). https://doi.org/10.1038/s41467-026-70221-9
الكلمات المفتاحية: الغليوبلاستوما, البلعميات الكبيرة (البلعميات), حجب نقاط التفتيش المناعية, cGAS-STING, مناعة السرطان