Clear Sky Science · pl
Podwójna dekonwolucja w wielofotonowej mikroskopii ze strukturalnym oświetleniem do obrazowania nad‑rozdzielczego w głębokich tkankach
Widzieć głębiej w żywych tkankach
Współczesna biologia często zależy od obserwowania najdrobniejszych detali wewnątrz grubych fragmentów tkanki, takich jak plastry mózgu czy rozwijające się embriony. Niestety, gdy światło przechodzi przez te gęsto upakowane środowiska, ulega załamaniu i zniekształceniu, co powoduje rozmycie obrazu właśnie wtedy, gdy naukowcy najbardziej potrzebują ostrego widoku. Artykuł przedstawia sposób na cyfrowe „odsmużenie” tych obrazów, pozwalając standardowemu, zaawansowanemu mikroskopowi ujawnić bardzo drobne struktury głęboko w tkance bez dodawania kosztownego, skomplikowanego sprzętu.
Dlaczego obrazowanie w głębi jest tak trudne
Mikroskopy fluorescencyjne pozwalają badaczom znakować określone cząsteczki i obserwować, jak komórki i tkanki są zbudowane i jak się zachowują. W ciągu ostatnich dekad kilka metod „nad‑rozdzielczości” przełamało tradycyjne ograniczenia ostrości, ujawniając detale znacznie poniżej 200 nanometrów. Jednak większość tych metod działa dobrze tylko blisko powierzchni próbki. W grubych tkankach, takich jak mózg myszy, zarówno światło używane do wzbudzania znaczników fluorescencyjnych, jak i emitowane światło docierające do detektora, ulegają zniekształceniom spowodowanym drobnymi nierównościami struktury tkanki. Te zniekształcenia, zwane aberracjami, rozmazują ognisko mikroskopu i zatracają informacje o wysokich częstotliwościach, szczególnie na głębokościach większych niż kilkadziesiąt mikrometrów.
Od napraw sprzętowych do rozwiązania programowego
Popularnym sposobem walki z aberracjami jest sprzętowa optyka adaptacyjna, która używa ruchomych zwierciadeł lub innych elementów do kształtowania czoła fali świetlnej i przywracania ostrego ogniska. Choć potężne, systemy te są kosztowne, technicznie wymagające i często korygują zaburzenia tylko dla jednego koloru lub jednego kierunku propagacji światła naraz. Autorzy proponują zamiast tego podejście obliczeniowe, które działa z typem mikroskopu już szeroko stosowanym w wielu laboratoriach: laserowo skanującym mikroskopem wielofotonowym. Zamieniając zwykły pojedynczy detektor światła na kamerę, rejestrują bogisty stos obrazów skanowanych, który koduje, jak zarówno światło wzbudzające, jak i emitowane zostały zniekształcone przez tkankę.
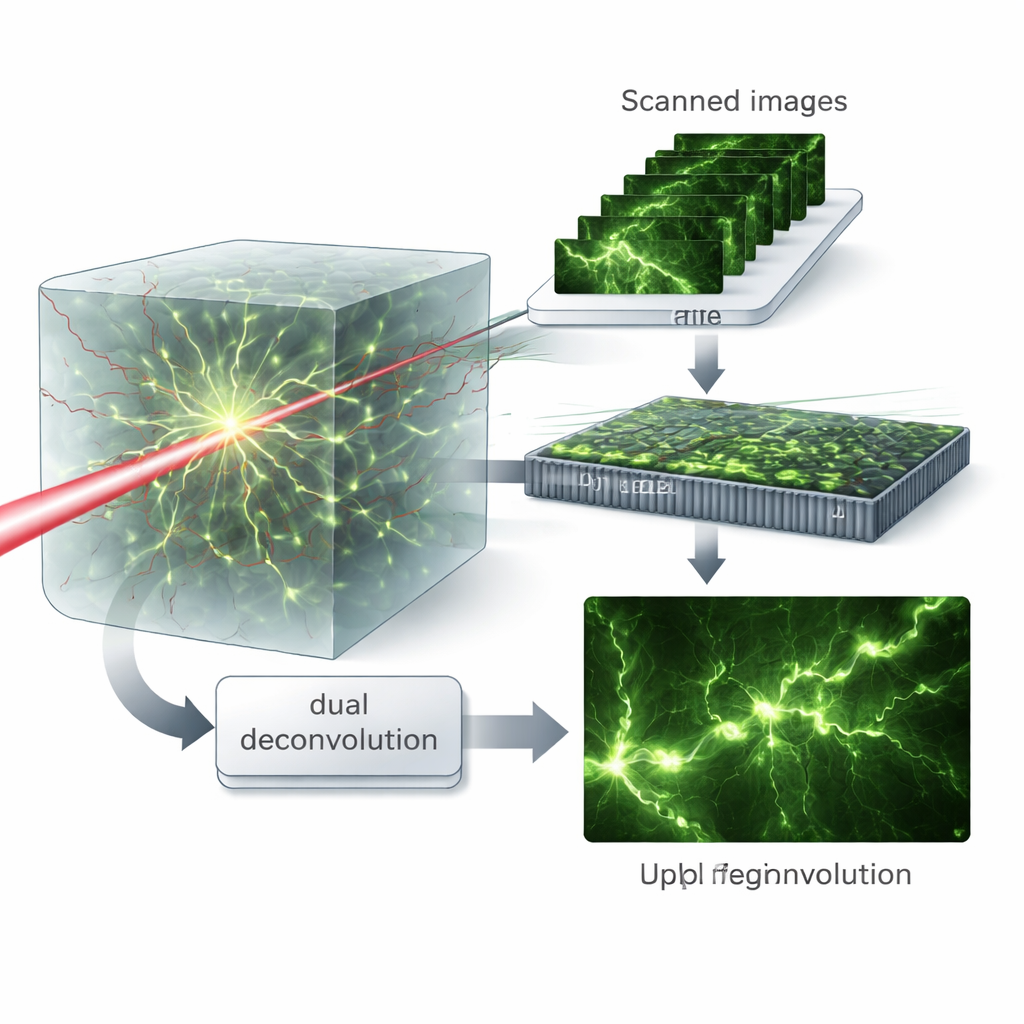
Wirtualne wzory i podwójne oczyszczanie
Kluczową intuicją jest traktowanie obrazów skanowanych tak, jakby próbka była oświetlana wieloma różnymi drobnymi wzorami światła — koncept, który autorzy nazywają wirtualnym oświetleniem strukturalnym. Matematyczne ponowne łączenie tych danych w dziedzinie częstotliwości pozwala oddzielić role procesu wzbudzania i emisji. Następnie wprowadzają algorytm „podwójnej dekonwolucji”, który na przemian estymuje i koryguje rozmycie po każdej stronie — światła wchodzącego i wychodzącego — zamiast sumować je w jedno efektywne rozmycie. To macierzowe podejście zachowuje więcej detali o wysokich częstotliwościach i pozwala algorytmowi odzyskać drobne struktury nawet przy silnych aberracjach.
Bardziej ostre widoki w symulacjach i w rzeczywistych próbkach
Aby przetestować swoją metodę, zespół najpierw użył symulacji komputerowych mikroskopii dwu‑fotonicznej, techniki obrazowania głębokiego, która wykorzystuje pary fotonów o niższej energii do wzbudzania fluorescencji tylko w punkcie ogniskowania. Przy silnych symulowanych zniekształceniach konwencjonalne rekonstrukcje dwu‑fotoniczne i standardowe rekonstrukcje ze strukturalnym oświetleniem dawały wyraźnie rozmyte obrazy. Natomiast podwójna dekonwolucja przywracała ostre wzory, których rozdzielczość zbliżała się do jednej czwartej długości fali fluorescencji — około 130 nanometrów — zgodnie z oczekiwaniami teoretycznymi. Autorzy następnie zbudowali niestandardowy układ dwu‑fotoniczny z kamerą naukową i zastosowali swój algorytm do rzeczywistych próbek, w tym kul fluorescencyjnych, wzorców testowych ukrytych za warstwami rozpraszającymi, hodowanych komórek, tkanki mózgowej myszy oraz całych preparatów danio pręgowanego. Wielokrotnie struktury, które w obrazach konwencjonalnych wydawały się rozmazane lub podwojone, po przetworzeniu ujawniały się jako wyraźnie rozdzielone elementy, a drobne elementy neuronalne, takie jak kolce dendrytyczne, pozostawały rozróżnialne na głębokościach do 180 mikrometrów w mózgu myszy.
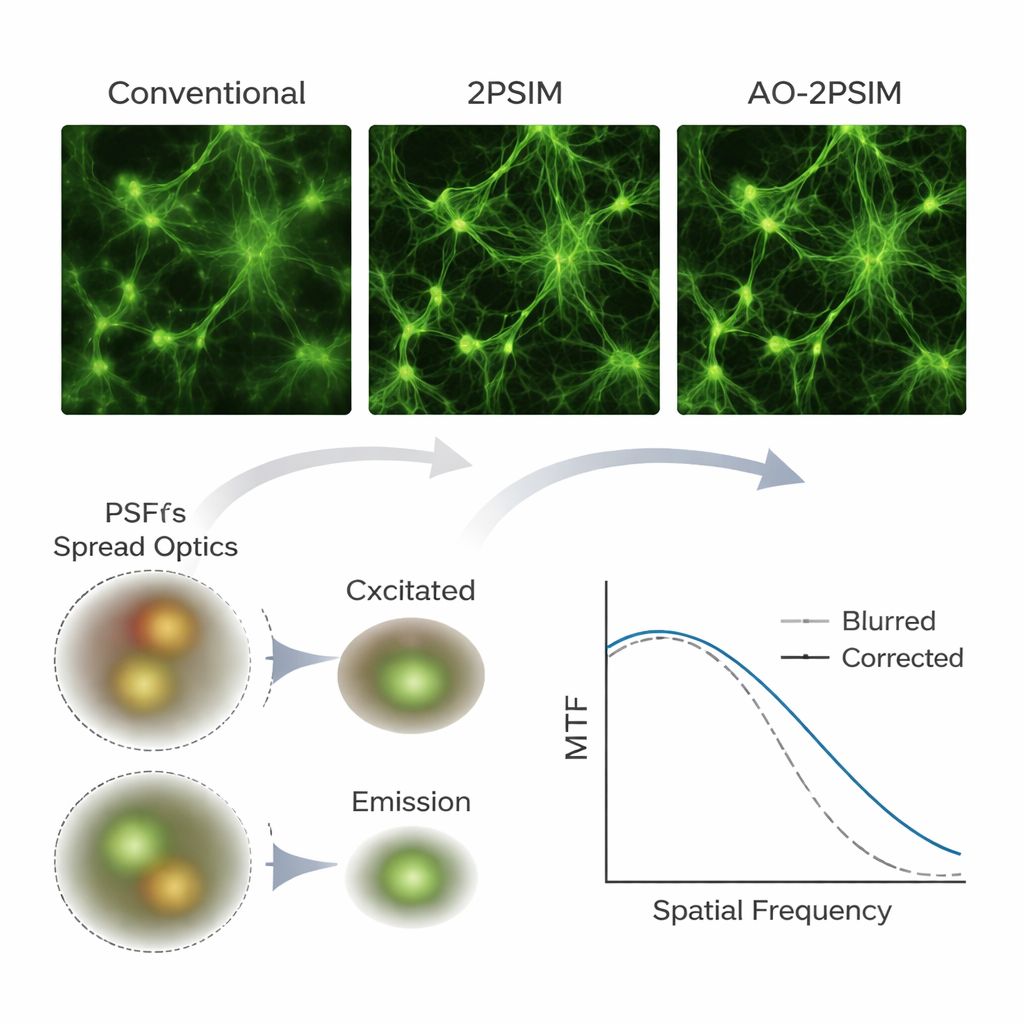
Co to oznacza dla obrazowania biologicznego
Dla osób spoza specjalizacji główne przesłanie jest takie, że autorzy pokazali, jak przekształcić istniejące mikroskopy wielofotonowe w znacznie mocniejsze narzędzia do obrazowania w głębokich tkankach, wykorzystując w przeważającej mierze oprogramowanie i wymianę na kamerę. Poprzez staranne modelowanie i korektę tego, jak tkanki załamują światło na wejściu i wyjściu, ich podejście z podwójną dekonwolucją podwaja zwykły limit rozdzielczości w wymagających, grubych próbkach bez polegania na złożonych adaptacyjnych zwierciadłach. Choć metoda wciąż zależy od zebrania wystarczającego sygnału i obecnie wymaga relatywnie wolnego skanowania, oferuje praktyczną, opłacalną drogę do rutynowego uzyskiwania ultraczystych widoków mózgu i innych narządów w trzech wymiarach, otwierając drzwi do bardziej szczegółowych badań nad organizacją struktur biologicznych i ich zmianami w czasie.
Cytowanie: Lim, S., Kang, S., Hong, J.H. et al. Dual deconvolution in multiphoton structured illumination microscopy for deep-tissue super-resolution imaging. Nat Commun 17, 2123 (2026). https://doi.org/10.1038/s41467-026-69798-y
Słowa kluczowe: mikroskopia nad‑rozdzielczości, obrazowanie dwu‑fotoniczne, optyka adaptacyjna, obrazowanie w głębokich tkankach, obrazowanie obliczeniowe