Clear Sky Science · nl
Multiplex NGS-panel voor volledige genoomherstel en moleculaire epidemiologie van canine morbillivirus
Waarom dit belangrijk is voor huisdieren en mensen
Hondenliefhebbers, natuurbeschermers en volksgezondheidswatchers hebben allemaal belang bij een virus dat bekendstaat als hondenziekte (canine distemper). Deze zeer besmettelijke ziekte kan huisdieren en wilde roofdieren verwoesten, en nauwe verwanten van het virus omvatten mazelen bij mensen. De hier beschreven studie onthult een nieuwe, betaalbare genetische test die de volledige genetische code van het distempervirus rechtstreeks uit zieke dieren leest, waardoor wetenschappers kunnen volgen hoe het zich verspreidt, verandert en mogelijk nieuwe soorten kan bedreigen.
Een virus dat diersoorten overschrijdt
Het canine distempervirus vormt wereldwijd een bedreiging en infecteert huishonden, wilde roofdieren zoals vossen en grote katten, en zelfs sommige niet‑roofdierachtige soorten. Het valt meerdere organen aan, veroorzaakt koorts, ademhalingsproblemen, darmziekten en soms hersenschade. Hoewel het momenteel geen menselijke ziekte is, tonen experimenten aan dat het virus zich kan aanpassen om dezelfde celtoegang te gebruiken als het mazelenvirus bij mensen. Daarom is het belangrijk te volgen hoe het virus evolueert in verschillende gastheren en regio’s—zowel om dieren te beschermen als om zeldzame maar ernstige gedragsveranderingen vroegtijdig te signaleren.
Van gedeeltelijke snapshots naar volledige genetische portretten
Tot nu toe waren de meeste studies van dit virus gebaseerd op het uitlezen van slechts één gen, bekend als H, dat het virus helpt zich aan cellen te hechten. Het bekijken van dit ene stuk code was nuttig om virussen in lijnen in te delen en brede verspreidingspatronen te volgen. Maar het laat veel van de meer dan 15.000 genetische “letters” weg die bepalen hoe het virus zich vermenigvuldigt, het immuunsysteem ontwijkt en zich aan nieuwe gastheren aanpast. Volledige genomen zijn veel informatiever, maar waren moeilijk te verkrijgen uit routinematige klinische monsters, vooral in omgevingen met beperkte middelen en in ondervertegenwoordigde regio’s zoals grote delen van Latijns‑Amerika.

Een nieuwe gereedschapsset om volledige virale genomen te lezen
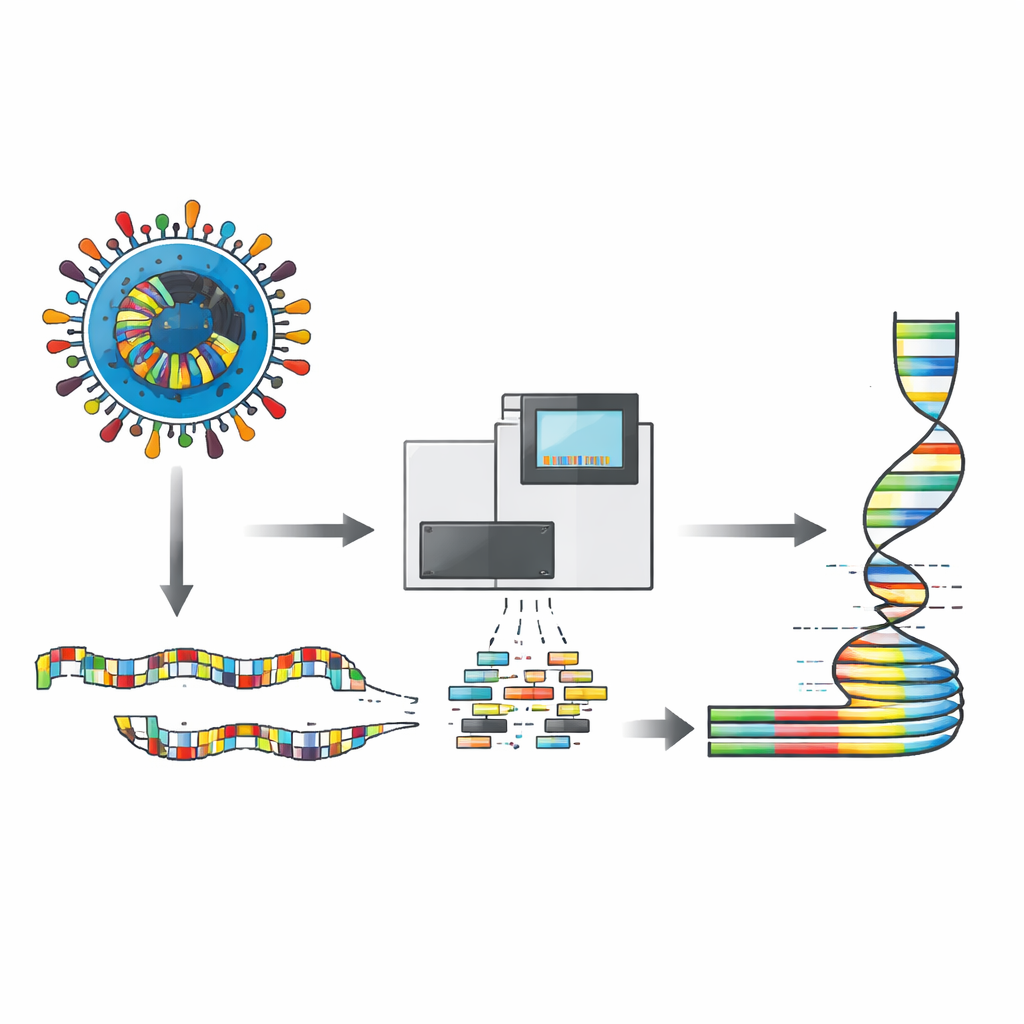
De onderzoekers ontwikkelden een laboratoriumpanel dat het virusgenoom in vele kleine, overlappende fragmenten opdraagt die allemaal in dezelfde reactie gekopieerd kunnen worden en vervolgens door een Illumina next‑generation sequencer gelezen worden. Het ontwerp gebruikte 236 korte starterfragmenten, gegroepeerd in twee mixes, gekozen om overeen te komen met distempervirussen van over de hele wereld, zodat ook uiteenlopende stammen gevangen kunnen worden. Deze opzet geeft de voorkeur aan korte fragmenten, die gemakkelijker te herstellen zijn uit beschadigde of lage‑kwaliteit monsters—precies het soort dat vaak van zieke of dode dieren wordt verzameld. Getest op een vaccinstam en 15 geïnfecteerde honden uit Bolivia, Ecuador, Mexico, Peru en Uruguay, dekte de methode routinematig meer dan 97% van het genoom, vaak met duizenden reads per positie, zelfs wanneer de oorspronkelijke virushoeveelheid in het monster laag was.
Wat de nieuwe genetische kaarten onthulden
Gewapend met deze volledige sequenties, vergeleek het team hun 15 Latijns‑Amerikaanse virussen met 173 eerder beschikbare volledige genomen. Dit bredere perspectief stelde hen in staat elk virus binnen bekende lijnen te plaatsen en fijnere vertakkingspatronen te zien die één gen niet kon oplossen. Honden uit Bolivia droegen virussen die behoren tot een lijn die eerder in Uruguay, Brazilië, Argentinië en Chili was gezien, waarmee het bekende bereik van die lijn werd uitgebreid. Mexicaanse honden droegen een Noord‑Amerikaanse lijn. Stammen uit Ecuador en Peru vormden een aparte cluster die dicht bij, maar los van, een andere Noord‑Amerikaanse groep zit, wat wijst op regionale diversificatie die mogelijk een eigen formele aanduiding verdient naarmate er meer data beschikbaar komen. Wanneer ze de analyse herhaalden met alleen het H‑gen, bleven veel brede groepen behouden, maar sommige relaties vervaagden, wat benadrukt hoe veel duidelijker het volledig‑genoombeeld kan zijn.
Verborgen variatie binnen individuele dieren
Aangezien de methode zeer diepe dekking genereert, kan ze ook minderheidsvormen van het virus detecteren die binnen één gastheer circuleren maar de infectie niet domineren. De onderzoekers vonden zulke minderheidsvarianten in de meeste onderzochte honden. Veel waren enkel‑letterveranderingen en sommige veranderden aminozuren in virale eiwitten die met de afweer van de gastheer interageren. In Mexicaanse monsters doken kleine deleties op in oppervlakte-eiwitten die het virus helpen aan cellen te binden, wat mogelijk verandert hoe het immuunsysteem het waarneemt. Eén Uruguayaans monster droeg een insertie in een eiwit dat betrokken is bij replicatie en immuunontwijking. Sommige van deze veranderingen kunnen echt virale experimenten binnen de gastheer weerspiegelen; andere kunnen artefacten van het amplificatieproces zijn. Hoe dan ook illustreert het werk dat de viruspopulatie binnen één hond niet uniform is maar een wolk van licht verschillende genomen vormt die evolutie kan aandrijven.
Wat dit betekent voor de toekomst
Voor niet‑specialisten is de kernboodschap dat wetenschappers nu een praktische, relatief goedkope manier hebben om vrijwel de gehele genetische code van het canine distempervirus rechtstreeks uit zieke dieren in het veld te lezen, zonder de trage, gespecialiseerde stap van het kweken van het virus in cellen. Dit opent de deur naar routinematige genomische surveillance in regio’s waar gegevens schaars waren, en verbetert ons vermogen te zien hoe het virus tussen landen beweegt, overspringt tussen huisdieren en wilde dieren, en nieuwe genetische mogelijkheden onderzoekt. Door whole‑genome monitoring te koppelen aan het inzicht in verborgen varianten binnen elke gastheer, versterkt deze aanpak pogingen om honden te beschermen, kwetsbare wilde dieren te behouden en een oog te houden op virussen die familie zijn van belangrijke menselijke ziekten.
Bronvermelding: Panzera, Y., Condon, E., Escardó, J. et al. Multiplex NGS Panel for whole-genome recovery and molecular epidemiology of canine morbillivirus. npj Vet. Sci. 1, 5 (2026). https://doi.org/10.1038/s44433-026-00007-8
Trefwoorden: hondenziektevirus, viraal genomica, multiplex-sequencing, ziekten in het wild, One Health