Clear Sky Science · nl
Gastheer-eiwitten geassocieerd met sterke neutraliserende SARS-CoV-2-antilichaamreacties in een cohort uit Zuid-Afrika
Waarom sommige mensen sterkere COVID-bestrijdende antilichamen maken
Wanneer mensen het virus dat COVID-19 veroorzaakt oplopen, maken hun lichamen antilichamen die het virus kunnen blokkeren om cellen te infecteren. Maar niet iedereen produceert deze krachtige “neutraliserende” antilichamen in gelijke mate. Deze studie stelde een eenvoudige maar belangrijke vraag: kunnen we aan de hand van aanwijzingen in het bloed kort na infectie voorspellen wie later bijzonder sterke virus-blokkerende antilichamen ontwikkelt, en wat zegt dat over hoe ons lichaam SARS-CoV-2 bestrijdt?
Patiënten volgen van ziekte tot herstel
Onderzoekers in Durban, Zuid-Afrika volgden 71 volwassenen die tijdens de eerste golf van COVID-19 waren opgenomen, voordat vaccins en grote varianten verschenen. Allen waren geïnfecteerd met de oorspronkelijke vorm van SARS-CoV-2 en waren nooit gevaccineerd. Er werden twee keer bloedmonsters afgenomen: eerst ongeveer zes dagen na de diagnose, toen patiënten nog acuut ziek waren, en opnieuw ongeveer een maand later tijdens het herstel. Vroege bloedmonsters werden geanalyseerd met een hoogdoorvoertechniek die ruwweg 5.000 verschillende eiwitten in bloedplasma tegelijk kan meten. Latere monsters werden getest om te bepalen hoe goed iemands antilichamen het levende virus konden neutraliseren en hoe sterk hun antilichamen binden aan het virale spike-eiwit.
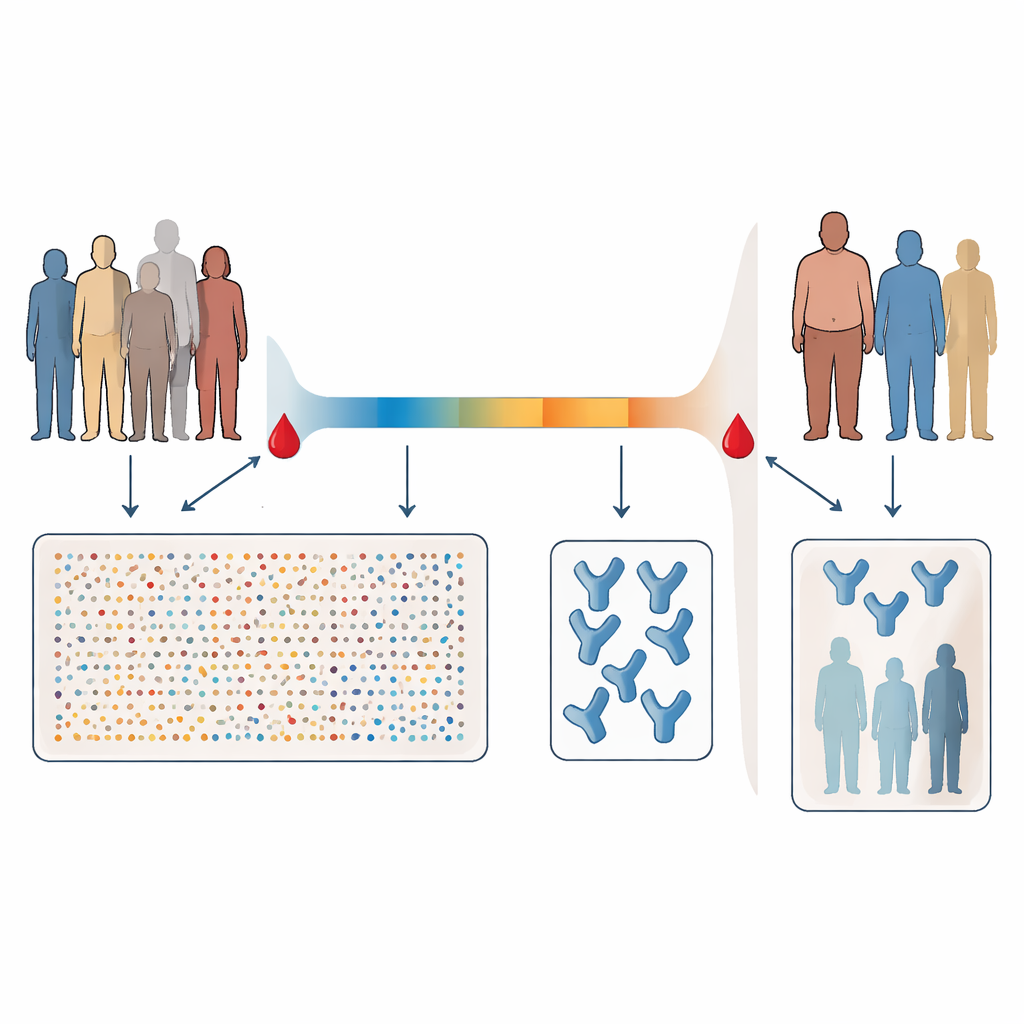
Ziektegraad, risicofactoren en sterkte van antilichamen
Zoals in veel andere studies zagen de onderzoekers dat mensen die zieker waren doorgaans sterkere neutraliserende antilichaamreacties hadden. De deelnemers werden ingedeeld op basis van of zij ooit extra zuurstof nodig hadden, een standaardkenmerk van ernstigere COVID-19. Degenen die zuurstof nodig hadden, en deelnemers die ouder waren, mannen of mensen met aandoeningen zoals hoge bloeddruk of diabetes, behoorden vaker tot de groep met hoge neutraliserende activiteit. Zelfs onder patiënten die nooit zuurstof nodig hadden, kwamen subtielere tekenen van ernstigere ziekte—zoals een hogere verhouding van neutrofielen tot lymfocyten in het bloed en dezelfde reeks risicofactoren—vaker voor bij mensen met sterke neutraliserende reacties. Dit suggereert dat, zelfs zonder intensieve zorg of beademing, wat ernstigere ziekte vaak samenhangt met krachtigere antilichamen.
Vroege eiwitsignalen die sterke antilichamen voorspellen
De centrale focus van het onderzoek was het patroon van eiwitten die vroeg in de infectie in het bloed circuleren. Door mensen met hoge en lage neutraliserende activiteit te vergelijken, en door neutralisatie ook als een continuüm te behandelen, identificeerde het team honderden eiwitten die verschilden tussen groepen. Veel hiervan overlappen met eiwitten die geassocieerd zijn met eenvoudige spike-bindende antilichamen, maar een subset bleek nauwkeuriger verbonden te zijn met de kwaliteit van de neutraliserende respons. Een opvallend eiwit was HSPA8, een lid van de heat-shock-eiwitten die andere eiwitten helpt vouwen en een sleutelrol speelt in hoe immuuncellen virale fragmenten presenteren aan helper-T-cellen. Hogere niveaus van HSPA8 vroeg in de infectie waren sterk gekoppeld aan betere neutraliserende activiteit later, en dit enkele eiwit kon op zichzelf redelijk goed hoge van lage neutraliseerders onderscheiden. In combinatie met twee andere eiwitten, FAP en MLN, verbeterde de voorspelling nog verder.
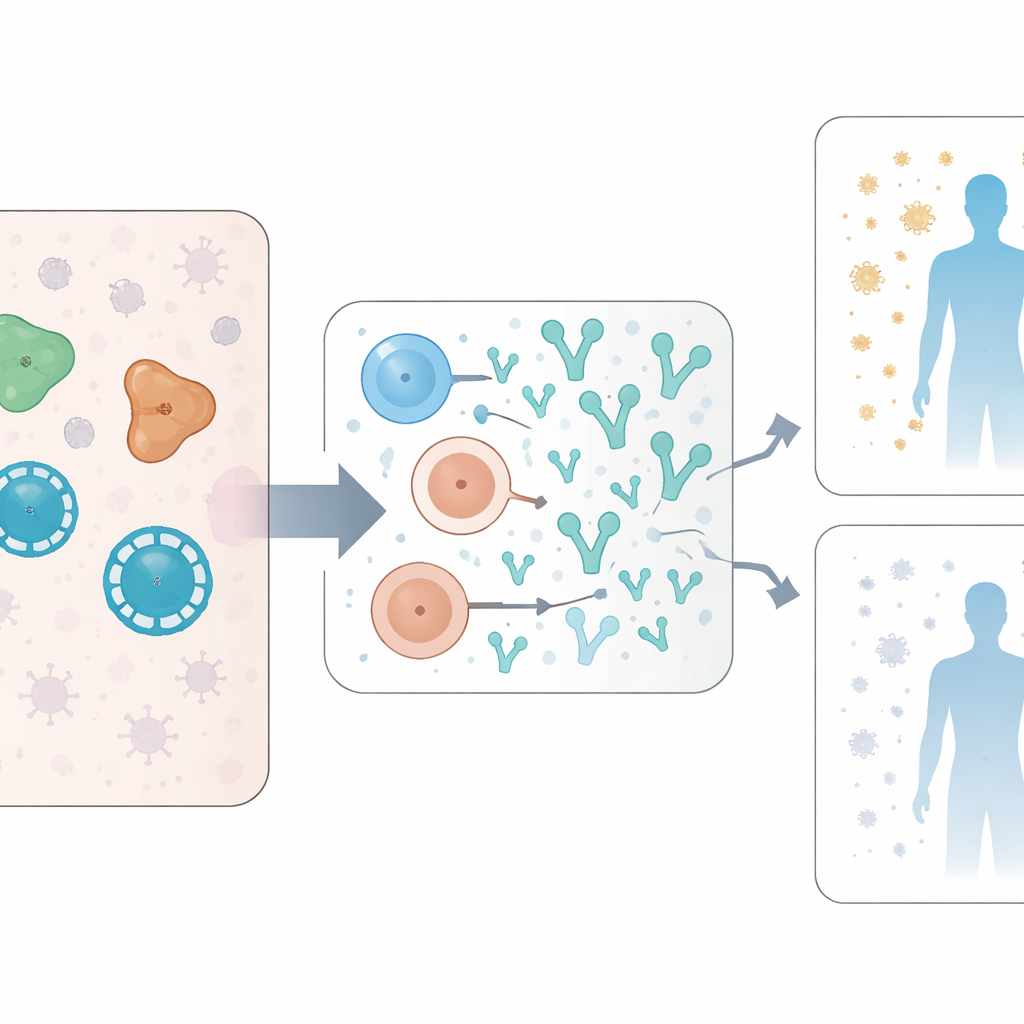
Pathways die metabolisme, infectie en immuniteit verbinden
Kijkend voorbij individuele eiwitten onderzochten de onderzoekers volledige biologische pathways die actiever waren bij mensen die later sterke neutraliserende antilichamen ontwikkelden. Verschillende van deze pathways zijn betrokken bij hoe cellen energie en vetten verwerken, waaronder vetzuurmetabolisme en oxidatieve fosforylering, evenals signalen zoals PI3K/Akt/mTOR. Dezezelfde pathways zijn bekend als doelwitten die SARS-CoV-2 benut om zich te vermenigvuldigen, en ze ondersteunen ook energievretende immuuncellen zoals geactiveerde B-cellen. De studie vond dat het blokkeren van vetzuurmetabolisme, in ander experimenteel werk dat de auteurs aanhalen, de virale replicatie kan dempen. Samen suggereert dit dat hoge virale activiteit en een opgevoerd cellulair metabolisme kunnen bijdragen aan een krachtiger neutraliserende antilichaamrespons, ook al dragen ze bij aan ernstigere ziekte.
Hoe ziekte-ernst, eiwitten en antilichamen met elkaar vervlochten zijn
De eiwitten die aan ziekte-ernst waren gekoppeld overlappen slechts deels met die geassocieerd met sterke neutralisatie, wat wijst op verwante maar niet identieke processen. Bijvoorbeeld het chemokine CXCL13—eerder beschreven als een merker van ernstige COVID-19—was hoger bij patiënten die zuurstof nodig hadden. Toen de onderzoekers echter alle patiënten die zuurstof nodig hadden uit de analyse verwijderden, verdwenen vrijwel alle eiwitverschillen tussen hoge en lage neutraliseerders. Dit impliceert dat de biologie van ernstigere ziekte, waaronder hogere virusbelastingen en sterkere ontsteking, diep verweven is met de ontwikkeling van robuuste neutraliserende antilichamen, zelfs bij patiënten die nooit in de buurt van intensieve zorg komen.
Wat dit betekent voor het begrijpen van COVID-19-immuniteit
Voor de niet-expert is de belangrijkste conclusie dat onze vroege bloedchemie een vingerafdruk draagt van hoe krachtig we later beschermd zullen zijn door neutraliserende antilichamen na COVID-19. Eiwitten die betrokken zijn bij het tonen van virale fragmenten aan het immuunsysteem, het hervormen van cellulair metabolisme en het reageren op ontsteking blijken allemaal van invloed te zijn op deze uitkomst. Hoewel ernstige ziekte gevaarlijk en nooit wenselijk is, kunnen dezelfde processen die sommige mensen zieker maken hen ook helpen sterkere, langer durende bescherming op te bouwen. Het in kaart brengen van deze gastheer-eiwit- en pathway-signaturen kan uiteindelijk leiden tot vaccins of behandelingen die het immuunsysteem stimuleren om sterke neutraliserende antilichamen te produceren zonder dat mensen ernstige ziekte hoeven door te maken.
Bronvermelding: Khairallah, A., Jule, Z., Piller, A. et al. Host proteins associated with strong neutralizing SARS-CoV-2 antibody responses in a South African cohort. Commun Med 6, 203 (2026). https://doi.org/10.1038/s43856-026-01427-7
Trefwoorden: neutraliserende antilichamen, SARS-CoV-2, proteomics, gastheerimmuunrespons, COVID-19-ernst