Clear Sky Science · de
Wirtseiweße, die mit starken neutralisierenden SARS‑CoV‑2‑Antikörperantworten in einer südafrikanischen Kohorte assoziiert sind
Warum manche Menschen stärkere COVID‑abwehrende Antikörper bilden
Wenn Menschen das Virus bekommen, das COVID‑19 verursacht, bildet ihr Körper Antikörper, die das Virus daran hindern können, Zellen zu infizieren. Nicht alle produzieren diese wirksamen „neutralisierenden“ Antikörper jedoch im gleichen Ausmaß. Die Studie stellte eine einfache, aber wichtige Frage: Lassen sich schon bald nach der Infektion Hinweise im Blut ablesen, die vorhersagen, wer später besonders starke virusblockierende Antikörper entwickelt, und was verrät das über die Art und Weise, wie unser Körper SARS‑CoV‑2 bekämpft?
Patienten von der Krankheit bis zur Genesung begleiten
Forscher in Durban, Südafrika, begleiteten 71 erwachsene Patienten, die in der ersten COVID‑Welle hospitalisiert wurden, bevor Impfstoffe und bedeutende Varianten auftraten. Alle waren mit der ursprünglichen Form von SARS‑CoV‑2 infiziert und weder geimpft noch zuvor immunisiert. Blutproben wurden zweimal entnommen: erstmals etwa sechs Tage nach der Diagnose, während die Patienten noch akut erkrankt waren, und erneut etwa einen Monat später in der Genesungsphase. Frühe Blutproben wurden mit einer Hochdurchsatzmethode analysiert, die etwa 5.000 verschiedene Proteine im Blutplasma gleichzeitig messen kann. Spätere Proben wurden daraufhin geprüft, wie gut die Antikörper jeder Person lebendes Virus neutralisieren konnten und wie stark sie an das virale Spike‑Protein binden.
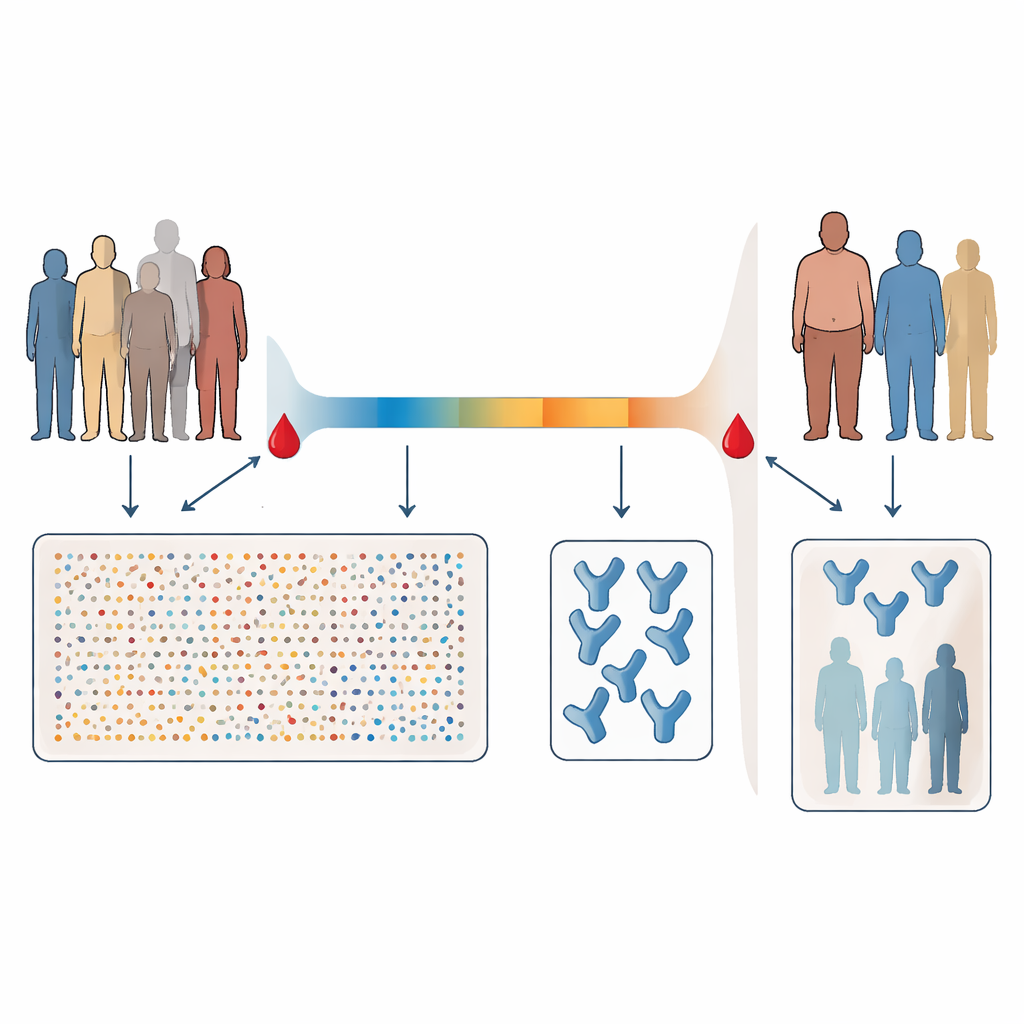
Krankheitsausprägung, Risikofaktoren und Antikörperstärke
Wie in vielen anderen Studien beobachtet, hatten Menschen mit schwererem Krankheitsverlauf tendenziell stärkere neutralisierende Antikörperantworten. Die Teilnehmenden wurden danach klassifiziert, ob sie jemals zusätzliches Sauerstoff benötigten, ein gängiger Marker für einen schwereren COVID‑19‑Verlauf. Personen mit Sauerstoffbedarf sowie ältere, männliche Teilnehmende oder solche mit Erkrankungen wie Bluthochdruck oder Diabetes gehörten häufiger zur Gruppe mit hoher Neutralisationskraft. Selbst unter Patienten, die nie Sauerstoff benötigten, waren subtilere Hinweise auf eine stärkere Erkrankung — etwa ein höheres Verhältnis von Neutrophilen zu Lymphozyten im Blut sowie dieselben Risikofaktoren — bei Menschen mit starken neutralisierenden Antworten häufiger. Das deutet darauf hin, dass selbst ohne Intensivpflege oder Beatmung ein etwas stärkerer Krankheitsverlauf oft mit potenteren Antikörpern einhergeht.
Frühe Proteinsignale, die starke Antikörper vorhersagen
Im Mittelpunkt der Arbeit stand das Muster der Proteine, die früh in der Infektion im Blut zirkulieren. Durch den Vergleich von Personen mit hoher und niedriger Neutralisationsaktivität sowie durch die Behandlung der Neutralisation als stetige Skala identifizierte das Team Hunderte von Proteinen, die zwischen den Gruppen variierten. Viele davon überschneiden sich mit Proteinen, die mit einfachen Spike‑bindenden Antikörpern assoziiert sind, aber ein Teil schien enger mit der Qualität der neutralisierenden Antwort verknüpft zu sein. Ein hervorgehobenes Protein war HSPA8, ein Mitglied der Hitzeschockprotein‑Familie, das anderen Proteinen beim Falten hilft und eine Schlüsselrolle dabei spielt, wie Immunzellen Virusfragmente Helfer‑T‑Zellen präsentieren. Höhere HSPA8‑Spiegel früh in der Infektion standen in starkem Zusammenhang mit besserer Neutralisationsaktivität später, und dieses eine Protein konnte allein schon hoher von niedriger Neutralisierungsstärke recht gut unterscheiden. In Kombination mit zwei weiteren Proteinen, FAP und MLN, verbesserte sich die Vorhersage weiter.
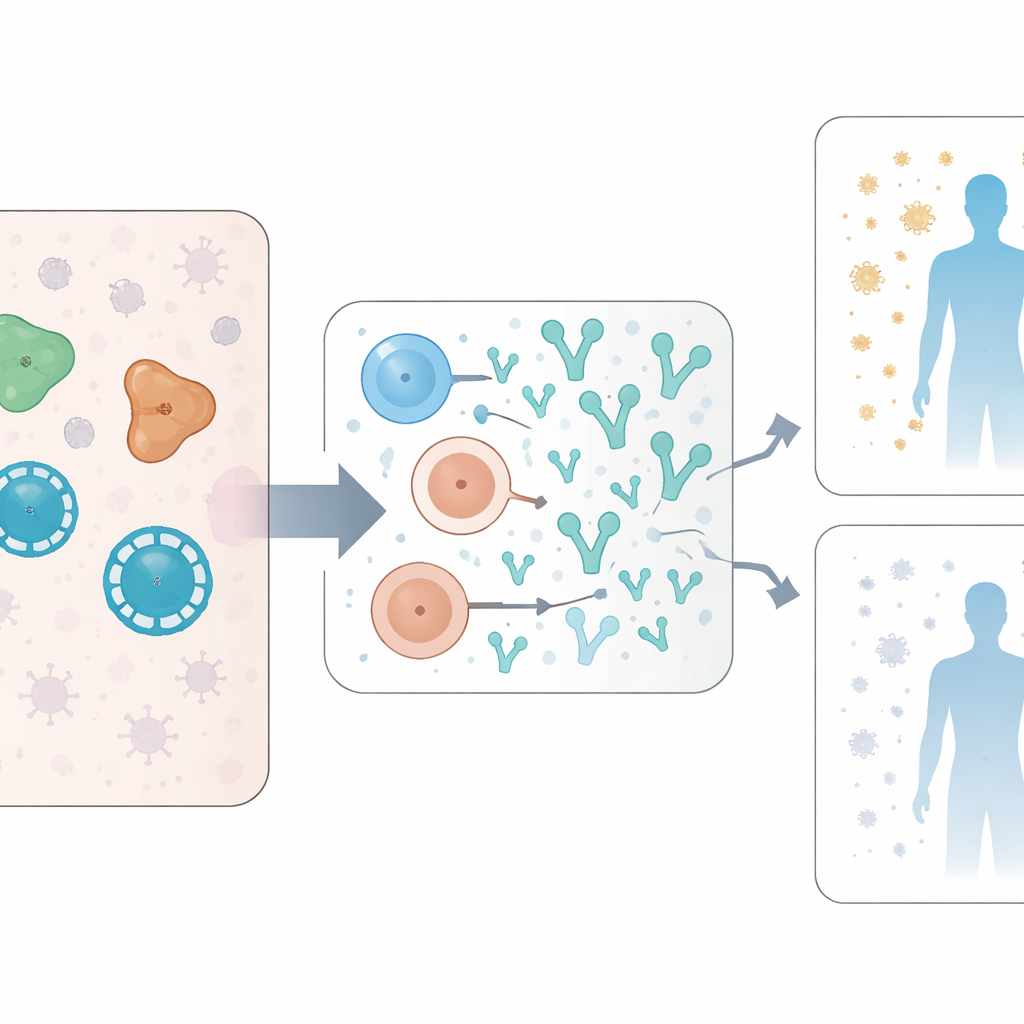
Signalwege, die Stoffwechsel, Infektion und Immunität verbinden
Über einzelne Proteine hinaus untersuchten die Forschenden ganze biologische Signalwege, die bei Personen aktiver waren, die später starke neutralisierende Antikörper entwickelten. Mehrere dieser Wege sind an der Art und Weise beteiligt, wie Zellen Energie und Fette verarbeiten, darunter der Fettsäurestoffwechsel und die oxidative Phosphorylierung, ebenso Signalwege wie PI3K/Akt/mTOR. Dieselben Wege sind dafür bekannt, von SARS‑CoV‑2 zur Replikation ausgenutzt zu werden, und sie unterstützen auch energieaufwendige Immunzellen wie aktivierte B‑Zellen. Die Studie zitiert experimentelle Arbeiten, die zeigen, dass die Blockade des Fettsäurestoffwechsels die Virusvermehrung dämpfen kann. Zusammengenommen deutet dies darauf hin, dass hohe Virusaktivität und ein hochgefahrener zellulärer Stoffwechsel eine stärkere neutralisierende Antikörperantwort begünstigen können, selbst wenn sie gleichzeitig zu schwererer Erkrankung beitragen.
Wie Schwere der Erkrankung, Proteine und Antikörper verflochten sind
Die mit dem Schweregrad assoziierten Proteine überschneiden sich nur teilweise mit denen, die mit starker Neutralisation verknüpft sind, was auf verwandte, aber nicht identische Prozesse hinweist. So war beispielsweise der Chemokine CXCL13 — zuvor als Marker für schweren COVID‑19 beschrieben — bei Patienten mit Sauerstoffbedarf erhöht. Als die Forschenden jedoch alle Patienten mit Sauerstoffbedarf aus der Analyse entfernten, verschwanden fast alle Proteinunterschiede zwischen hohen und niedrigen Neutralisierern. Das legt nahe, dass die Biologie schwererer Erkrankung, einschließlich höherer Viruslasten und stärkerer Entzündungsreaktionen, eng mit der Entwicklung robuster neutralisierender Antikörper verknüpft ist, selbst bei Patienten, die niemals in die Nähe intensivmedizinischer Betreuung kommen.
Was das für das Verständnis der COVID‑19‑Immunität bedeutet
Für eine sachlich interessierte Leserschaft lautet die wichtigste Erkenntnis: Unsere frühe Blutchimie trägt einen Fingerabdruck dessen, wie stark wir später durch neutralisierende Antikörper nach einer COVID‑19‑Infektion geschützt sein werden. Proteine, die daran beteiligt sind, virale Fragmente dem Immunsystem zu zeigen, den Zellstoffwechsel umzugestalten und auf Entzündungen zu reagieren, scheinen allesamt dieses Ergebnis zu beeinflussen. Während schwere Erkrankungen gefährlich und niemals wünschenswert sind, könnten dieselben Prozesse, die manche Menschen schwerer erkranken lassen, ihnen zugleich helfen, stärkeren und länger anhaltenden Schutz aufzubauen. Die Kartierung dieser Wirt‑Protein‑ und Signalweg‑Signaturen könnte letztlich dazu beitragen, Impfstoffe oder Therapien zu entwickeln, die das Immunsystem dazu bringen, starke neutralisierende Antikörper zu produzieren, ohne dass Menschen eine schwere Erkrankung durchlaufen müssen.
Zitation: Khairallah, A., Jule, Z., Piller, A. et al. Host proteins associated with strong neutralizing SARS-CoV-2 antibody responses in a South African cohort. Commun Med 6, 203 (2026). https://doi.org/10.1038/s43856-026-01427-7
Schlüsselwörter: neutralisierende Antikörper, SARS‑CoV‑2, Proteomik, Wirt‑Immunantwort, COVID‑19‑Schweregrad